70 Yaş Üzeri Hastalar İçin Meme Kanserinde Kriyoablasyona FDA Pazarlama Yetkisi Verdi
- ABD Gıda ve İlaç Dairesi (FDA), IceCure Medical’in geliştirdiği ProSense® kriyoablasyon sistemine 70 yaş ve üzeri düşük riskli erken evre meme kanseri hastalarında adjuvan endokrin tedavi ile birlikte kullanımı için 3 Ekim 2025'te pazarlama yetkisi (marketing authorization) verdi.
- Bu karar, kriyoablasyonu yalnızca araştırma düzeyinden çıkarıp, seçilmiş bir hasta grubunda resmi endikasyon haline getirdi.
- Ameliyat gerektirmeyen, günübirlik ve minimal invaziv bir yöntem olarak kriyoablasyon; hem cerrahi yükü azaltma, hem de kozmetik açıdan memeyi koruma avantajıyla, ileri yaştaki hastalara yeni bir tedavi seçeneği sunuyor.
- Dayanağını ICE3 klinik araştırmasının (NCT02200705) sonuçlarından alan bu gelişme, meme kanseri tedavisinde “de-eskalasyon” yaklaşımının en güçlü örneklerinden biri olarak görülüyor.
📌 Kısa Mesaj
Kriyoablasyon + endokrin tedavi, uygun seçilmiş 70+ yaş düşük riskli ER+/HER2− hastalarda FDA pazarlama yetkisine sahip bir seçenek oldu. Bu, approval (ilaç/cihaz onayı) ifadesinden farklı olarak endikasyon için pazarlama yetkisi verildiği anlamına gelir.
❄️ Kriyoablasyon Nedir?
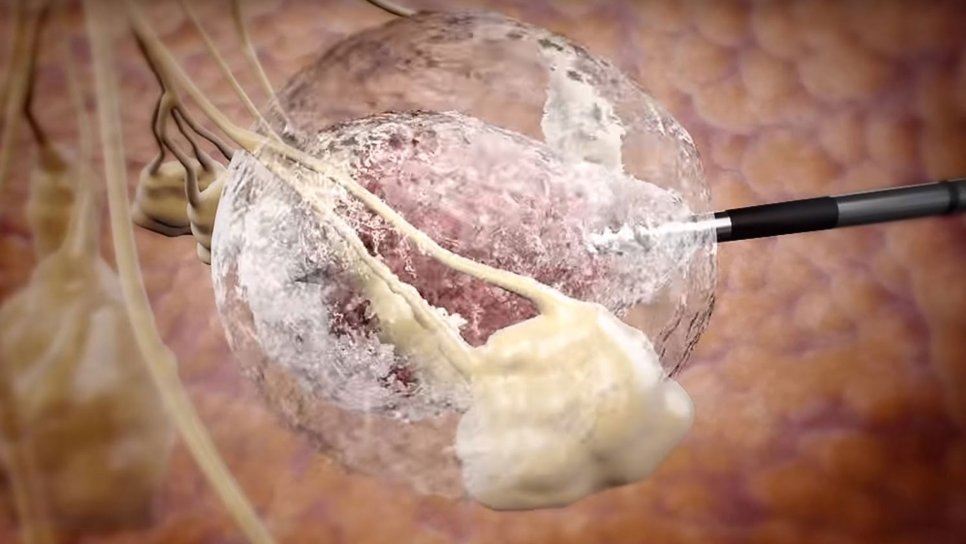
Kriyoablasyon, tümör dokusunun sıvı azot ile dondurularak yok edilmesi prensibine dayanan, ultrason eşliğinde uygulanan minimal invaziv bir tedavidir. İşlem sırasında oluşan “ice ball” (buz küresi), tümörü çevreleyip kanser hücrelerini geri dönüşsüz biçimde tahrip eder.
- Süre: Yaklaşık 20–30 dakika, çoğunlukla aynı gün taburculuk.
- Uygulama: Ofis/klinik ortamında, gerçek zamanlı görüntüleme ile.
- Kozmetik: Meme şeklini korur, belirgin ameliyat izi bırakmaz.
Bir sonraki parça: ICE3 çalışmasının sayısal sonuçları (IBTR, DFS, OS), yan etki profili ve hasta seçim kriterleri için görselleştirilmiş tablo ve kutular.
📊 ICE3 Çalışmasının Bulguları
FDA pazarlama yetkisi, ICE3 (NCT02200705) adlı çok merkezli faz-2 çalışmasının sonuçlarına dayanmaktadır. Çalışmaya 194 kadın dahil edildi (≥60 yaş, tümör ≤1.5 cm, ER pozitif, HER2 negatif).
| Parametre | Sonuç |
|---|---|
| Ipsilateral tümör tekrarı (IBTR) | %3.6 (7 hasta, 5 yılda) |
| 60 ay IBTR (Kaplan-Meier) | %4.3 (95% CI: %2.1–%8.7) |
| Hastalıksız sağkalım (DFS) | %92.8 |
| Meme kanserine özgü sağkalım | %96.7 |
| Genel sağkalım | %88.6 |
⚠️ Güvenlik Profili
Yan etkiler çoğunlukla hafif (CTCAE grade 1) düzeyindeydi.
- Morarma: %25.7
- İğne giriş yerinde ağrı: %20.9
- Lokal ödem: %19.3
- Orta şiddetli AE: %9.6
- Ciddi AE: %2.1
👩⚕️ Kimler İçin Uygun?
FDA pazarlama yetkisi belirli hasta grubunu kapsıyor:
- Yaş: 70 yaş ve üzeri
- Tümör boyutu: ≤1.5 cm, tek odaklı
- Moleküler profil: ER pozitif, HER2 negatif
- PR pozitiflik: %92.8
👉 Çok odaklı tümörler veya DCIS varlığında kriyoablasyonun etkinliği sınırlı. Bu nedenle hasta seçimi kritik öneme sahip.
🚀 Gelecek Perspektifi
FDA’nın pazarlama yetkisi, kriyoablasyonun meme kanseri tedavisinde “de-eskalasyon” stratejisinin güçlü bir temsilcisi olduğunu gösteriyor. Gelecekte bu yöntemin kapsamı daha da genişleyebilir.
- 🔍 Daha genç hasta gruplarında etkinlik ve güvenlik verilerinin değerlendirilmesi
- 🖥️ Gelişmiş görüntüleme teknikleri ile multifokal tümörlerin daha iyi saptanması
- 🧬 İmmünoterapi ve hedefe yönelik ilaçlarla kombinasyon araştırmalarının yapılması
- 🌍 Geniş ölçekli post-market çalışmalar ile gerçek yaşam verilerinin doğrulanması
📝 Sonuç
FDA’nın ProSense® kriyoablasyon sistemine verdiği pazarlama yetkisi, düşük riskli erken evre meme kanserinde ameliyatsız tedavi çağını başlatan tarihi bir adım olarak görülüyor.
Bu gelişme, doğru seçilmiş hastalarda cerrahi kadar etkin, daha az invaziv, kozmetik açıdan koruyucu ve hızlı iyileşme sağlayan yeni bir standart alternatifi gündeme taşıyor.
Klinik Pratiğe Yansıyan Mesajlar
- Endikasyon sınırları: Şimdilik sadece 70 yaş ve üzeri, düşük riskli (ER+, HER2−) hastalar için geçerli.
- Alternatif değil, seçenek: Cerrahi yerine değil, uygun hastalarda alternatif olarak sunuluyor.
- Kozmetik & konfor: Meme şeklinin korunması, hızlı iyileşme ve düşük yan etki profili.
- De-eskalasyonun örneği: Gereksiz cerrahi yükünü azaltan minimal invaziv yaklaşım.
🌟 Öne Çıkan
Kriyoablasyon + endokrin tedavi artık FDA pazarlama yetkisine sahip bir onaylı endikasyon. Bu, erken evre meme kanseri tedavisinde ameliyatsız yaklaşımların resmi olarak tanınmaya başladığını gösteriyor.
📚 Kaynaklar
- IceCure Medical. ProSense® Cryoablation granted FDA Marketing Authorization for treatment of low-risk breast cancer in women aged 70 and above. News release. . Erişim: . Bağlantı
- Fine RE, Gilmore RC, Tomkovich KR, et al. Cryoablation without excision for early-stage breast cancer: ICE3 trial 5-year follow-up on ipsilateral breast tumor recurrence. Annals of Surgical Oncology. 2024;31:7273–7283. DOI: 10.1245/s10434-024-16181-0
- ClinicalTrials.gov. Cryoablation of low risk small breast cancer — ICE3 trial. Güncelleme: . Erişim: . Kayıt sayfası