
Aksiyon Alınabilir Transkriptom: Hassas Onkolojide RNA Dizileme Rehberi
Hassas onkolojide DNA mutasyonlarının ötesine geçmek: RNA-seq verilerinin klinik karar destek süreçlerine entegrasyonu için yeni bir çerçeve.
Son on yılda hassas onkoloji, belirli kanser türlerine yönelik tedavilerden, tümörün histolojisinden bağımsız (histology-agnostic) moleküler biyobelirteç odaklı tedavilere doğru evrildi. NTRK füzyonları için larotrektinib, BRAF V600E mutasyonu için dabrafenib veya yüksek tümör mutasyon yükü (TMB-H) için pembrolizumab gibi onaylar bu dönüşümün en somut örnekleridir. Ancak sadece DNA dizileme (DNA-seq) kullanmak, buzdağının suyun altındaki kısmını gözden kaçırmamıza neden olmaktadır.
Neden RNA dizileme? DNA-seq ve IHC'nin eksik kaldığı noktalar
Proteinler, onkogenez sürecindeki hücresel aktivitelerin ana yürütücüleridir. Geleneksel olarak protein varlığı İmmünohistokimya (IHC) ile ölçülse de, bu yöntem genellikle tek bir biyobelirteci hedefler. RNA-seq ise yüzlerce geni aynı anda ve nicel (kantitatif) olarak değerlendirme kapasitesine sahiptir.
Birçok gen füzyonu DNA'daki intronik bölgelerde meydana gelir ve standart DNA-seq panelleri tarafından kaçırılabilir. RNA-seq, doğrudan ekzon birleşimlerine odaklandığı için aksiyon alınabilir füzyonları (NTRK, RET, FGFR2 vb.) çok daha yüksek hassasiyetle yakalar.
Antikor-ilaç konjugatları (ADC) ve CAR-T hücre tedavileri için hedeflerin (TROP2, HER3, Folat Reseptörü-α vb.) varlığı kritiktir. RNA-seq, bu hedeflerin tümördeki yoğunluğunu sayısal olarak vererek tedavi seçimini isabetli hale getirir.
MET ekzon 14 atlaması (skipping) gibi mutasyonlar, DNA düzeyinde karmaşık olsa da RNA düzeyinde net bir şekilde görülür. RNA-seq, bu kritik varyantların tespitinde DNA tabanlı testlerden istatistiksel olarak daha üstündür.
MammaPrint veya Oncotype DX gibi testlerin ötesinde, tümör mikroçevresinin immün durumunu veya homolog rekombinasyon eksikliğini (HRD) gösteren karmaşık RNA imzaları, prognostik ve prediktif birer pusuladır.
Aksiyon alınabilir transkriptom: klinik kullanım alanları
Araştırmacılar, RNA verilerinin tedavi kararlarında kullanılabilmesi için "aksiyon alınabilir transkriptom" listesi oluşturmuştur. Bu liste, DNA'da görülmeyen ancak RNA düzeyinde saptanan epigenetik değişimleri ve protein üretimindeki sapmaları hedefler.
| RNA Temelli Biyobelirteç | Klinik Kullanım ve Örnek | Hedeflenen Tedavi |
|---|---|---|
| Gen Füzyonları | FGFR2 Füzyonları (Kolanjiyokarsinom) | Pemigatinib, Futibatinib |
| Onkojen Aşırı İfadesi | MET RNA Aşırı İfadesi (NSCLC) | Kapmatinib, Tepotinib |
| Yüzey Antijenleri | TACSTD2 (TROP2) mRNA İfadesi | Sakitusumab Govitekan (ADC) |
| Tümör Baskılayıcı Kaybı | MTAP veya BRCA1 RNA Düşüklüğü | PRMT5 veya PARP İnhibitörleri |
| İmmün İmzalar | İnterferon-γ İmzaları | İmmün Kontrol Noktası İnhibitörleri |
Pan-kanser yaklaşımı ve benchmark analizi
RNA-seq'in en büyük zorluklarından biri, bir genin "yüksek" ifadesinin neye göre tanımlanacağıdır. Makale, bir tümörün RNA ifadesini sadece kendi türüyle değil, tüm kanser türlerini kapsayan geniş bir veri seti (TCGA Pan-Cancer gibi) ile kıyaslamayı önermektedir. Örneğin, meme kanserindeki ortalama TROP2 ifadesi referans alınarak, nadir bir kanser türünde bu düzeyde bir ifade saptanması, o hastanın bir ADC tedavisinden fayda görebileceğinin "isabetli" bir işareti olabilir.
RNA Kaynaklı Biyobelirteçlerin Hassas Onkolojideki Klinik Uygulamaları
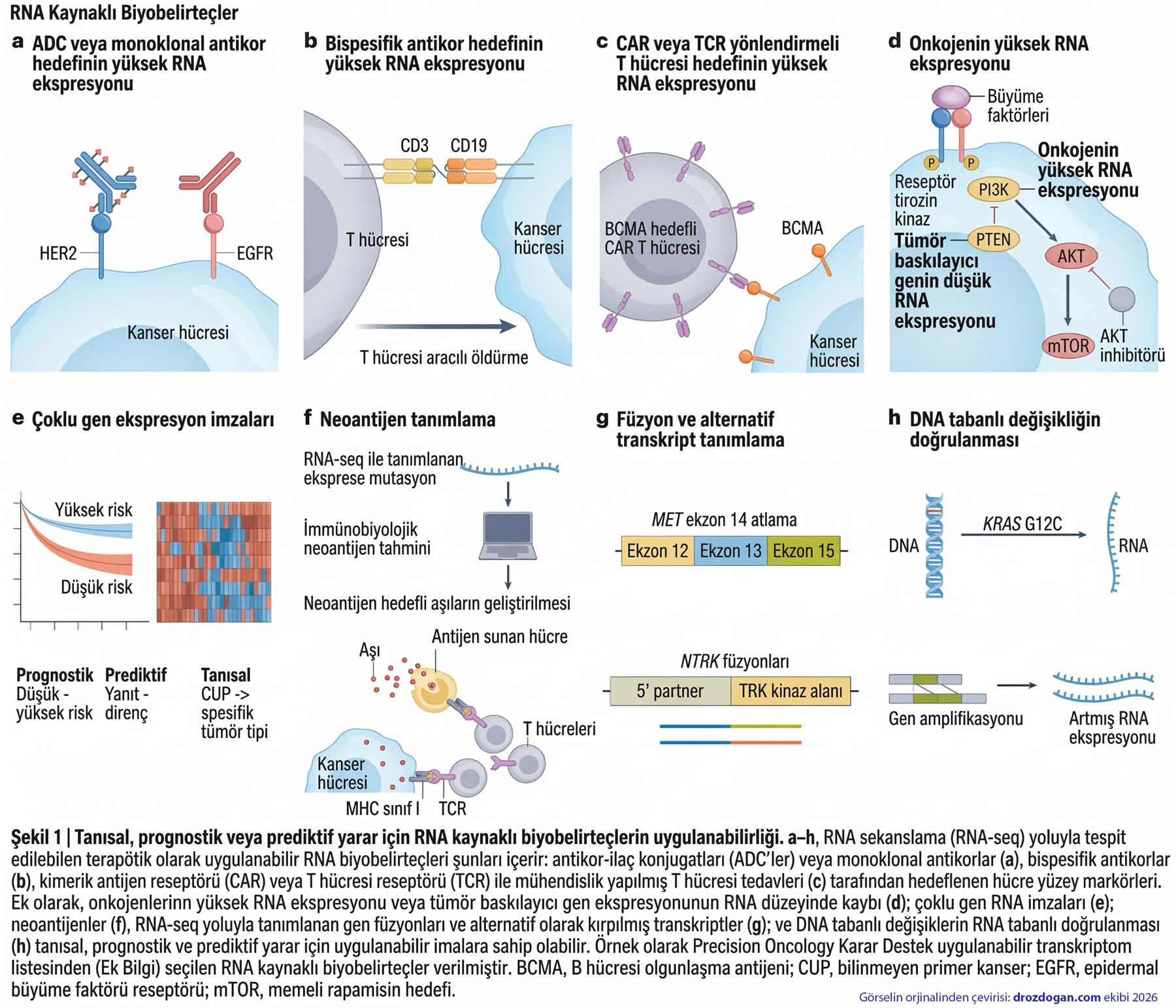
Aşağıdaki şekil, RNA sekanslamanın (RNA-seq) kanser hastaları için tanısal, prognostik ve prediktif kararları yönlendirmek üzere nasıl kullanıldığını özetlemektedir. Diyagram, antikor hedeflerinin belirlenmesinden (a-c) onkojenik yolak analizine (d), neoantijen tanımlamadan (f) ve gen füzyonlarının tespitine (g) kadar uzanan, her biri hassas tıp için kritik olan sekiz farklı klinik uygulama panelini (a-h) detaylandırmaktadır.
Aksiyon Alınabilir Transkriptomun Hassas Onkolojideki Rolü
Aşağıdaki şekil, kanser hastalarında tedavi seçimini yönlendirebilen aksiyon alınabilir biyobelirteçlerin (genomik değişiklikler, transkript imzaları, protein ekspresyonu vb.) tespiti amacıyla DNA-seq, RNA-seq ve IHC yöntemlerinin nasıl birleştirildiğini ve birbirini tamamladığını gösterir. Tespit edilen biyobelirteçlere göre hedefe yönelik tedaviler, immünoterapiler ve neoantijen hedefleri gibi en uygun terapötik aksiyonlar belirlenir.

Klinik iş akışına entegrasyon ve teknik zorluklar
RNA'nın DNA'ya göre daha kararsız bir molekül olması ve hızlı degradasyonu (parçalanması), klinik laboratuvarlar için en büyük engeldir. Ancak güncel teknolojiler (anchored multiplex PCR ve exome-capture mRNA-seq), parafine gömülü doku (FFPE) örneklerinden bile yüksek kaliteli RNA verisi elde edilmesini mümkün kılmıştır.
DROZDOGAN Akademi Yorumu
Kanserle olan şifa yolculuğumuzda yıllarca hücrenin "kitabını" (DNA) okuduk. Ancak bu makale bize şunu hatırlatıyor: Kitapta yazanlar kadar, hücrenin o sayfaları ne kadar yüksek sesle okuduğu (RNA) da önemlidir. Aksiyon alınabilir transkriptom, onkolojideki isabetli rehberlik vizyonumuzun bir sonraki dev adımıdır.
Biyoinformatik ile kliniğin bu muazzam kesişimi, bize daha önce "tedavi edilemez" veya "hedefsiz" dediğimiz hastalar için yeni pencereler açıyor. Biyolojik restorasyon; sadece mutasyonu yok etmek değil, hücrenin bozulan orkestrasını RNA düzeyinde yeniden hizalamaktır. Geleceğin onkolojisi, hücrenin sessiz çığlıklarını dahi duyabilen bu yüksek teknolojilerin şefkatli rehberliğinde inşa edilecektir.
Bilimsel Kaynaklar ve Referanslar
- 1. Johnson A, Meric-Bernstam F, et al. The actionable transcriptome: a framework for incorporating RNA sequencing into precision oncology. Nat Rev Clin Oncol. 2026;23:213-229. doi:10.1038/s41571-025-01110-1
- 2. Meric-Bernstam F, et al. ADC targets across various tumour types: TCGA Pan-Cancer analysis. Nature Medicine. 2024.
- 3. NCCN Guidelines v1.2026. Non-Small Cell Lung Cancer - RNA-based NGS fusion detection.






