Kanserle Mücadelede Yeni Bir Cephe: Hücre Yaşlanması (Senesens) ve Gizemli Rolü
Kanserle mücadelede her yeni bilgi, umut ışığı demektir. Geleneksel tedavi yöntemlerinin yanı sıra, kanserin karmaşık biyolojisini anlamaya yönelik devam eden araştırmalar, hastalığın farklı yönlerine ışık tutarak yeni tedavi stratejilerinin kapılarını aralıyor. Son zamanlarda bilim dünyasında büyük ilgi gören ve aslında vücudumuzun doğal bir süreci olan "hücre yaşlanması" veya bilimsel adıyla "hücresel senesens", kanser tedavisinde paradoksal ve potansiyel olarak çığır açıcı bir rol oynadığına dair güçlü kanıtlarla gündemde.
Bu yazıda, 14 Temmuz 2025'te Cancer Cell dergisinde yayımlanan "Senescence in Cancer" başlıklı son derleme makalesinden aldığım bilgilerle, senesensin kanserdeki bu gizemli ve çok yönlü etkisini, tümör mikroçevresiyle olan karmaşık ilişkilerini ve gelecekteki tedavi yaklaşımlarını derinlemesine inceleyeceğiz.
Hücresel Senesens: Doğal Bir Savunma Mekanizması mı, Yoksa İkili Bir Rol mü?
- Senesens, vücudumuzun hasarlı veya stresli hücrelerin kontrolsüz çoğalmasını engellemek için geliştirdiği doğal bir savunma mekanizmasıdır.
- İlk olarak 1961'de Hayflick ve Moorhead tarafından gözlemlenen bu durum, o zamandan beri hem tümör oluşumunu baskılayan önemli bir mekanizma hem de yaşlanmanın temel bir özelliği olarak kabul edilmektedir.
- Senesent hücreler (SnC'ler), programlı hücre ölümü (apoptoz) geçiren hücrelerin aksine, bölünmeyi duraksatırlar, ancak ölmezler.
- Bunun yerine, metabolik olarak aktif kalırlar ve bulundukları mikroçevreyi, özellikle de tümör mikroçevresini (TME) önemli ölçüde etkilerler.
- Kanser bağlamında senesens, paradoksal bir ikili rol oynar:
- Bir yandan, potansiyel olarak kötü huylu hücrelerin büyümesini durdurarak tümör gelişimini engelleyebilir.
- Diğer yandan ise, Senesensle İlişkili Salgı Fenotipi (SASP) adı verilen karmaşık bir salgı profili aracılığıyla tümör ilerlemesini kolaylaştırabilir.
📊 Kanser Hücrelerinin "Yaşlanma" Halleri: Senesensin Ayırt Edici Özellikleri
Senesent tümör hücreleri, aktif olarak çoğalmayan, ancak geri dönüşümlü olarak "uykuda" olan durgun tümör hücrelerinden temelden farklıdır. Senesent hücreler, genellikle hücre döngüsüne yeniden girmeye dirençlidirler. Bu durum, artık sadece kalıcı büyüme duraklamasıyla değil, bir dizi biyokimyasal, yapısal ve fonksiyonel özellikle tanımlanan daha geniş bir kavram olarak ele alınıyor:
- Kalıcı DNA Hasar Sinyalleşmesi: Onkojenik veya oksidatif stresin neden olduğu sürekli DNA hasarı.
- Kromatin Yeniden Modellemesi: Proliferatif genlerin heterokromatizasyonu.
- Metabolik Değişimler: Mitokondriyal disfonksiyon ve metabolik yeniden programlama.
- Apoptoza Direnç: Hücre ölümüne karşı artan bir direnç.
- Senesensle İlişkili Salgı Fenotipi (SASP): Senesent tümör hücrelerinin karmaşık salgı aktivitesi.
SASP: Tümör Mikroçevresinin Orkestra Şefi (SASPom)
- SASP, senesent hücrelerin en belirleyici özelliklerinden biridir ve tümör mikroçevresini (TME) derinden etkiler.
- SASP'nin salgı profili, sadece sitokinler ve interlökinlerle kalmayıp, ekstraselüler veziküller, kodlama yapmayan RNA'lar, biyoaktif lipidler ve diğer medyatörleri içeren geniş bir "SASPom" repertuvarını kapsar.
- Bu faktörler, senesent durumu hem otokrin (kendini pekiştirme) hem de parakrin (komşu hücreleri etkileme) yollarla güçlendirir.
- SASP, bağışıklık gözetimini modüle edebilir, doku yeniden modellemesini teşvik edebilir ve bağlama bağlı olarak tümör ilerlemesini veya baskılanmasını etkileyebilir.
⚠️ Kanserde Hücresel Senesensi Tetikleyen Faktörler
- Onkogen Kaynaklı Senesens (OIS): RAS gibi anormal onkogen aktivasyonu.
- Tümör Baskılayıcı Genlerin (TSG) Kaybı: PTEN, Rb gibi genlerin işlevini yitirmesi.
- Tedavi Kaynaklı Senesens (TIS): Kemoterapi, radyoterapi, hedefe yönelik tedaviler ve immünoterapi gibi birçok antikanser tedavisi.
- Telomeraz ve Epigenetik Yolların Hedeflenmesi: Telomeraz inhibitörleri ve epigenetik modülatörler.
- Hücre Döngüsü İnhibisyonu: CDK4/6 inhibitörleri (palbosiklib, abemasiklib, ribosiklib gibi).
Senesensin Kanserdeki İkilemi: Tümörü Baskılar mı, İlerlemesini Mi Sağlar?
2005 yılında yapılan çalışmalar, OIS'in kontrolsüz hücre çoğalmasına karşı bir tümör baskılayıcı bariyer olarak işlev gördüğünü gösterdi. Ancak, senesensin tümör ilerlemesine de katkıda bulunabileceği ortaya konuldu. Bu ikili rol, hücresel ve mikroçevresel faktörler arasındaki karmaşık etkileşime bağlıdır.
| Rol | Etkileri (Kanser Üzerine) | Mekanizma / Örnek |
|---|---|---|
| Tümör Baskılayıcı Etki |
|
|
| Tümör Destekleyici Etki |
|
|
Tümör Mikroçevresinde Senesens: Bir Kanser Havası
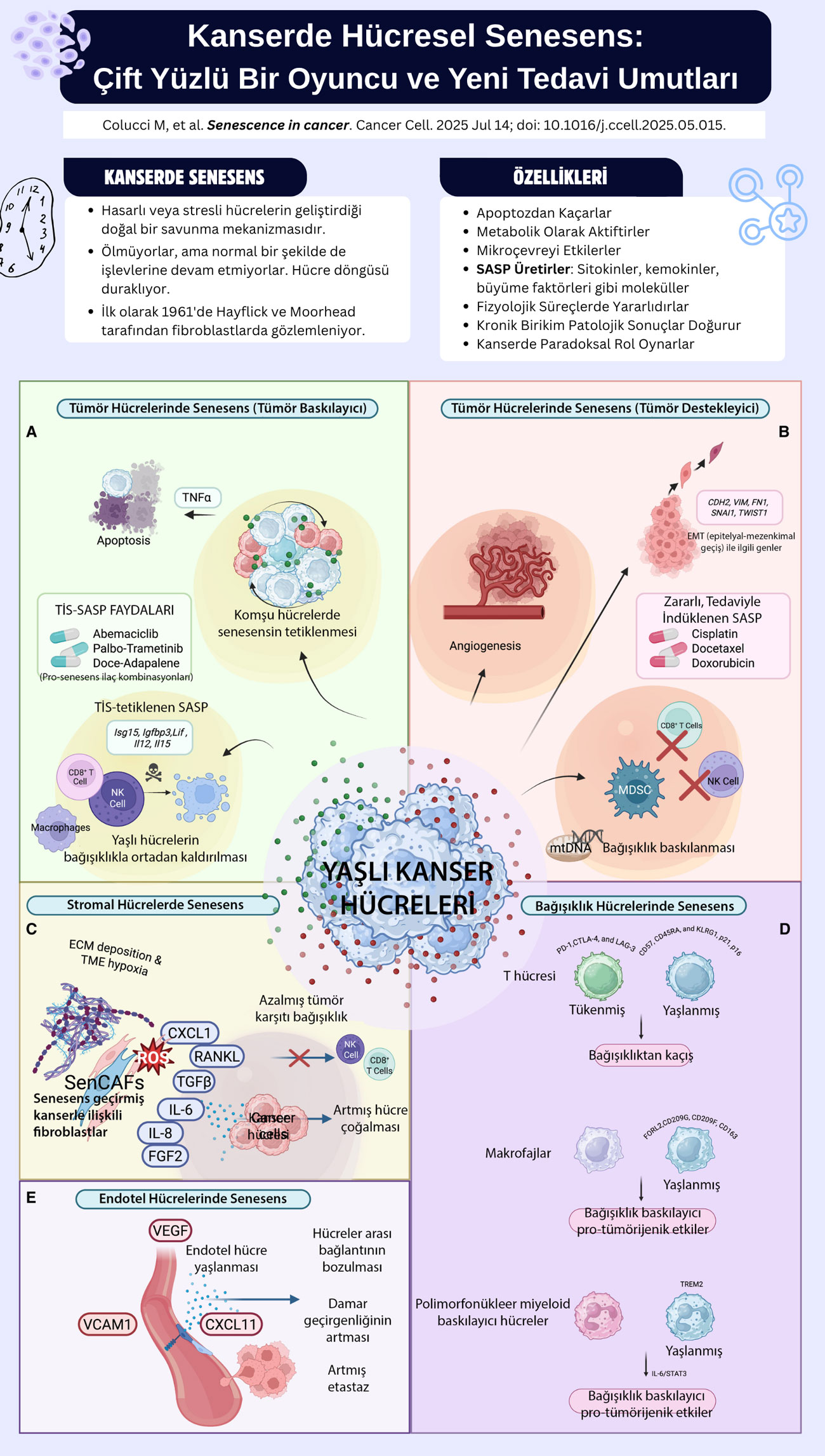
- Stromal Hücrelerde Senesens (SenCAFs): Kanserle ilişkili fibroblastlar (CAF'ler) senesens geçirebilir ve SASP'leri tümör büyümesini ve metastazı daha da kötüleştirebilir.
- Bağışıklık Hücrelerinde Senesens (İmmünosenesens): Bağışıklık sistemi yaşlanması, genel olarak kanser riskini artırır. Tükenmiş T hücreleri gibi hipofonksiyonel immün hücreler, tümör immün kaçışını kolaylaştırabilir.
- Damarsal Yapılarda Senesens (Endotel Hücreleri): Senesent endotel hücreleri, damar mimarisini bozar ve metastazı kolaylaştırır.
Kanser Tedavisinde Hücresel Senesensi Hedefleme Stratejileri
Hücre ölümü tek başına antikanser ajanların terapötik etkilerini tam olarak açıklamak için yeterli değildir; senesensin anahtar bir antiproliferatif mekanizma olarak kritik rolü göz ardı edilemez. Bu nedenle, senesensi hedeflemek onkolojide umut vadeden bir strateji haline gelmiştir.
| Strateji | Amaç | Örnek Bileşikler / Tedaviler |
|---|---|---|
| Pro-Senesens Bileşikleri (Senesensi Tetikleyenler) | Kanser hücrelerinde hücre döngüsü duraklaması indüklemek ve tümör büyümesini durdurmak. |
|
| Senolitik Bileşikler (Senesent Hücre Katilleri) | Tümörlerdeki senesent kanser hücrelerini seçici olarak yok etmek, tedavi direncini ve metastazı azaltmak. |
|
| Senomorfik Bileşikleri (SASP Modülatörleri) | SASP'yi baskılayarak veya yeniden programlayarak biriken senesent hücrelerin zararlı etkilerini azaltmak, anti-tümör fonksiyonlarını korumak. |
|
"Tek-İki Yumruk" Yaklaşımı: Senesensi Stratejik Olarak Kullanmak
Kanser tedavisinde "tek-iki yumruk" yaklaşımı, pro-senesens tedavileriyle tümörlerde senesens indüklenmesini, ardından senolitik tedavilerle senesent hücrelerin ortadan kaldırılmasını hedefler.
- Bu strateji, metastazı ve tedavi direncini azaltarak terapötik etkiyi artırma potansiyeline sahiptir.
- Örneğin, prostat kanserinde dosetakselin neden olduğu zararlı SASP, adapalen ile birleştirildiğinde anti-tümör faktörlerini artırarak NK hücre aktivasyonunu geliştirmiş ve tümör baskılanmasını iyileştirmiştir.
Hassas Tıp İçin Biyobelirteçler ve Yapay Zeka Desteği
- Yeni Tanımlama Araçları: Senesens Tanımlama Aracı (SIT), SENCAN, SenMayo ve DeepScence gibi araçlar, senesent hücreleri in vivo ve in vitro olarak tanımlama ve karakterize etme potansiyeli sunuyor.
- Yapay Zeka Destekli Patoloji: Genişlemiş hücre boyutu, kromatin reorganizasyonu gibi morfolojik özellikleri tanıyarak senesent hücreleri belirleyebilir. SAMP'ler, Deep-SeSMo ve SenPred gibi YZ araçları, senesens tespiti ve kanser risk tahmini için potansiyel sunmaktadır.
- Non-İnvaziv Tespit (Sıvı Biyopsi): Vücut sıvılarında SASP faktörlerinin tespiti, senesens için non-invaziv bir biyobelirteç olarak büyük umut vaat etmektedir.
Sonuç ve Gelecek Yönelimleri: Kansersiz Yarınlara Bir Adım Daha
Kanserde senesensin biyolojik ve genetik ortamı, etkilerinin faydalı mı yoksa zararlı mı olacağında belirleyici bir rol oynar. Tümör genomik yapısına dayalı tedavilerin kişiselleştirilmesi, kanser hücreleri üzerindeki terapötik etkiyi maksimize ederken, tümör mikroçevresi içindeki potansiyel sonuçları da tahmin etmeye yardımcı olacaktır. Bu kişiselleştirilmiş yaklaşımı desteklemek için, dolaşımdaki biyobelirteçler aracılığıyla senesens seviyelerinin izlenmesi, klinisyenlere tedavi kararlarını bilgilendirmek için eyleme dönüştürülebilir veriler sunabilir.
Ayrıca, immün hücrelerdeki senesens çalışmaları, immün gözetim, tümör ilerlemesi ve tedavi yanıtı için önemli çıkarımlar sunmaktadır.
Gelecekte, yapay zeka ve makine öğrenimi teknolojileri, senesent hücreleri tespit etmede, yanıtları tahmin etmede ve tedavi etkilerini izlemede kritik bir rol oynayacaktır. YZ tabanlı modeller, büyük ölçekli ve çok modlu veri kümelerini entegre ederek hücresel senesensi daha kapsamlı ve gelişmiş bir şekilde anlamamızı sağlayacak, böylece hassas tıbbın dönüşümüne yol açacaktır.
Colucci M, Sarill M, Maddalena M, Valdata A, Troiani M, Massarotti M, Bolis M, Bressan S, Kohl A, Robesti D, Saponaro M, Shi Q, Song P, Brina D, Calì B, Alimonti A. Senescence in cancer. Cancer Cell. 2025 Jul 14;43(7):1204-1226. doi: 10.1016/j.ccell.2025.05.015. Epub 2025 Jun 12. PMID: 40513577.






