PAXG (Sispilatin, Paklitaksel, Kapesitabin, Gemsitabin) Tedavi Protokolü
PAXG Nedir?
PAXG (Sisplatin, nab-paklitaksel, kapesitabin, gemsitabin), neoadjuvan (ameliyat öncesi) amaçla rezektabl, borderline rezektabl veya lokal ileri (metastazsız) pankreas duktal adenokarsinomu (PDAC) için kullanılan yoğun bir çoklu kemoterapi rejimidir. Klinik pratikte FOLFIRINOX’a alternatif bir seçenek olarak değerlendirilir.
🧭 Kanıt Durumu — Kısa Not
Ön sunumlara göre faz III CASSANDRA (ASCO 2025) çalışması, neoadjuvan PAXG’nin mFOLFIRINOX’a kıyasla olaydan arınmış sağkalımı (EFS) anlamlı uzattığını bildirmiştir. Genel sağkalım (OS) verileri henüz olgunlaşmamıştır ve kılavuz entegrasyonu netleşme aşamasındadır.
⚙️ Bileşenler & Etki Mekanizmaları
- C — Sisplatin (platin bileşiği): DNA’da çapraz bağ oluşturarak onarımı/çoğalmayı engeller → apoptoz.
- P — Paklitaksel (nab-paklitaksel) (taksan): Mikrotübülleri stabilize eder, depolimerizasyonu inhibe eder → G2/M fazında mitotik arrest ve apoptoz.
- X — Kapesitabin (oral 5-FU pro-ilacı): Tümörde 5-FU’ya dönüşür; timidilat sentazı inhibe ederek DNA/RNA sentezini bozar.
- G — Gemsitabin (nükleozid analoğu): dFdCTP’ye dönüşerek DNA’ya entegre olur; zincir uzamasını durdurur ve ribonükleotid redüktazı inhibe eder → çift mekanizma ile sitotoksisite.
🔗 Sinerji
- Platin kaynaklı DNA hasarı, antimetabolitlerle (gemsitabin/5-FU) birleşince replikasyon stresi artar.
- Taksan ile mitotik duraklama, DNA hasarının onarılamamasını kolaylaştırır.
- Oral kapesitabin, sürekli 5-FU maruziyeti sağlayarak rejimin doz yoğunluğunu destekler.
Amaç: tümör küçülmesini hızlandırmak, cerrahi rezektabiliteyi artırmak ve R0 rezeksiyon şansını yükseltmek.
🎯 Tedavinin Amacı
- Ameliyat öncesi tümör yükünü azaltmak: Neoadjuvan kullanımda tümör küçülmesini sağlayarak cerrahi şansını artırmak.
- Negatif cerrahi sınır (R0) oranını yükseltmek: Geride tümör bırakmadan rezeksiyon yapılabilmesini kolaylaştırmak.
- Lenf nodu tutulumu riskini azaltmak: N0 oranını artırarak uzun dönem sağkalımı iyileştirmek.
- Mikrometastazların erken baskılanması: Cerrahi sırasında/srasında uzak yayılım riskini azaltmak.
- CASSANDRA faz III verisi: Neoadjuvan PAXG, mFOLFIRINOX’a göre olaydan arınmış sağkalımı (EFS) anlamlı uzattı. Ancak genel sağkalım (OS) verileri henüz olgunlaşmamış olup, kılavuz entegrasyonu ilerleyen yayınlarla netleşecektir.
- CA19-9 biyobelirteçlerinde düşüş: Tedaviye yanıtın biyokimyasal göstergesi olarak önemli kabul edilir.
🧾 Tedavi Endikasyonu
- Rezektabl PDAC: Küratif cerrahi hedeflenen, damar teması minimal olgular.
- Borderline rezektabl PDAC: Sınırlı vasküler temas (ör. SMV/PV kısmi temas) olup teknik olarak rezeksiyon hedeflenebilen olgular.
- Lokal ileri (metastazsız) PDAC: Uzak metastaz yok; downstaging ile cerrahi şansı artırma hedefi olan seçilmiş olgular.
- Performans durumu: ECOG 0–1; yoğun çoklu kemoterapiyi tolere edebilecek genel durum.
- Organ fonksiyonları: Yeterli kemik iliği, böbrek ve karaciğer fonksiyon rezervi.
- Metastaz yokluğu: Karaciğer/akciğer/uzak metastaz saptanmamalıdır (BT/MR ± PET ile evreleme).
- Multimodal plan: Neoadjuvan tedavi → yeniden evreleme (görüntüleme + CA19-9) → uygunsa cerrahi; gerektiğinde radyoterapi. Kararlar multidisipliner konseyde alınmalıdır.
❗ Netleştirme
“İleri evre” terimi çoğu zaman metastatik hastalığı çağrıştırsa da, PAXG’nin kullanım bağlamı neoadjuvan amaçla lokalize (rezektabl/borderline) veya seçilmiş lokal ileri, metastazsız olgulardır. Metastatik PDAC’da amaç ve rejim seçimi farklılaşır.
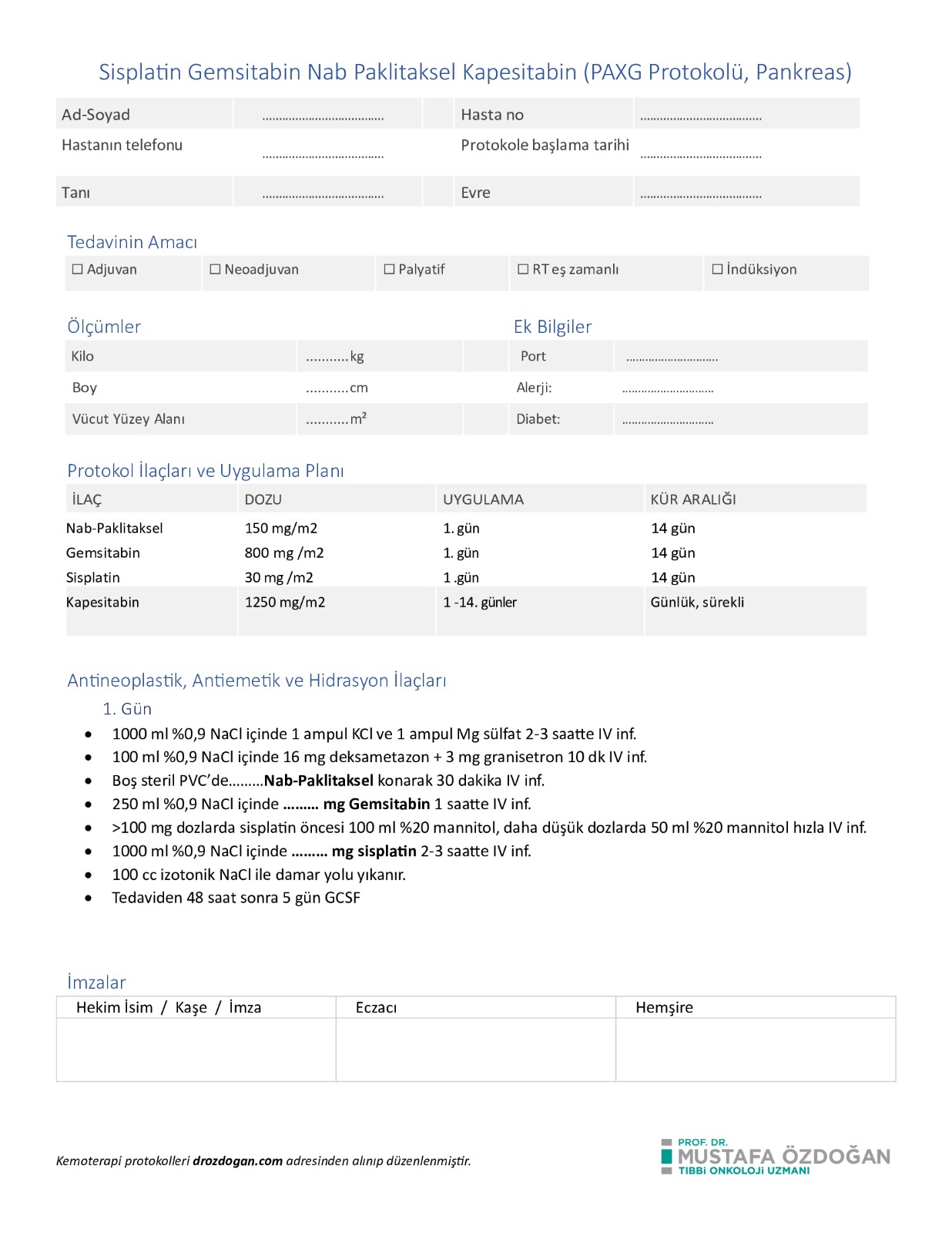
💉 Doz ve Premedikasyon
- Sisplatin: 30 mg/m² IV, 14 günde bir.
Hidrasyon: Güncel kısa-hidrasyon protokollerinde toplam 1.75–2.25 L IV sıvı (çoğunlukla 1 L pre + 1 L post); magnezyum/potasyum replasmanı önerilir. - Nab-paklitaksel (Abraxane): 150 mg/m² IV, 14 günde bir.
- Gemcitabin: 800 mg/m² IV, 14 günde bir.
- Kapesitabin: 1250 mg/m² oral, günde 2 kez.
🛡️ Premedikasyon
- Nab-paklitaksel: Alerji riski düşük; merkezine göre opsiyonel premedikasyon (dexametazon, antihistaminik, H2 bloker).
- Sisplatin: Zorunlu antiemetik + hidrasyon desteği (5-HT3 antagonisti ± NK1 antagonisti + dexametazon).
Uygulama planı: PAXG genellikle 14 günde bir, toplam 4 kür (8 hafta) uygulanır. Ardından görüntüleme + CA19-9 ile yanıt değerlendirilir ve uygun ise cerrahi planlanır.
⛔ Tedaviye Uygun Olmayan Durumlar
- Kötü performans durumu: ECOG ≥2 veya Karnofsky <70 olan hastalar (yoğun kemoterapiyi tolere edemez).
- Böbrek fonksiyon bozukluğu: Sisplatin nefrotoksiktir; kreatinin klerensi <60 mL/dk ise kontrendike olabilir.
- Kemik iliği rezervi yetersizliği: Lökosit, nötrofil, hemoglobin ve trombosit düşüklüğü olan hastalarda ciddi miyelosupresyon riski.
- Karaciğer fonksiyon bozukluğu: Paklitaksel, gemcitabin ve kapesitabin hepatik metabolize olur; bilirubin ve transaminaz yüksekliğinde dikkat gerekir.
- İleri yaş ve eşlikçi hastalıklar: Özellikle 75 yaş üzeri ve kardiyak, pulmoner, nörolojik komorbiditesi olan hastalarda toksisite artar.
- Daha önce platin/taksan bazlı tedavi almış olmak: Rezistans veya kümülatif toksisite riski.
- Şiddetli nöropati: Paklitaksel ve sisplatin nöropatiyi artırabilir; mevcut nöropatisi olan hastalarda semptomlar kötüleşir.
- DPD eksikliği: Kapesitabin (5-FU’ya dönüşür) kullanımı DPD eksikliğinde ciddi toksisite ve ölüm riski taşır.
- Gebelik ve emzirme: Tüm ajanlar teratojeniktir; kontrendikedir.
SGK Geri Ödeme Durumu
Türkiye’de PAXG (Sisplatin + Nab-Paklitaksel + Gemcitabin + Kapesitabin) kombinasyonu, ileri evre pankreas kanseri tedavisinde SGK kapsamında geri ödenmektedir.
Ancak Nab-Paklitaksel, ithal ilaç grubunda yer alır ve temini için:
- Sağlık Bakanlığı Endikasyon Dışı Onay Belgesi alınmalıdır.
- İlaç, TEB aracılığıyla Yurt Dışı İlaç Birimi üzerinden temin edilir.
→ Kısacası, rejim SGK kapsamında olsa da nab-paklitakselin tedarik süreci özel izin ve ithalat yoluyla gerçekleşmektedir.
💉 Doz Aralığı
- Sisplatin: 30 mg/m² IV, 14 günde bir.
- Nab-paklitaksel (Abraxane): 150 mg/m² IV, 14 günde bir.
- Gemcitabin: 800 mg/m² IV, 14 günde bir.
- Kapesitabin: 1250 mg/m² oral, günde 2 kez (merkez protokolüne göre süre/siklik değişebilir).
Uygulama planı: PAXG genellikle 14 günde bir olmak üzere 4 kür (8 hafta) uygulanır. Ardından görüntüleme + CA19-9 ile yanıt değerlendirilir; uygunsa cerrahi planlanır.
🛡️ Premedikasyon & Destek
- Sisplatin – antiemetik: 5-HT3 antagonisti ± NK1 antagonisti + deksametazon.
- Sisplatin – kısa hidrasyon (güncel): Toplam ~1.75–2.25 L IV (sıklıkla 1 L pre + 1 L post); Mg/K replasmanı önerilir. (Merkez protokolüne göre mannitol seçilmiş durumlarda eklenebilir.)
- Nab-paklitaksel: Aşırı duyarlılık riski düşüktür; merkezine göre opsiyonel premedikasyon (dexametazon, antihistaminik, H2 bloker).
📝 Küçük Protokol Notu
Kapesitabin süresi bazı merkezlerde “gün 1-7” veya “devamlı” şema ile uygulanabilir; hematolojik toksisite ve deri toksisitesine göre bireyselleştirilmiş doz/süre ayarı önerilir.
⚠️ Dikkat Edilmesi Gereken Durumlar
- Hematolojik toksisite: Lökopeni, nötropeni, anemi ve trombositopeni sık görülür. Her kür öncesi hemogram kontrolü yapılmalı, gerekirse G-CSF desteği eklenmelidir.
- Renal toksisite (Sisplatin): Kreatinin, üre, eGFR düzenli izlenmeli. Kısa hidrasyon: genellikle 1 L pre + 1 L post (%0.9 NaCl) + elektrolit desteği ile toplam ~1.75–2.25 L uygulanır. Hipomagnezemiye karşı magnezyum replasmanı önerilir.
- Gastrointestinal etkiler: Bulantı, kusma, mukozit ve iştahsızlık yaygındır. NK1 + 5-HT3 antagonisti + deksametazon içeren üçlü antiemetik rejim önerilir. Kapesitabin kullanılırken ishal ve ağız yaralarına dikkat edilmelidir.
- El-ayak sendromu (Kapesitabin): Eritrodisestezi belirtilerinde (kızarıklık, hassasiyet, soyulma) doz azaltımı veya ara verilmesi gerekebilir.
- Periferik nöropati: Özellikle nab-paklitaksel ve sisplatin ile. Uyuşma, karıncalanma artarsa doz modifikasyonu yapılmalıdır.
- Yaşlı / eşlikçi hastalıklar: ECOG ≥2 veya 75 yaş üstü olgularda toksisite riski artar. Daha düşük dozlar veya alternatif rejimler düşünülmelidir.
- İlaç etkileşimleri: Kapesitabin + varfarin (INR takibi zorunlu). Sisplatin + aminoglikozid/NSAİİ/kontrast maddeler nefrotoksisiteyi artırabilir.
- Beslenme durumu: Kaşeksi riski yüksek. Enteral/parenteral destek tedavisi planlanmalı.
- Tümör yanıt takibi: Tedavi sonrası BT/MR + CA19-9 değerlendirilmesi yapılmalı. Yanıt varsa cerrahi multidisipliner konseyde planlanmalıdır.
📊 Yan Etkiler
Klinik çalışmalarda PAXG rejimine bağlı bildirilen en sık yan etkiler ve görülme oranları aşağıdaki tabloda özetlenmiştir:
| Yan Etki | Sıklık (%) |
|---|---|
| Nötropeni (her derecede) | %40–60 |
| Febril nötropeni | %5–10 |
| Anemi | %30–50 |
| Trombositopeni | %20–30 |
| Periferik nöropati | %25–35 |
| Bulantı-kusma | %40–60 |
| İshal | %20–35 |
| Mukozit (ağız içi yaralar) | %10–25 |
| El-ayak sendromu | %15–25 |
| Yorgunluk | %40–60 |
| Alopesi (saç dökülmesi) | %30–40 |
| Hepatotoksisite (AST/ALT ↑) | %10–20 |
| Renal toksisite (kreatinin ↑) | %5–15 |
| Elektrolit bozuklukları (hipomagnezemi) | %10–20 |
| Enfeksiyon riski (nötropenik ateş dahil) | %5–10 |
Not: Yüzdeler Faz II–III klinik çalışmalardan (özellikle CASSANDRA ve İtalyan PAXG çalışmaları) derlenmiş ortalama verilerdir. Gerçek oranlar, hastanın performans durumu ve destek tedavisine göre değişebilir.
📚 Kaynaklar
- CASSANDRA Faz III Çalışması – Neoadjuvan PAXG ve mFOLFIRINOX karşılaştırması (ASCO 2025, oral sunum; OS verileri henüz olgunlaşmamış).
- Italian PAXG çalışma grubu: Nab-paklitaksel + gemcitabin + kapesitabin + sisplatin rejimi üzerine faz II klinik sonuçlar.
- Conroy T, et al. FOLFIRINOX or Gemcitabine as Adjuvant Therapy for Pancreatic Cancer. N Engl J Med. 2018;379:2395-2406. (karşılaştırmalı bağlam için).
- Oncologist. 2023 Nov 23;29(2):e173–e186. doi:10.1093/oncolo/oyad297 – Sisplatin kısa-hidrasyon protokolleri.
- NCCN Clinical Practice Guidelines in Oncology: Pancreatic Adenocarcinoma. Versiyon 2025.
Not: Burada özetlenen veriler, yayınlanmış çalışmalara ve uluslararası kılavuzlara dayalıdır. Klinik uygulama, hastanın performans durumu ve merkez deneyimine göre farklılık gösterebilir.






