Sarkomların Gizemli Kökenleri: Yumuşak Doku ve Kemik Sarkomlarında Patogenetik Faktörler
🔬 Sarkomlar: Nadir Ama Ciddi Kanserler
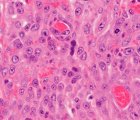
Sarkomlar, vücudun bağ dokularından köken alan nadir fakat agresif tümörlerdir. Kemikler, kaslar, yağ dokusu, sinirler ve damarlar gibi birçok yapıyı tutabilirler. Vakaların çoğu yumuşak doku kökenlidir; ancak bazıları kemiklerde gelişir.
Toplumda seyrek görülse de, sarkomlar hızlı yayılma eğilimi ve zorlayıcı tedavi süreçleri nedeniyle hem klinik hem de bilimsel açıdan büyük önem taşır.
🧬 Peki, Neden Ortaya Çıkıyorlar?
Vakaların çoğunda net bir neden gösterilemese de, birçok yatkınlaştırıcı faktör tanımlanmıştır:
- 🧬 Genetik yatkınlık ve kalıtsal sendromlar
- 🧪 Somatik gen mutasyonları
- ☢️ Radyasyon ve kemoterapi öyküsü
- 🌫️ Endüstriyel kimyasallara maruziyet
- 🦠 Kronik enfeksiyon ve tahriş
Bu yazıda, sarkomların karmaşık biyolojik kökenlerini ele alarak daha iyi tanı, risk değerlendirmesi ve hedefe yönelik tedavi yollarına ışık tutacağız.
İLGİLİ KONULAR:
- Sarkom Tanısında Histopatoloji ve İmmünohistokimya Birlikte Ne Anlatıyor?
- Sarkomlarda Genomik, Transkriptomik ve İmmünojenomik Analiz ve Yeni Tedavi Hedefleri
🧬 Genetik Yatkınlık: Kalıtımın Gölgesi Altındaki Sarkomlar
Bazı yumuşak doku ve kemik sarkomu hastaları, özellikle çocukluk yaş grubunda, doğuştan gelen genetik riskler taşır. Bu riskler bazen tanımlanmış kalıtsal sendromlara (örneğin Li-Fraumeni), bazen de henüz adı konmamış genetik varyasyonlara bağlı olabilir.
Yeni nesil dizileme teknolojileriyle yapılan çalışmalar, sarkom hastalarının yaklaşık %50’sinde kanser riskiyle ilişkili genetik mutasyonlar bulunduğunu göstermektedir.
🧬 Li-Fraumeni Sendromu: TP53 Geninin Mirası
Li-Fraumeni Sendromu (LFS), TP53 geninde kalıtsal mutasyon taşıyan bireylerde ortaya çıkar ve çocukluk çağında sarkom dahil olmak üzere çok sayıda kanser türüne yatkınlık oluşturur.
- Sarkom türleri: Osteosarkom, rabdomyosarkom, pleomorfik sarkom, liposarkom, leiomyosarkom
- Diğer kanserler: Meme kanseri, beyin tümörleri, lösemi, adrenal korteks tümörleri
- Mekanizma: TP53 mutasyonları, p53 proteinini işlevsiz hale getirerek DNA onarımını bozar ve tümör gelişimini hızlandırır.
🧬 Kalıtsal Sendromlar ve Sarkom Riski
🌿 FAP ve Gardner Sendromu: Bağırsağın Ötesindeki Risk
Familyal Adenomatöz Polipozis (FAP), kalıtsal bir bağırsak kanseri sendromudur. Ancak bu sendrom, sadece bağırsakları değil, intra-abdominal desmoid tümörler gibi yumuşak doku lezyonlarına da zemin hazırlar.
Bu tümörler, APC genindeki mutasyonlara bağlı gelişir ve sendrom, Gardner Sendromu olarak da adlandırılır. Desmoid tümörler genellikle metastaz yapmaz ama lokal agresif özellik gösterir.
👁️ Retinoblastom: Gözden Vücuda Yayılan Tehdit
Retinoblastom (RB), özellikle kalıtsal tipte ise, yaşamın ilerleyen dönemlerinde osteosarkom ve diğer yumuşak doku sarkomları açısından yüksek risk oluşturur.
RB1 genindeki mutasyonlar bu riski artırır. Ayrıca radyoterapi almak, ikinci bir sarkomun gelişme süresini kısaltabilir ve riskini yükseltebilir.
🔬 NF1 (Nörofibromatozis Tip 1): Sinir Kılıfından Kaynaklanan Tehlike
NF1 sendromu, Von Recklinghausen hastalığı olarak da bilinir ve NF1 geninde mutasyon sonucu gelişir.
Bu gen, hücre çoğalmasını düzenleyen Ras sinyal yolunu baskılayan nörofibromin proteinini kodlar. Mutasyonlar sonucu bu kontrol kaybolur ve malign periferik sinir kılıfı tümörleri (MPNST) gelişebilir.
🧩 Diğer Nadir Sendromlar
Rothmund-Thomson sendromu, otozomal resesif geçişli ve osteosarkom riskini artıran nadir bir sendromdur. Ciltte pigmentasyon bozuklukları, saç dökülmesi ve iskelet anomalileriyle karakterizedir.
🧬 Genetik ve Moleküler Patogenez: Hücresel Düzeyde Sarkom Anlayışı
Sarkomların genetik yapısı başlıca iki gruba ayrılır: spesifik genetik değişiklikler (örneğin füzyon genleri veya nokta mutasyonları) ve spesifik olmayan genetik değişiklikler (karmaşık, dengesiz karyotipler). Bu ayrım, tedavi hedeflerinin belirlenmesinde kritik önem taşır.
🔬 Somatik Gen Mutasyonları: Tümörün İçindeki Değişimler
Yumuşak doku ve kemik sarkomlarında yaşam boyunca edinilen somatik mutasyonlar sık görülür. Bu mutasyonlar, sarkomun alt tipine göre değişir. Örnek olarak:
- TP53 mutasyonu → Farklılaşmamış pleomorfik liposarkom
- NF1 mutasyonu → Miksofibrosarkom
- PIK3CA mutasyonu → Miksoid liposarkom
- MDM2, CDK4, HMGA2, YEATS4, SAS amplifikasyonları → Liposarkom
🧠 NF1: Ras yolunu baskılayan nörofibromin proteinini kodlar. Kaybı, malign sinir kılıfı tümörlerinde etkilidir.
📊 PIK3CA: PI3K enziminin alt birimidir. Miksoid liposarkomlarda daha kısa hastalıksız sağkalım ile ilişkilidir.
🛑 TP53: Hücre döngüsünü durdurur, apoptoz başlatır. Mutasyonu p53 işlev kaybına yol açar.
🔁 ATRX: Telomer uzunluğu korumada rol alır. Ekspresyon kaybı, alternatif mekanizmalara yönelimi gösterir.
🧬 RB1: Tümör baskılayıcıdır. Delesyonları, tümörleşmenin erken evrelerinde rol oynar.
🚫 MDM2: p53’ü inhibe eder. Amplifikasyonu, TP53 mutasyonlarına alternatif bir yol olarak sarkom gelişimini destekler.
🌀 CDK4: Hücre döngüsünü düzenler. MDM2 ile birlikte sık amplifiye edilir.
📎 YEATS4: Transkripsiyon faktörüdür. MDM2 ile birlikte amplifiye edilerek p53'ü baskılar.
🧵 HMGA2: Gen içi yeniden düzenlemelere uğrar. MDM2 ve CDK4 ile birlikte çalışarak yaşlanma karşıtı etki gösterir.
🧷 SAS (TSPAN31): CDK4 ile birlikte amplifiye olur. Sinyal iletiminde görev alabilir.
🧬 Kromozomal Translokasyonlar: Füzyon Genlerinin Gücü
Bazı yumuşak doku sarkomlarında tekrarlayan kromozomal translokasyonlar görülür. Bu translokasyonlar, genler arası füzyonlar oluşturarak tümör gelişimi ve devamlılığında rol oynayan anormal proteinlerin sentezine neden olur. Bu genetik imzalar, hem kesin tanı koymakta hem de tedavi hedefleri belirlemede önemlidir.
Ewing Sarkomu: %85-90 olguda t(11;22) → EWSR1::FLI1
Daha nadiren: EWSR1::ERG veya CIC::DUX4
Desmoplastik Küçük Yuvarlak Hücreli Tümör: t(11;22) → EWSR1::WT1
Miksoid Liposarkom: t(12;16) → FUS::DDIT3
Sinovyal Sarkom: t(X;18) → SS18::SSX1/SSX2/SSX4
Alveoler Rabdomyosarkom: t(2;13) veya t(1;13) → PAX3::FOXO1 / PAX7::FOXO1
Şeffaf Hücreli Sarkom: t(12;22) → EWSR1::ATF1
Alveoler Yumuşak Kısım Sarkomu: der(17)t(X;17) → ASPSCR1::TFE3
Ekstraiskeletal Miksoid Kondrosarkom: t(9;22) → EWSR1::NR4A3
Dermatofibrosarkoma Protuberans: t(17;22) resiprokal translokasyonu – Halka kromozomlarda
Soliter Fibröz Tümör: Kromozom 12q13 inversiyonu → NAB2::STAT6
Epitelyoid Hemanjioendotelyoma: t(1;3) → WWTR1::CAMTA1
🧬 Kromozomal İstikrarsızlık: Karmaşık Karyotiplerin Rolü
Yumuşak doku sarkomlarının yaklaşık üçte biri belirli bir translokasyon taşırken, geri kalan büyük kısmı karmaşık karyotiplere sahiptir. Genomik değişiklik sayısı arttıkça sarkomun histolojik derecesi de genellikle artar. Bu durum, daha agresif tümör özellikleri ve kötü prognoz ile ilişkilidir.
🧪 Tümör Sınıflandırması için Moleküler Genetik Testler
İmmünohistokimya, sitogenetik analiz ve yeni nesil dizileme (NGS) teknolojileri, yumuşak doku sarkomlarının tanı ve sınıflandırmasında kritik rol oynar. Özellikle füzyon genlerine yönelik testler, ayırıcı tanıya genetik temelli bir yaklaşım sunar.
Yakın gelecekte, gen ekspresyon profilleme gibi ileri moleküler teknikler sayesinde, hastalığın doğal seyri daha net tahmin edilebilecek; aynı zamanda hastaya özel hedefe yönelik tedaviler mümkün olacaktır.
💥 Radyoterapi ve Kemoterapi: Tedavinin Gölgesindeki Riskler
Radyoterapi (RT), hem yumuşak doku hem de kemik sarkomları için bilinen bir risk faktörüdür. RT’ye bağlı yumuşak doku sarkomlarının en sık görülen tipi farklılaşmamış pleomorfik sarkom (UPS), kemik sarkomlarında ise osteosarkom öne çıkar. Meme kanseri için RT alan kadınlarda en sık karşılaşılan ikincil sarkom ise kutanöz anjiosarkomdur.
Sarkom riski; radyoterapi dozu, maruziyet süresi ve yaş gibi faktörlere bağlı olarak değişir. Çocukluk çağı kanserlerinden kurtulan bireylerde bu risk daha yüksektir. Özellikle hem RT hem de antrasiklinler / alkilleyici ajanlar ile kemoterapi alanlarda görülme olasılığı artar. İkincil sarkomlar, primer sarkomlara göre daha kötü seyirli olabilir ancak potansiyel olarak tedavi edilebilir olmaları nedeniyle agresif tedaviye değerdir.
🌍 Endüstriyel Kimyasallar: Çevresel Faktörlerin Etkisi
Mesleki epidemiyoloji verileri sınırlı olsa da bazı kimyasal ajanlarla sarkom ilişkisi net olarak gösterilmiştir. Öne çıkan örnekler:
- Vinil klorür / Arsenik: → Hepatik anjiosarkom
- Fenoksi herbisitler: → Yumuşak doku sarkomu ile muhtemel ilişki
- Klorofenol türevleri: (ör. TCDD) → Maruziyet yüksekse sarkom riski artar
💡 Kronik Ödem, Tahriş ve Travma: Vücudun Yanıtı
Özellikle anjiosarkomlar, uzun süreli ödem sonrası gelişebilir. Bu durumun en klasik örneği, mastektomi sonrası lenfödemli kolda gelişen Stewart-Treves sendromudur.
Yabancı cisimlere bağlı kronik tahriş ve travmalar da desmoid tümörler ve diğer sarkomlarla ilişkilendirilmiştir. Travma sadece semptomları başlatan etken değil, bazı hayvan modellerinde tümör gelişimini tetikleyici bir unsur olarak da değerlendirilmiştir.
🦠 Viral Enfeksiyonlar: Görünmez Tehditler
Viral enfeksiyonlar nadiren sarkom gelişiminde rol oynasa da bazı örnekler dikkat çekicidir:
- HHV-8 (İnsan Herpes Virüsü 8): → Kaposi sarkomu patogenezinde
- EBV (Epstein-Barr Virüsü): → HIV/AIDS veya immünsüprese hastalarda düz kas tümörleri
✅ Sonuç
Yumuşak doku ve kemik sarkomları, genetik yatkınlıklar, somatik mutasyonlar, kromozomal translokasyonlar, radyoterapi, kemoterapi, kimyasal maruziyet ve kronik inflamasyon gibi birçok faktörün etkileşimiyle gelişen karmaşık hastalıklardır.
Moleküler genetik testler, bu nadir tümörlerin sınıflandırılmasında ve tedaviye yön vermede her geçen gün daha fazla önem kazanmaktadır. Bu bilgilerin ışığında kişiselleştirilmiş tedavi seçenekleri gelecekte daha da öne çıkacaktır.
Unutulmamalıdır ki, bu nadir kanserlerle mücadelede bilimin ışığında atılan her adım, hastalar için bir umut kaynağıdır.