
Gen Haritalama ve DNA Dizileme Nedir? Sonuçların Analizi ve Genetik Varyant Türleri
Kanser tedavisi, son yıllarda genetik bilimindeki olağanüstü ilerlemeler sayesinde kökten değişiyor. Gen haritalama ve DNA dizileme teknolojileri, her hastanın kanserine özel genetik değişiklikleri belirleyerek kişiselleştirilmiş tedavi yöntemleri geliştirilmesine olanak tanıyor. Peki, bu teknolojiler nasıl çalışır ve kanser tedavisinde neden bu kadar önemlidir? Gelin, bu soruları detaylı bir şekilde ele alalım.
Gen Haritalama ve DNA Dizileme Kavramları
Gen haritalama ve DNA dizileme/sekanslama farklı kavramlardır. Şöyle özetleyebiliriz:
-
Gen Haritalama: Genlerin bir kromozom üzerindeki yerlerini ve birbirlerine olan uzaklıklarını belirler. Daha genel bir harita sunar ve hastalıklarla ilişkilendirilen gen bölgelerinin bulunmasına yardımcı olur.
-
DNA Dizileme/Sekanslama: Genetik materyaldeki baz çiftlerinin (A, T, C, G) tam sırasını belirler. Gen haritalamadan daha ayrıntılıdır ve genlerin yapısını, mutasyonları ve varyasyonları tespit etmeyi sağlar.
Örnekle açıklarsak: Gen haritalama, bir kitabın içindeki bölümlerin hangi sırayla olduğunu anlamaktır; DNA dizileme/sekanslama ise, o kitabın tüm kelimelerini ve cümlelerini okumaktır.
DNA Dizileme Nedir?
DNA dizileme, bir organizmanın genetik materyalindeki baz çiftlerinin sırasını belirleme işlemidir. Bu işlem, kanser gibi karmaşık hastalıkların genetik temelini anlamak için kritik bir araçtır. Kanser hücreleri, sağlıklı hücrelerden farklı olarak genetik mutasyonlar içerir. Bu mutasyonları tespit etmek, doğru tedavi stratejilerini belirlemek için önemlidir.
DNA Dizileme Sürecinin Adımları
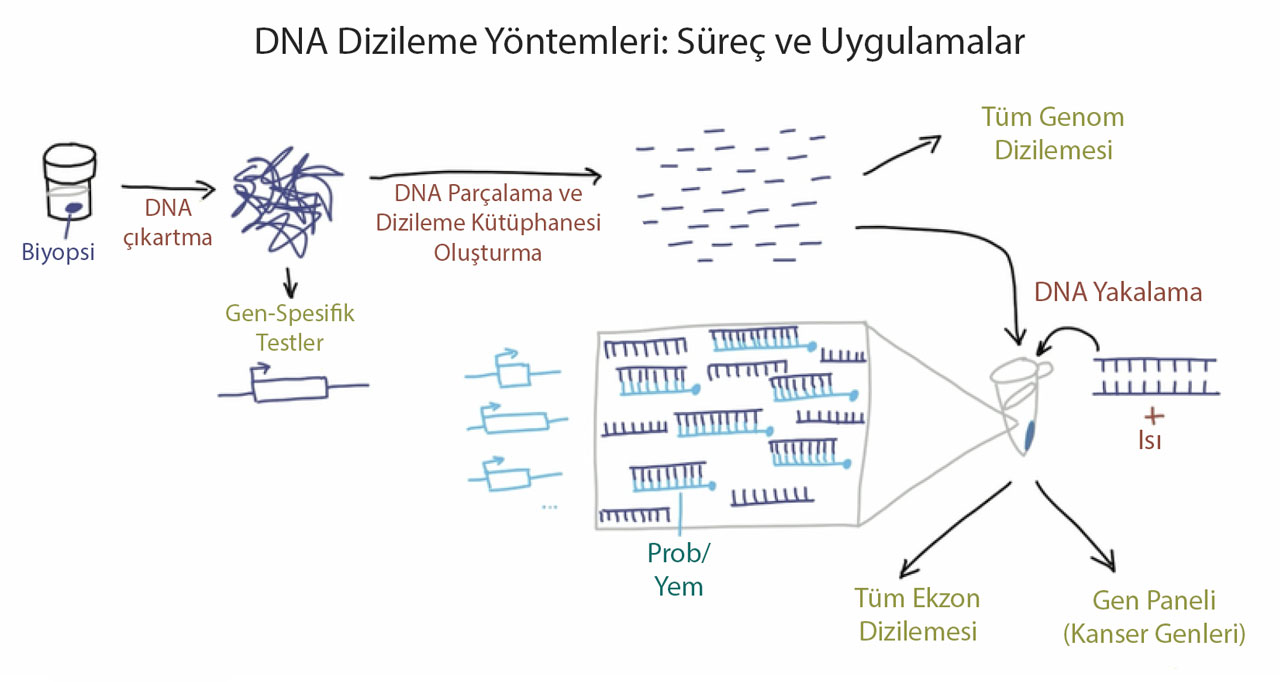
- DNA Ekstraksiyonu: İlk adım, kanser hücrelerinden DNA’nın saflaştırılmasıdır. Bu işlem, hücrelerin açılarak genetik materyalin izole edilmesiyle başlar.
- DNA Parçalama: Uzun DNA iplikçikleri, kısa fragmanlara ayrılır. Bu fragmanlar dizileme işlemini kolaylaştırır.
- Dizileme Kütüphanesi Hazırlama: DNA fragmanlarının uçlarına özel adaptörler eklenir ve bu adaptörler sayesinde dizileme cihazında işlem görecek hale getirilir.
- Dizileme: Dizileme cihazları, bu fragmanlardaki baz çiftlerini sırasıyla okur ve milyonlarca kısa okuma (read) oluşturur.
- Hizalama ve Analiz: Kısa okuma dizileri, referans genomla karşılaştırılır. Bu aşamada, genetik varyasyonlar (mutasyonlar) ve bunların biyolojik anlamları belirlenir.
NGS (Next-Generation Sequencing) Nedir ve Neden Önemlidir?
NGS, yani yeni nesil dizileme teknolojisi, genomik verilerin hızlı ve kapsamlı bir şekilde elde edilmesini sağlayan ileri düzey bir DNA dizileme yöntemidir. Geleneksel Sanger dizileme yöntemine kıyasla çok daha hızlı, yüksek kapasiteli ve düşük maliyetli bir çözüm sunar. Kanser araştırmalarında, NGS'nin sağladığı devrim niteliğindeki farkları şu şekilde özetleyebiliriz:
1. Hız ve Kapsam
NGS, aynı anda milyonlarca DNA fragmanını paralel olarak dizileyebilir. Bu, bir bireyin tüm genomunu analiz etmek için harcanan zamanı büyük ölçüde azaltır. Sanger dizileme ile yalnızca belirli bir gen üzerinde çalışılabilirken, NGS tüm genomu veya belirli gen panellerini aynı anda inceleyebilir.
2. Derinlik ve Hassasiyet
NGS, çok düşük miktarlarda bulunan genetik varyantları bile tespit edebilir. Bu, kanser gibi heterojen yapıya sahip hastalıklarda kritik öneme sahiptir. Örneğin, bir tümörde azınlıkta bulunan ve geleneksel yöntemlerle tespit edilemeyen mutasyonlar NGS ile kolayca belirlenebilir.
NOT: Genetik varyant, bir genin doğal genetik çeşitliliğini temsil eden ve genellikle zararsız olan DNA dizisi farklılıklarını ifade eder. Mutasyon ise, genetik materyalde meydana gelen ve genellikle hastalığa yol açabilen kalıcı bir değişikliği ifade eder; tüm mutasyonlar bir varyanttır, ancak tüm varyantlar mutasyon değildir.
NGS’nin Kanser Tedavisinde Yarattığı Değişim
NGS, kanser tedavisinde çığır açan bir teknoloji olarak kabul edilir. Çünkü hastalığın genetik temellerine inerek, yalnızca genel tedavilerle değil, bireye özel tedavi yaklaşımlarıyla sonuç elde edilmesini mümkün kılar. Bu sayede, geleneksel kemoterapi yerine daha etkili ve daha az yan etkiye sahip hedefe yönelik tedaviler veya immünoterapiler geliştirilebilmektedir.
Ayrıca NGS yalnızca kanserde değil, diğer hastalıkların (örneğin nadir genetik hastalıklar veya bulaşıcı hastalıklar) tanı ve tedavisinde de oldukça önemli bir rol oynamaya başlamıştır.
Tüm Genom Dizileme (Whole Genome Sequencing) ve Diğer Yaklaşımlar
Tüm genom dizilemesi, organizmanın tüm genetik materyalini analiz eder. Bu yaklaşım, kanser araştırmalarında sıkça kullanılsa da klinik ortamda her zaman en uygun seçenek değildir. Bunun nedeni, çok fazla bilgi üretmesi ve bu bilgilerin bir kısmının klinik anlamının olmamasıdır.
Daha Odaklı Yaklaşımlar
- Gen Panelleri: Yalnızca kanserle ilişkilendirilen belirli genlerin analiz edilmesi için kullanılır.
- Tüm Ekzon Dizilemesi (Whole Exome Sequencing): Protein kodlayan gen bölgelerini (ekzonlar) hedefler. Bu yöntem, daha düşük maliyetli ve klinik olarak daha uygulanabilir bilgiler sağlar.
- DNA Yakalama Teknolojileri: İlgi alanındaki genlerin izole edilmesi için kullanılır. Bu yöntem, hedeflenen genetik bölgeleri yüksek doğrulukla analiz etme imkanı sunar.
Kanser Tedavisinde Gen Dizilemenin Rolü
1. Hedefe Yönelik Tedavi Geliştirme
Gen dizileme sayesinde kanser hücrelerinde bulunan belirli mutasyonlar tespit edilebilir. Örneğin, EGFR mutasyonu taşıyan akciğer kanseri hastaları, bu mutasyonu hedefleyen tedavilerle daha iyi sonuçlar alabilir.
2. Kombinasyon Tedavilerinin Seçimi
Bir hastanın tümöründe birden fazla genetik değişiklik bulunabilir. Dizileme, hangi mutasyonların öncelikli tedavi edilmesi gerektiğini belirlemede yol gösterir.
3. Tedavi Direncini Anlama
Kanser tedavisine direnç geliştiren hastalarda, dizileme ile yeni mutasyonlar tespit edilerek tedavi stratejileri güncellenebilir.
4. Erken Tanı ve Risk Tahmini
Kalıtsal genetik mutasyonları taşıyan bireylerde (örneğin, BRCA1 ve BRCA2 gen mutasyonları), gen dizileme, kanser riskini belirlemede ve koruyucu önlemlerin alınmasında hayati bir rol oynar.
DNA Dizileme Teknolojilerinin Zorlukları
- Veri Yoğunluğu: Tüm genom dizilemesi, analiz edilmesi gereken büyük miktarda veri üretir.
- Maliyet: Gelişmiş teknolojilere rağmen, DNA dizileme hala yüksek maliyetlidir.
- Biyoinformatik Analiz: Üretilen verinin anlamlandırılması için güçlü yazılımlara ve uzmanlara ihtiyaç vardır.
- Etik Sorunlar: Genetik bilgilerin depolanması ve paylaşılması sırasında mahremiyetin korunması önemlidir.
Güncel Gelişmeler ve Gelecek Perspektifi
DNA dizileme teknolojileri sürekli gelişmektedir. Özellikle, daha hızlı ve düşük maliyetli dizileme cihazlarının geliştirilmesi, bu teknolojiyi daha erişilebilir hale getirmektedir. Gelecekte, kanser tedavisinde genetik bilgilerin daha kapsamlı ve rutin bir şekilde kullanılması beklenmektedir.
Öne Çıkan Yenilikler
- Sıvı/Likit Biyopsiler: Kan dolaşımındaki tümör DNA’sını analiz ederek invaziv olmayan tanı ve takip imkanı sunar.
- CRISPR Teknolojisi: Gen düzenleme araçlarıyla hastaya özel tedavi stratejileri geliştirilmesi hedeflenmektedir.
- Yapay Zeka Destekli Analizler: Büyük veri setlerinin yorumlanmasında daha etkin çözümler sunar.
Dizileme Sonuçlarının Analizi ve Varyant Tespiti
DNA dizileme, yalnızca genetik materyalin sırasını belirlemekle kalmaz, aynı zamanda bu dizilerdeki değişiklikleri tespit ederek hastalıkların genetik temelini anlamamıza olanak tanır. Dizileme sonrası analiz, genetik varyasyonların (mutasyonlar) belirlenmesi ve bu bilgilerin biyolojik anlamının çıkarılması açısından kritik bir süreçtir. Bu bölümde, dizileme sonuçlarının nasıl analiz edildiğini ve en yaygın varyant türlerinin nasıl tespit edildiğini ele alacağız.
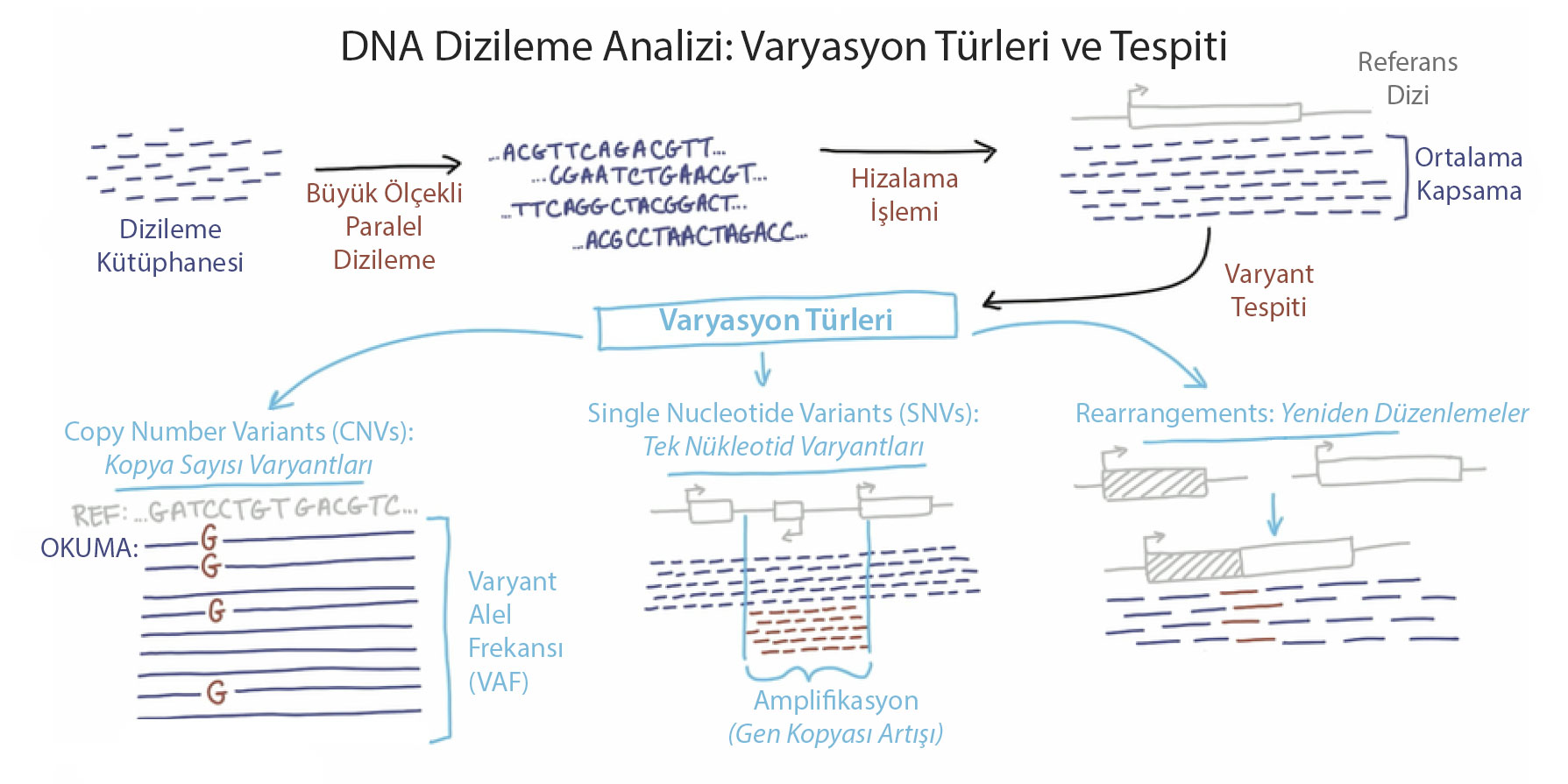
Yukarıdaki görsel, DNA dizileme analiz sürecini ve genetik varyasyon türlerini göstermektedir. Tek nükleotid varyantları (SNV), kopya sayısı varyantları (CNV) ve yeniden düzenlemeler gibi farklı varyasyon türlerinin nasıl tespit edildiği, dizileme kütüphanesinden başlayarak varyant tespiti sürecine kadar detaylandırılmıştır. Görsel, genetik verilerin hizalanması, ortalama kapsama ve varyasyon frekanslarının analizini görsel bir şekilde sunmaktadır.
Dizileme Sonuçlarının İlk İşlenmesi: Okuma ve Hizalama
Dizileme cihazları, kısa DNA fragmanlarından oluşan milyonlarca okuma (read) üretir. Bu okumalar, referans bir genom dizisiyle hizalanarak genetik varyasyonların tespit edilmesine olanak tanır. İlk adımlarda şunlar gerçekleştirilir:
- Hizalama (Alignment): Her bir okuma, referans genomdaki uygun konumuna yerleştirilir.
- Kapsama (Coverage): İlgi alanınızdaki genetik bölgenin her bir baz çiftinin kaç kez dizilendiğini ifade eder. Daha yüksek kapsama, daha güvenilir analizler sağlar.
- Filtreleme: Düşük kaliteli okumalar elenir ve analiz yalnızca yüksek kaliteli verilere dayanır.
Genetik Varyant Türleri
1. Tek Nükleotid Varyantları (Single Nucleotide Variants - SNVs)
SNV’ler, bir baz çiftinin yerini bir başka baz çiftinin almasıyla oluşan değişikliklerdir, tıpkı bir cümlede tek bir harfin değiştirilmesi gibi. Örneğin, referans genomda bir "C" bulunurken, analiz edilen dizide aynı pozisyonda "G" gözlemlenebilir. SNV’lerin tespitinde şu faktörler değerlendirilir:
- Varyant Alel Frekansı (VAF): Belirli bir varyantı içeren okumaların toplam okumalar içindeki yüzdesidir.
- Örneğin, bir bölgede 10 okuma varsa ve bunların 4'ü varyant içeriyorsa, VAF %40’tır.
- VAF’nin Önemi:
- Düşük VAF, somatik mutasyonlara işaret edebilir (örneğin, kanser hücrelerindeki mutasyonlar).
- Yüksek VAF, kalıtsal mutasyonların veya homozigot varyantların göstergesi olabilir.
2. Kopya Sayısı Varyantları (Copy Number Variants - CNVs)
Kopya sayısı varyantları, genetik materyalin belirli bölgelerinde kopya sayısındaki artış veya azalmaları ifade eder. Kanser hücrelerinde sıklıkla gözlemlenen bu varyantlar, hücrelerin büyüme ve bölünme hızını etkileyen genlerdeki değişimlerle ilişkilidir.
- Amplifikasyon: Belirli bir gen bölgesinde ekstra kopyaların bulunması. Örneğin, HER2 geninin amplifikasyonu, bazı meme kanserlerinde agresif bir seyirle ve hedefe yönelik akıllı ilaçlara uygunlukla ilişkilendirilir.
- Silinmeler: Genomun belirli bir bölgesinin kaybolması, tümör baskılayıcı genlerin inaktivasyonu ile sonuçlanabilir.
3. Yeniden Düzenlemeler (Rearrangements)
Yeniden düzenlemeler, genomun farklı bölgelerindeki DNA parçalarının birleştirilmesiyle oluşur. Bunlar, tersinmeler, translokasyonlar veya kromozomal parçaların daha karmaşık yeniden düzenlenmelerini içerebilir.
- Örnek: Gen Füzyonları
- EML4-ALK füzyonu, bazı akciğer kanserlerinde sıkça gözlemlenen bir yeniden düzenlemedir. Bu, iki genin birleşmesi sonucu oluşan bir onkogen (kanser yapan gen) örneğidir.
- Tespit Yöntemi:
- Yeniden düzenlemeler, dizileme okumalarının referans genomda beklenen konumlarına hizalanmamasıyla tespit edilir.
- Örneğin, bir okumanın bir ucu bir gene, diğer ucu ise başka bir gene hizalanırsa bu, iki gen arasında bir füzyonun göstergesi olabilir.
Varyantların Klinik Önemi
Dizileme sonrası tespit edilen her bir varyantın, hastalık süreçleri ve tedavi kararları üzerindeki etkisi değerlendirilir. Örneğin:
- Hedefe Yönelik Tedaviler: EGFR, KRAS veya BRAF gibi spesifik mutasyonlar, bu mutasyonları hedefleyen tedavi seçeneklerini belirler.
- Prognostik Değer: CNV’ler ve gen füzyonları, kanserin agresifliği ve tedaviye yanıtı hakkında ipuçları sağlar.
- Tedavi Direnci: Tedavi sırasında ortaya çıkan yeni SNV’ler veya CNV’ler, ilaca karşı direnç mekanizmalarını anlamada kritik rol oynar.
Sonuç
Gen haritalama ve DNA dizileme, kanser tedavisinde devrim niteliğinde bir değişim yaratmaktadır. Bu teknolojiler, her hastanın kanserine özgü genetik özellikleri belirleyerek, daha etkili ve kişiselleştirilmiş tedavi stratejileri sunar. Ancak, bu teknolojilerin etkin bir şekilde kullanılabilmesi için biyoinformatik altyapının güçlendirilmesi ve maliyetlerin düşürülmesi gerekmektedir. Gelecek, genetik bilimin kanser tedavisinde sınırları daha da zorlayacağı bir döneme işaret etmektedir.






