Jinekolojik Kanserlerde Paklitaksel, Karboplatin ve Bevacizumab Tedavisi
Karboplatin + Paklitaksel + Bevacizumab, başlıca epitelyal over kanseri, seçilmiş ileri/rekürren endometriyum kanseri ve persistan/rekürren/metastatik serviks kanseri olgularında kullanılan bir konvansiyonel kemoterapi + hedefe yönelik tedavi kombinasyonudur. Standart platin–taksan rejimine, tümör damar oluşumunu baskılayan anti-VEGF monoklonal antikor bevacizumab eklenmektedir.
Over kanserinde bu kombinasyon, başta GOG-0218 ve ICON7 olmak üzere faz 3 çalışmalarda; serviks kanserinde ise GOG-240 çalışmasında kemoterapiye ek bevacizumab ile progresyonsuz ve/veya genel sağkalımda anlamlı artış göstermiştir. Endometriyum kanserinde veriler daha sınırlı olup, faz 2 randomize MITO END-2 gibi çalışmalar kartopu niteliğindedir.
- Endikasyonlar (özet):
- Over: İleri evre (FIGO III–IV) epitelyal over, fallop tüpü ve primer periton kanseri – birinci basamak.
- Endometriyum: İleri evre veya rekürren, kemoterapi verilecek seçilmiş olgular (off-label / çalışma verileri).
- Serviks: Persistan, rekürren veya metastatik serviks kanseri – platin + paklitaksel ile (çoğu protokolde sisplatin veya karboplatin seçenekli).
- Tipik şema: 3 haftada bir kombinasyon; sonrasında bevacizumab ile idame tedavi (over/serviks için).
- Kemoterapiye bağlı hematolojik toksisite, nöropati ve alopesi.
- Bevacizumab’a bağlı hipertansiyon, proteinüri, tromboemboli ve nadiren GIS perforasyonu riski.
- Yakın takip, komorbidite yönetimi ve gerektiğinde doz modifikasyonu gerektirir.
- DFS/PFS’yi uzatmak, nüksü geciktirmek.
- Tümör yükünü azaltmak ve semptom kontrolünü sağlamak.
- Over/endometriyum için cerrahi ile birlikte uzun dönem sağkalımı artırmak; serviks kanserinde ileri evre/palyatif ortamda yaşam süresini uzatmak.
Temel endikasyonlar: Over, Endometriyum, Serviks
1. Over kanseri (epitelyal over, fallop tüpü, primer periton)
Over kanserinde karboplatin + paklitaksel + bevacizumab kombinasyonu, güncel kılavuzlara göre başlıca ilk tanılı ileri evre (FIGO III–IV) epitelyal over olgularında, birinci basamak sistemik tedavi seçeneği olarak değerlendirilir. Özellikle:
- Primer veya interval sitoredüksiyon sonrası suboptimal rezidü tümörü olan hastalar,
- Stage IV, büyük volümlü karın içi hastalık veya nodal/distant metastazlı olgular,
- Organ fonksiyonları ve performansı kombinasyonu tolere etmeye uygun hastalar
için güçlü bir seçenektir.
2. Endometriyum kanseri (ileri / rekürren)
Endometriyum kanserinde standart kemoterapi rejimi karboplatin + paklitaksel olup, bevacizumab eklenmesiyle ilgili veri başta MITO END-2 olmak üzere daha küçük faz 2 çalışmalara dayanmaktadır. Bu nedenle:
- İleri evre veya rekürren, kemoterapi planlanan seçilmiş olgularda,
- Özellikle yüksek tümör yükü veya belirgin vasküler komponenti olan hastalarda,
- Hasta ve merkez deneyimi, maliyet ve geri ödeme koşulları da göz önüne alınarak
off-label / kılavuz dışı bir seçenek olarak gündeme gelebilir. Klinik kararda hasta-hekim ortak kararı ve etik kurul/endikasyon dışı onay süreçleri önemlidir.
3. Serviks kanseri (persistan / rekürren / metastatik)
Serviks kanserinde, GOG-240 çalışmasıyla platin + paklitaksel kemoterapisine bevacizumab eklenmesi; persistan, rekürren veya metastatik hastalıkta genel sağkalımı uzatan ilk hedefe yönelik tedavi olarak tanımlanmıştır.
- Pelvik nüks, uzak metastaz veya radyoterapi sonrası persistan hastalık,
- Performans durumu iyi, organ fonksiyonları yeterli hastalar,
- GIS perforasyonu ve ciddi kanama riski düşük olan olgular
için uygundur. Protokollerde platin kolu sisplatin veya karboplatin olabilmekle birlikte; burada anlatım, over/endometriyum rejimiyle uyumlu olması için karboplatin üzerinden yapılmıştır.
Standart platin–taksan ile karşılaştırma
Uygun ve riskli hasta profilleri
- ECOG 0–1 performans durumuna sahip, sistemik tedaviyi tolere edebilecek hastalar.
- Over/endometriyumda ileri evre veya rekürren, servikste persistan/rekürren/metastatik hastalık.
- Kontrol altında hipertansiyonu olan ancak ağır kardiyovasküler olay öyküsü bulunmayan hastalar.
- Proteinürisi minimal veya yok, gastrointestinal perforasyon riski düşük olan hastalar.
- Ciddi, kontrolsüz hipertansiyon, yakın zamanda geçirilmiş inme veya ağır kardiyovasküler olay öyküsü olanlar.
- Belirgin proteinüri, böbrek fonksiyon bozukluğu veya tekrarlayan tromboemboli öyküsü.
- Yakın zamanda (<~28 gün) majör cerrahi geçirmiş ve yara iyileşmesi tamamlanmamış hastalar.
- Gastrointestinal perforasyon veya ciddi GIS ülser/kolit öyküsü olan, fistül riski yüksek hastalar.
Karboplatin
Karboplatin, platin türevi alkilleyici ajan olup, DNA üzerinde intrastrand ve interstrand çapraz bağlar oluşturarak replikasyon ve transkripsiyonu bozar; sonuçta apoptoza yol açar. Sisplatine göre genellikle daha az nefro- ve emetojenik, ancak belirgin miyelosupresif etki ile karakterizedir.
- Dozu çoğunlukla AUC bazlı (Calvert formülü ile GFR üzerinden) hesaplanır.
- Nötropeni ve trombositopeni, doz sınırlayıcı temel yan etkileridir.
Paklitaksel
Paklitaksel, taksan grubu mikrotübül stabilize edici ajandır. Mikrotübülleri stabilize ederek depolimerizasyonu engeller ve mitotik iğ oluşumunu bozar; hücreyi G2/M fazında arreste eder.
- Doza bağlı olarak periferik nöropati, alopesi, miyelosupresyon ve hipersensitivite reaksiyonları görülebilir.
- Hipersensitivite riskini azaltmak için steroid ve antihistaminik içeren premedikasyon gerektirir.
Bevacizumab
Bevacizumab, vasküler endotelyal büyüme faktörü (VEGF-A)’ya bağlanarak reseptörü ile etkileşmesini engelleyen rekombinant humanize monoklonal antikordur.
- Neoanjiojenezi ve tümör damar permeabilitesini azaltarak tümör büyümesi ve metastazı baskılamayı hedefler.
- Temel yan etkileri arasında hipertansiyon, proteinüri, tromboembolik olaylar, yara iyileşme sorunları ve nadiren GIS perforasyonu yer alır.
1. Over kanseri (GOG-0218, ICON7 ve diğerleri)
Birinci basamak over kanseri tedavisinde karboplatin + paklitaksel + bevacizumab kombinasyonunu değerlendiren iki temel faz 3 çalışma GOG-0218 ve ICON7’dir. Bu çalışmalarda:
- Bevacizumab’ın kemoterapi ile birlikte başlanıp sonrasında tek başına idame edilmesi; platin–taksan kemoterapisine kıyasla progresyonsuz sağkalımda anlamlı uzama sağlamıştır.
- Özellikle yüksek riskli ileri evre (suboptimal rezidü, stage IV) alt gruplarda fayda daha belirgindir.
- Toksisite profili öngörülebilirdir; doğru hasta seçimi ve yakın takip ile yönetilebilir.
2. Endometriyum kanseri (MITO END-2 ve seçilmiş veriler)
MITO END-2 faz 2 çalışmasında, ileri veya rekürren endometriyum kanserinde karboplatin + paklitaksel ile aynı rejime bevacizumab eklenmesi karşılaştırılmış; genel olarak tolere edilebilir ek toksisite ile yanıt ve PFS üzerinde iyileşme sinyalleri bildirilmiştir. Ancak:
- Çalışma faz 2 düzeyindedir; faz 3 onaylayıcı veri yoktur.
- Kılavuzlarda standart seçenek olarak yer almaz; daha çok seçilmiş olgular için off-label tartışılır.
3. Serviks kanseri (GOG-240 ve gerçek yaşam verileri)
GOG-240 faz 3 çalışması, persistan/rekürren/metastatik serviks kanserinde platin + paklitaksel kemoterapisine bevacizumab eklenmesinin; yalnız kemoterapi kollarına göre genel sağkalımı anlamlı derecede uzattığını göstermiş ve bu popülasyonda bevacizumab’ı standart hedefe yönelik ajan haline getirmiştir.
- Platin olarak sisplatin veya karboplatin kullanılabilmekte, sağkalım açısından anlamlı fark görülmemektedir.
- Türkiye’den gerçek yaşam çalışmalarında da (ör. metastatik/rekürren serviks kanserli kohortlar) kemoterapi + bevacizumab kombinasyonunun etkin ve tolere edilebilir olduğu bildirilmiştir.
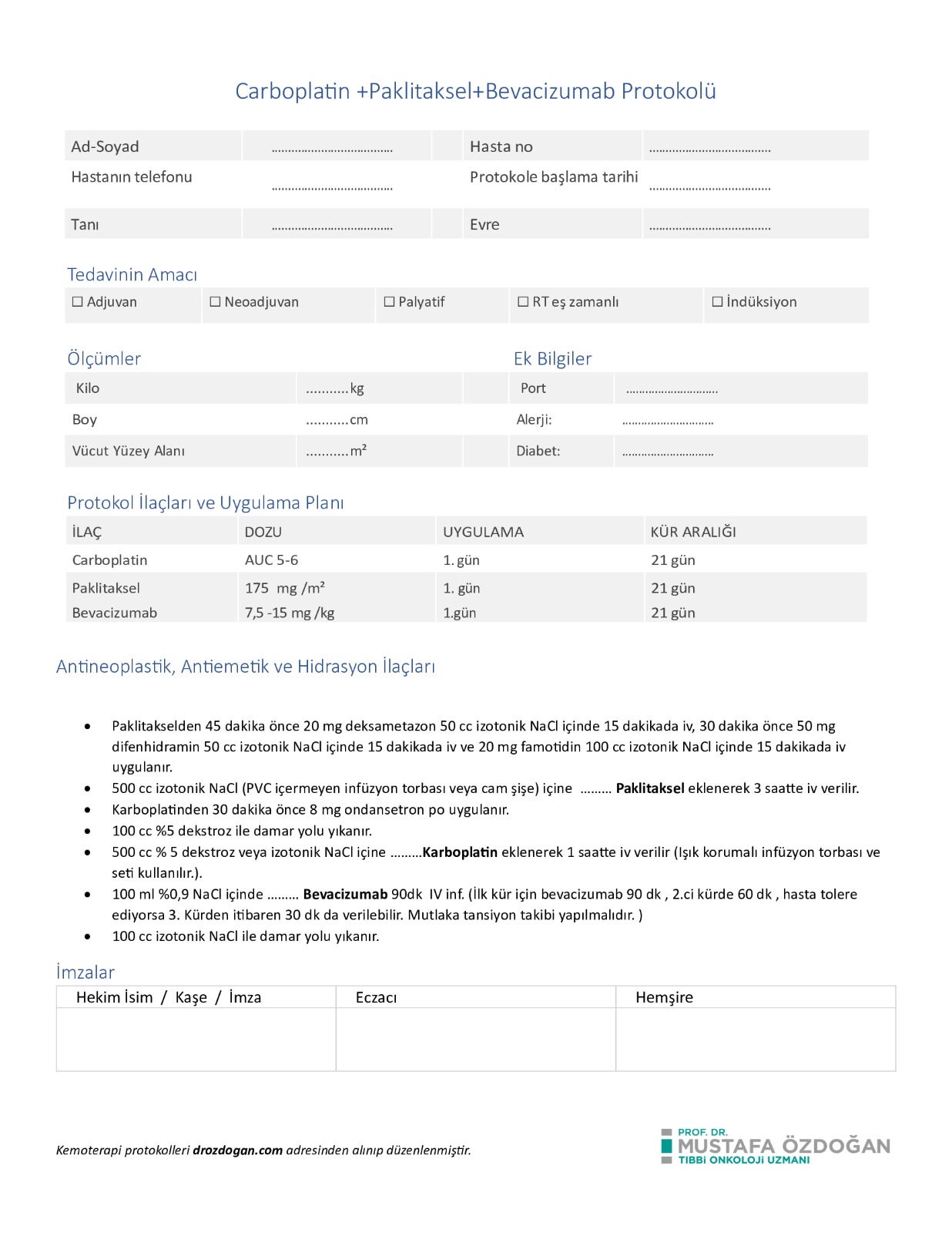
Over ve endometriyum kanserinde; serviks kanserinde ise GOG-240’a benzer protokollerde, 3 haftada bir (21 günde bir) uygulanan standart bir şema şu şekilde özetlenebilir:
- Gün 1
- Paklitaksel: 175 mg/m², yaklaşık 3 saatlik intravenöz infüzyon.
- Karboplatin: AUC 5–6 (Calvert formülü ile hesaplanır), IV infüzyon.
- Bevacizumab: 7,5-15 mg/kg IV infüzyon (kemoterapiyle birlikte başlanabilir veya bazı protokollerde ilk siklus sonrasında eklenebilir).
- Siklus sayısı: Genellikle 6 siklus (3 haftada bir) over ve serviks için; endometriyumda hasta ve merkez pratiğine göre değişir.
- İdame tedavi: Kemoterapi tamamlandıktan sonra bevacizumab, 3 haftada bir olacak şekilde, toplam tedavi süresi yaklaşık 12–15 aya tamamlanacak biçimde idame olarak devam ettirilebilir (over ve serviks için).
- Paklitaksel için: Hipersensitivite riskini azaltmak amacıyla kortikosteroid, H1 ve H2 blokörü içeren premedikasyon protokolü uygulanır.
- Bevacizumab için: İlk infüzyonda daha uzun süreli (yaklaşık 90 dakika), sonraki infüzyonlarda toleransa bağlı olarak daha kısa süreli infüzyon planlanabilir.
- Ön değerlendirme: Kan basıncı kontrolü, idrarda protein taraması, tam kan sayımı, böbrek ve karaciğer fonksiyonları, tromboemboli öyküsü ve yara iyileşme durumu mutlaka gözden geçirilmelidir.
A. Sık görülen yan etkiler
- Hematolojik: Nötropeni, anemi, trombositopeni; nadiren febril nötropeni.
- Nörolojik: Paklitaksele bağlı periferik nöropati (el–ayakta uyuşma, yanma, his kaybı).
- Genel: Yorgunluk, alopesi, bulantı–kusma, mukozit.
- Bevacizumab ilişkili: Hipertansiyon, proteinüri, baş ağrısı.
B. Ciddi / yaşamı tehdit edebilen yan etkiler
- GIS perforasyonu veya fistül: Ani başlayan şiddetli karın ağrısı, ateş, peritonit bulguları.
- Ağır hipertansiyon: Tedaviye dirençli yüksek kan basıncı, hipertansif kriz.
- Tromboembolik olaylar: Derin ven trombozu, pulmoner emboli, inme.
- Şiddetli proteinüri / nefrotik sendrom: Belirgin ödem, nefrotik aralıkta protein kaybı.
- Şiddetli miyelosupresyon: Grade 3–4 nötropeni, febril nötropeni, ciddi trombositopeni.
C. Yönetim stratejileri
- Hematolojik toksisite: Siklus erteleme, karboplatin/paklitaksel doz azaltımı, yüksek riskli hastalarda G-CSF profilaksisi, gerekirse eritrosit/trombosit transfüzyonu.
- Nöropati: Paklitaksel doz azaltımı veya tedaviye ara verme; ilerleyici nöropatide paklitakselin kesilmesi düşünülebilir.
- Hipertansiyon: Antihipertansif tedavinin optimize edilmesi; persistan veya ciddi hipertansiyonda bevacizumab doz aralığının uzatılması veya kesilmesi.
- Proteinüri: Düzenli idrar protein takibi; belirgin proteinüride bevacizumabın geçici veya kalıcı olarak kesilmesi.
- GIS perforasyonu şüphesi: Acil cerrahi ve multidisipliner değerlendirme; bevacizumab kesin olarak kesilir.
Karboplatin + paklitaksel + bevacizumab rejiminde doz ayarlamaları; hematolojik parametreler, organ fonksiyonları, toksisite dereceleri ve bevacizumab’a özgü riskler dikkate alınarak yapılır.
| Durum / Toksisite | Önerilen Yaklaşım (Genel Çerçeve) |
|---|---|
| Grade 3–4 nötropeni (febril olmayan) veya ciddi trombositopeni | Bir sonraki siklusu ertele; tam kan sayımı düzeldikten sonra karboplatin ve/veya paklitaksel dozunda yaklaşık %20 doz azaltımı düşün. Tekrarlayan tabloda G-CSF profilaksisi planlanabilir. |
| Febril nötropeni | Acil değerlendirme ve geniş spektrumlu antibiyotik tedavisi başlat; nötropeni düzeldikten sonra kemoterapi ajanlarında anlamlı doz azaltımı ve rutin G-CSF profilaksisi düşünülür. |
| Grade 2–3 periferik nöropati (paklitaksel ilişkili) | Paklitaksel dozunu kademeli azalt; ilerleyici veya günlük yaşamı belirgin etkileyen nöropatide paklitakseli kes ve gerekirse karboplatin + bevacizumab veya başka protokollere geç. |
| Şiddetli hipertansiyon (kontrolsüz) | Antihipertansif tedaviyi yoğunlaştır; kan basıncı kontrol altına alınana kadar bevacizumabı geçici olarak durdur. Persistan durumlarda bevacizumab kalıcı olarak kesilebilir. |
| Proteinüri >2 g/24 saat | Bevacizumabı geçici olarak kes; böbrek fonksiyonları ve proteinüri düzeyine göre yeniden başlatma veya kalıcı kesme kararı ver. |
| GIS perforasyonu, fistül veya ciddi kanama | Bevacizumab kalıcı olarak kesilir; cerrahi ve yoğun destek tedavisi gerekir. Kemoterapinin devamı, hastanın klinik durumuna göre yeniden değerlendirilir. |
| Genel performans durumunda belirgin bozulma (örn. ECOG ≥2) | Rejimin yoğunluğu yeniden gözden geçirilir; ajan sayısını azaltma, daha az yoğun şemalara geçiş veya sadece idame stratejisi/palyatif bakım seçenekleri değerlendirilir. |
Karboplatin + paklitaksel + bevacizumab, over, endometriyum ve serviks kanserlerinde seçilmiş hastalar için kullanılan güçlü bir kemoterapi + hedefe yönelik tedavi kombinasyonudur. Amaç, tümörü küçültmek, hastalığın yeniden büyümesini geciktirmek ve yaşam süresini uzatmaktır.
Tedavi genellikle 3 haftada bir verilir; birkaç kür kemoterapiden sonra, bazı hastalarda yalnızca bevacizumab ile idame tedavisi bir süre daha devam edebilir.
Bu süreçte:
- Yorgunluk, saç dökülmesi, bulantı, kan değerlerinde düşme,
- El ve ayaklarda uyuşma/karıncalanma,
- Tansiyon yükselmesi, idrarda protein artışı
gibi yan etkiler görülebilir. Ani nefes darlığı, göğüs ağrısı, şiddetli karın ağrısı, yüksek ateş veya kontrolsüz hipertansiyon gibi bulgular ortaya çıkarsa, vakit kaybetmeden hekime başvurmak büyük önem taşır.
- Karboplatin ve paklitaksel, Türkiye’de uzun süredir kullanılan standart kemoterapi ajanlarıdır.
- Over, endometriyum ve serviks kanserleri dahil olmak üzere yeri tanımlanmış endikasyonlarda, genellikle SUT listesinde yer alan ve SGK tarafından geri ödenen ilaçlardır.
- Doz ve kullanım koşulları, ilgili endikasyon ve SUT maddelerine göre değişebilir; her merkez kendi medula/sut kontrollerini yapmalıdır.
- Bevacizumab, Türkiye’de birden fazla kanser türünde ruhsatlı olmakla birlikte; Altuzan/Avastin ticari formlarının jinekolojik onkoloji endikasyonlarında SGK tarafından rutin geri ödemesi bulunmamaktadır. Ancak diğer eş değerleri SGK tarafından belli endikasyonlarda karşılanmaktadır.
Karboplatin + paklitaksel + bevacizumab, over ve serviks kanserinde etkinliği büyük faz 3 çalışmalarla gösterilmiş; endometriyum kanserinde ise daha sınırlı faz 2 verileri bulunan, yoğun fakat rasyonel bir kombinasyon tedavisidir.
Bununla birlikte, kombinasyonun içerdiği toksisite yükü ve bevacizumaba özgü riskler, ayrıca Türkiye’deki SGK geri ödeme kısıtları nedeniyle:
- Doğru hasta seçimi,
- Hipertansiyon, proteinüri ve tromboemboli açısından yakın izlem,
- Gerektiğinde zamanında doz modifikasyonları,
- Onkolojik, cerrahi, kardiyolojik, nefrolojik ve gerektiğinde hukuki/sosyal hizmet desteğini içeren multidisipliner yaklaşım
tedavinin başarısı açısından kritik önemdedir. Hastaya, tedavinin hedefleri, yan etkileri ve olası mali/idari süreçler hakkında şeffaf ve ayrıntılı bilgilendirme yapılması; hem uyumu hem de yaşam kalitesi üzerinde olumlu etki sağlayabilir.
- Perren TJ, et al. A Phase 3 Trial of Bevacizumab in Ovarian Cancer (ICON7). N Engl J Med; ilgili yıl ve cilt-sayı bilgileri ile.
- Burger RA, et al. Incorporation of Bevacizumab in the Primary Treatment of Ovarian Cancer (GOG-0218). N Engl J Med; ilgili yıl ve cilt-sayı bilgileri ile.
- Daniele G, et al. Bevacizumab, carboplatin, and paclitaxel in the first-line treatment of advanced ovarian cancer: multicenter deneyimler.
- Lorusso D, et al. MITO END-2: Carboplatin–Paclitaxel compared to Carboplatin–Paclitaxel–Bevacizumab in advanced or recurrent endometrial cancer. Gynecol Oncol 2019;155(3):406-412.
- Tewari KS, et al. Improved Survival with Bevacizumab in Advanced Cervical Cancer (GOG-240). N Engl J Med 2014;370:734-743.
- Godoy-Ortiz A, et al. Bevacizumab for recurrent, persistent or advanced cervical cancer: review of clinical evidence.
- Ercelep Ö, et al. Efficacy and safety of bevacizumab in Turkish patients with metastatic and recurrent cervical cancer. Turk J Obstet Gynecol 2020;17(2):123-127.
- NCCN Clinical Practice Guidelines in Oncology: Ovarian Cancer / Endometrial Carcinoma / Cervical Cancer. Güncel versiyonlar.
- ESMO Clinical Practice Guidelines: Newly diagnosed and relapsed epithelial ovarian carcinoma; Endometrial cancer; Cervical cancer.
- T.C. Sosyal Güvenlik Kurumu (SGK). Sağlık Uygulama Tebliği (SUT) ve “Geri Ödeme Listeleri”. Güncel çevrimiçi erişim.






