PIK3CA Mutasyonu İlişkili Aşırı Büyüme Spektrumu için Alpelisib FDA Onayı Aldı
Sistemik tedavi gerektiren ve şiddetli belirtiler gösteren PIK3CA ile ilişkili aşırı büyüme spektrumu (PROS) olan yetişkin ve 2 yaşından büyük pediatrik hastalar için alpelisib (Vijoice, Novartis) adlı akıllı ilaç, 5 Nisan 2022’de hızlandırılmış FDA (ABD Gıda ve İlaç İdaresi) onayı aldı.
Alpelisib etken maddesi daha önce 24 Mayıs 2019'da menopoza girmiş ve hormon reseptörü pozitif, HER2 negatif ileri evre veya metastatik ve PIK3CA mutasyonlu meme kanserli hastalar için hormonal tedavi ilacı fulvestrant ile birlikte Piqray kutu adı ile onaylanmıştı (bakınız ilgili onay).
PIK3CA ile İlişkili Aşırı Büyüme Spektrumu Nedir?
PIK3CA ile ilişkili segmental aşırı büyüme olarak da bilinen PROS (PIK3CA-Related Overgrowth Spectrum), genellikle PIK3CA genindeki somatik mutasyonlar nedeniyle vücut bölümlerinin aşırı büyümesine neden olan bir grup nadir hastalıktır. Tek bir hastalık değil bir grup hastalık olduğu için "spektrum" olarak adlandırılır. Bu bozukluklar şunları içerir;
- Fibroadipoz hiperplazisi (fibroadipoz aşırı büyümesi)
- Clove sendromu
- Megalensefali kılcal malformasyon sendromu (MCAP sendromu)
- Hemihiperplazi çoklu lipomatozis sendromu (HHML sendromu)
- Hemimegalensefali
- Yüze sızan lipomatozis (yüzün bir tarafının aşırı büyümesine neden olan doğuştan gelen bir bozukluk)
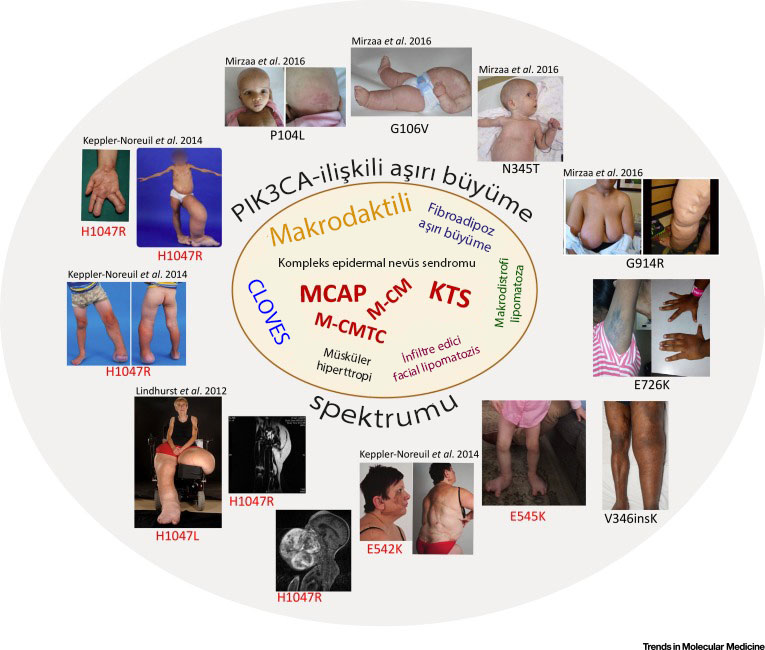
PROS’un belirtileri, ortaya çıkardığı duruma bağlı olarak değişiklik gösterir ve normalden daha büyük bir beyne (megalensefali), düşük kas tonusuna (hipotoni), nöbetlere, zihinsel engellere, kan damarlarında değişikliklere ve vücudun bir bölgesinin veya birden fazla bölgesinin aşırı büyümesine neden olabilir.
PROS için Alpelisibin Etkinliği
Alpelisibin etkinliği, bir başka hasta grubuna yardımcı olabilmesi umuduyla genişletilen erişim programı kapsamında alpelisib kullanan, 2 yaşından büyük hastalar ile yürütülen tek kollu klinik bir çalışma olan EPIK-P1'den elde edilen gerçek dünya verileri kullanılarak değerlendirildi.
PROS klinik belirtileri gösteren hastalar, tedavi sağlayan doktorlar tarafından şiddetli ya da yaşamı tehdit eden olarak sınıflandırıldı. Ayrıca PIK3CA geninde mutasyon olduğuna dair raporlandırmalar da vardı.
Alpelisibin etkinliği, ilk doz alımından önceki 24 hafta için yapılan görüntüleme testinde en az bir hedef lezyonu tanımlanmış toplamda 37 hastada değerlendirildi.
Sonuçlar
Ana etkinlik sonuç ölçütü, kör bağımsız merkezi radyoloji değerlendirmesi ile belirtildiği üzere 24. haftada radyolojik yanıta sahip hasta oranıydı. Bu oran, takiben en az 1 görüntüleme değerlendirmesi ile onaylanan 3 lezyona kadar ölçülebilir hedef lezyon toplamında başlangıca göre ≥%20’lik bir azalma olarak tanımlandı. Yanıt süresi, ek bir etkinlik sonuç ölçütüydü.
- Etkinlik popülasyonuna dahil 37 hastanın %27’sinde, 24. haftada radyolojik bir yanıt vardı.
- Yanıt verenlerin ise %60’ı uzun vadeli yanıta sahipti (12 ay veya daha fazla).
Hastalarda meydana gelen en yaygın (≥ %10) yan etkiler şunlardı;
- İshal
- Stomatit (ağı iltihabı)
- Hiperglisemi
Önerilen alpesilib dozu;
- 2 – 18 yaş arası pediatrik hastalarda günde bir kez, yemek ile oral olarak 50 mg.
- Klinik olarak belirtilirse 6 yaş ve üzeri pediatrik hastalarda 24. haftadan sonra doz, 125 mg’a yükseltilebilir.
- 18 yaşından büyük yetişkin hastalarda günde bir kez, yemek ile oral olarak 250 mg.
1. FDA approves alpelisib for PIK3CA-related overgrowth spectrum. Food and Drug Administration: https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-alpelisib-pik3ca-related-overgrowth-spectrum
2. NIH GARD Information: PIK3CA-related overgrowth spectrum. National Organization for Rare Disorders (NORD): https://rarediseases.org/gard-rare-disease/pik3ca-related-overgrowth-spectrum/