Tedaviye Direnç Gelişmiş EGFR-Mutant Akciğer Kanserinde Ivonescimab
IASLC Dünya Akciğer Kanseri Kongresi (WCLC25) · HARMONi Faz 3 çalışması
⚠️ Neden Önemli?
EGFR-mutant küçük hücreli dışı akciğer kanseri (KHDAK)'nda, üçüncü nesil TKI'ler sonraki aşamalar için etkili ve kalıcı tedavi seçenekleri sınırlıdır. PD-1/VEGF birleşikli antikor olan ivonescimab, kemoterapi ile birlikte, ilerlemeyi geciktiriyor (PFS) ve beyin metastazlı hastalarda da umut verici sinyaller gösteriyor.
Geliştirici firma: Çinli biyoteknoloji şirketi Akeso Inc. tarafından keşfedildi ve geliştirilmiştir. Uluslararası iş birliği: ABD merkezli Summit Therapeutics ile Kuzey Amerika, Avrupa ve Japonya dahil olmak üzere bazı bölgelerde geliştirme ve pazarlama hakları lisanslanmıştır.
Onay durumu: Akeso'nun pazara sunduğu ilk bispesifik PD-1/VEGF antikoru olan ivonescimab, 2024’te Çin NMPA tarafından EGFR-mutant NSCLC'de onaylanmıştır. Diğer bölgelerde (FDA veya EMA gibi) henüz onaylanmamıştır. Bununla birlikte, kılavuz niteliğinde fayda göstergesi nedeniyle FDA Fast Track statüsü almıştır.
Bu nedenle, ivonescimab hem mekanizması hem de klinik sonuçlarıyla KHDAK tedavisinde önemli bir potansiyele sahiptir ve global onay süreçlerinin tamamlanmasıyla başta TKI sonrası dönemde yer bulabilir.
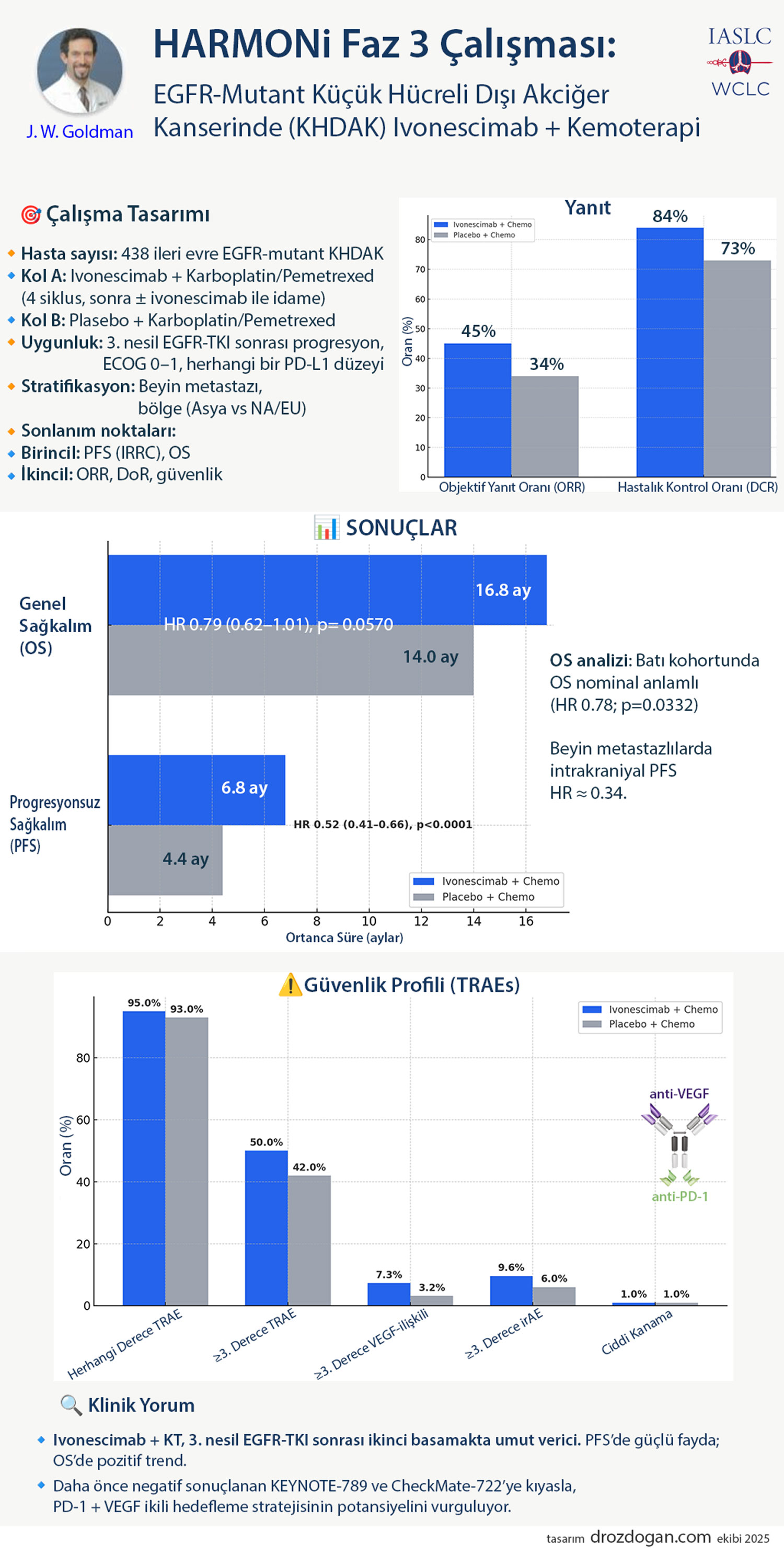
🧪 Çalışma Tasarımı (HARMONi, Faz 3)
- Popülasyon: 438 ileri/metastatik EGFR-mutant KHDAK hastası
- Randomizasyon (1:1): Ivonescimab (20 mg/kg Q3W) + Karboplatin/Pemetreksed (4 kür, sonra pemetreksed ± ivonescimab idame) vs Plasebo + Karboplatin/Pemetreksed
- Stratifikasyon: Beyin metastazı durumu; coğrafi bölge (Asya vs NA/EU)
- Birincil sonlanımlar: PFS (IRRC), OS
- İkincil sonlanımlar: ORR, DoR, güvenlik/tolerabilite
📊 Ana Bulgular
| Sonuç | Ivonescimab + KT | Plasebo + KT | HR (95% GA) | p-değeri |
|---|---|---|---|---|
| PFS (Birincil) | 6.8 ay | 4.4 ay | 0.52 (0.41–0.66) | <0.0001 |
| OS (Birincil) | 16.8 ay | 14.0 ay | 0.79 (0.62–1.01) | 0.0570 |
| ORR (IRRC) | 45% | 34% | – | – |
| DoR (medyan) | 7.6 ay (5.5–10.6) | 4.2 ay (2.9–4.7) | – | – |
| Hastalık Kontrol Oranı (DCR) | 84% | 73% | – | – |
Ek sinyal: Beyin metastazlı hastalarda intrakraniyal PFS HR ≈ 0.34. OS analizi toplu popülasyonda istatistiksel eşiği geçmese de Batı kohortunda nominal olarak anlamlı (HR ≈ 0.78; p≈0.0332) eğilim raporlandı.
⚠️ Güvenlik (TRAEs)
- Herhangi derece: %95 vs %93
- ≥3. derece: %50 vs %42
- ≥3. derece VEGF-ilişkili: %7.3 vs %3.2
- ≥3. derece irAE: %9.6 vs %6.0
- <%1 ciddi kanama; yeni güvenlik sinyali yok
🔍 Klinik Yorum ve Etki
- PFS’de %48 risk azalması (HR 0.52) klinik olarak anlamlı ve tutarlı.
- OS tüm popülasyonda sınırda; uzun dönem Batı takibinde nominal anlamlılık eğilimi mevcut.
- Beyin metastazlı hastalarda belirgin intrakraniyal fayda, gerçek yaşam pratiğinde değerli olabilir.
- Güvenlik profili, beklenen VEGF ve immün-ilişkili toksisitelerle yönetilebilir.
Alt metin: Bu sonuçlar, geçmişte negatif çıkan PD-1 + KT denemelerinden (KEYNOTE-789, CheckMate-722) farklı olarak, PD-1 + VEGF ikili hedefleme stratejisinin ikinci basamakta yeni bir standart adayına dönüşebileceğini düşündürüyor.
1. Goldman JW, Passaro A, Laskin J, et al. Ivonescimab vs placebo plus chemo, phase 3 in patients with EGFR+ NSCLC progressed with 3rd gen EGFR-TKI treatment: HARMONi. Presented at: International Association for the Study of Lung Cancer 2025 World Conference on Lung Cancer; September 6-9, 2025; Barcelona, Spain. Abstract 4808.
2. Ivonescimab plus chemotherapy demonstrates statistically significant and clinically meaningful improvement in progression-free survival in patients with EGFR-mutant non-small cell lung cancer after EGFR TKI therapy in global study. News release. Summit Therapeutics. May 30, 2025. Accessed September 7, 2025. https://www.smmttx.com/wp-content/uploads/2025/05/2025_PR_0530-_-HARMONi-Data-_-FINAL.docx.pdf
3. Phase III study of AK112 for NSCLC patients. ClincialTrials.gov. Updated October 8, 2024. Accessed September 7, 2025. https://clinicaltrials.gov/study/NCT06396065