
Yaşlanmanın ve Uzun Yaşamın Sırrı Genler Üstü Bağlantılarda Gizli
Bir süredir araştırmacılar yaşlanma sürecinin özellikle mutasyonlar olmak üzere DNA değişikliklerinin birikmesinden kaynaklandığı teorisini üzerine kafa yormaktadır. Biriken mutasyonlar daha sonra doku ve organ bozulmasına neden olan gen arızalarına yol açarak yaşa bağlı hastalık süreçlerini tetikleyebileceği düşünülmüştür. Ancak yeni araştırma sonuçları, epigenetik (genler üstü, genlerin çalışmasını düzenleyen) değişiklikler de dahil olmak üzere diğer faktörlerin aslında yaşlanmanın ana nedenleri olabileceğini düşündürmüştür.
Hücrelerimizin çekirdeğinde, genetik bilginin uzun süreli saklanmasını sağlayan, nesillerinin devamı ve biyolojik gelişmeleri için gerekli olan genetik talimatları taşıyan kompleks DNA molekülü bulunur. DNA’da bulunan talimatlar genlerle ifade edilir ve DNA’daki talimatların hepsine birden genom adı verilir. Genlerin sistematik olarak çalışması epigenetik mekanizmalarla sağlanır.
Epigenetik, güneş ışığına maruz kalma, sigara içme, yediğimiz yiyecekler, fiziksel aktivitemiz ve soluduğumuz hava gibi yaşam tarzı ve çevresel faktörler de dahil olmak üzere genlerin genetik olmayan faktörler tarafından nasıl etkilenebileceğini inceleyen bir bilim dalıdır. Epigenetik değişiklikler, DNA dizisindeki değişiklikler değil, genlerin ifade edilme şekillerinde yani "aktif" veya "aktif olmayan" olarak ifade edilmesindeki değişikliklerdir. Epigenetik faktörler, hücrelerde hangi genlerin aktif veya pasif olduğunu kontrol eder. Epigenetik düzenlemelerde ve mekanizmalarda yer alan tüm oluşumlara ise epigenom denir.

Biyolojik yaşlanma sürecinin temelinde, moleküler yapıların ve dolayısıyla işlevlerin değişimi vardır. Biyomoleküllerin değişen enerji durumları, entropik değişimlerin sonucunda gerçekleşir. Entropi, sistemin açık veya kapalı olmasına bağlı olmadan, yoğunlaşmış enerjinin dağılması anlamına gelir. Enerji durumlarındaki bu değişikliklere adaptasyon gösterebilme yeteneği olgunlaşma dönemine kadar korunabilmektedir. Üretkenlik veya doğurganlık döneminin ardından canlı organizmalarda mevcut bu denge yavaş yavaş bozulur ve moleküllerin, değişen enerji durumlarından dolayı inaktif hale gelmesi daha olası bir hal almaya ve vücut bağışıklığı zayıflamaya başlar.
Yaşlanmanın Önemli Bir Nedeni: Epigenetik Bilginin Kaybı
Ocak 2023’te ayında Cell dergisinde yayınlanan bir araştırmada, epigenomdaki değişikliklerin yaşlanmayı hızlandırabileceğini veya tersine çevirebileceği gösterildi.
Araştırmacılar fareler üzerinde insan ve diğer memeli hücrelerinde yaşam tarzı veya çevresel faktörlerden kaynaklanan bazı değişiklikleri taklit etti. Epigenetik işlev bozukluğuna neden olan değişiklerin fareleri biyolojik olarak yaşlandırdığı gözlemlendi. Çalışmanın ikinci kısmı için, araştırmacılar kök hücrelerde aktif olan genleri kullanarak gen terapisi uyguladılar. Gen terapisinin araştırmacıların neden olduğu yaşlanmayla ilişkili epigenetik değişiklikleri tersine çevirdiği görüldü.
Çalışmanın Grafik Özeti
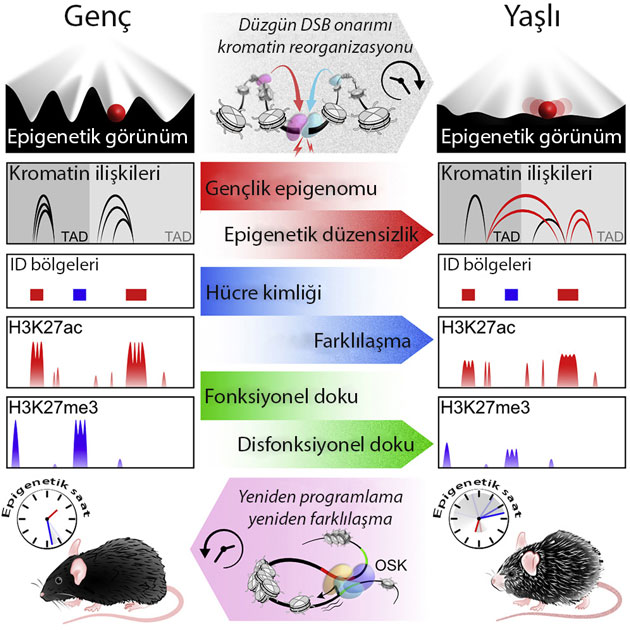
DNA kırılmalarına hücresel bir tepki olarak epigenetik görünüm aşınır.- Bu epigenetik bilgi kaybı, yaşlanmanın ayırt edici özelliklerini hızlandırır.
- Bu değişiklikler epigenetik yeniden programlama ile tersine çevrilebilir.
- Epigenomu manipüle ederek, yaşlanma ileri ve geri sürülebilir.
Harvard Tıp Fakültesi Blavatnik Enstitüsü'nde genetik profesörü ve Paul F. Glenn Yaşlanma Araştırmaları Biyolojisi Ortak Direktörü olan David Sinclair ve ekibi yaşlanmada epigenetik değişikliklerin rolü hakkındaki hipotezlerini "ICE" (epigenom üzerinde tetiklenen değişiklikler) adlı bir sistem kullanarak gerçekleştirdi. Bu sistemde farelerdeki epigenetik değişikler DNA’larına kesikler atılıp memeli hücrelerinde yaşam tarzı veya çevresel faktörlerden kaynaklanan değişiklikleri taklit edildi. Sık periyotlarla kesik atılan DNA’ların protein kodlayan kısımlarında mutasyona sebep olmamasına dikkat edildi.
Bir organizmanın kronolojik (nüfur) yaşı, yaşadığı günler, aylar ve yıllara dayanırken, biyolojik yaş yaşlanma biyobelirteçleri temel alınarak ölçülen bir yaş ölçüsüdür. İnsan biyolojik yaşlanmanın belirtileri arasında mitokondri (hücrelerimizin güç kaynakları) işlev bozukluğu ve telomerlerin (kromozomlarımızın kapalı uçları) kısalması bulunur. Biyolojik yaşımız, kronolojik yaşımızdan çok farklı olabilir.
Araştırmacılar, ICE farelerinde hipotezlerinin doğru olduğunu gösteren epigenetik bir kaos gördüler. Epigenetik faktörlerin normal işlevlerinin durduğunu ve bunun yerine kromozom kesiklerine yönlenerek tamir işlemini gerçekleştirip orijinal yerlerine geri döndükleri gözlemlendi. Ancak zaman ilerledikçe, bazı epigenetik faktörler orijinal yerlerine geri dönmeyi bıraktığında epigenetik arızalar meydana gelmeye başladı. (Çalışmada hangi epigenetik faktörün tamirde görev yaptığı ve orijinal konumuna gelmediği belirtilmemiştir.)
Epigenetik arızalarını ICE farelerinin biyolojik yaşlanma biyobelirteçlerinin artmasına dolayısıyla daha yaşlı görünmesine ve davranmasına neden olduğunu gözlemledi. Dokuların ve organların sağlığı, hücrelerin kimliklerini kaybettikleri için bozuldu ve başarısız oldu. (Vücudumuzdaki her hücre aynı genlere sahiptir, ancak aynı zamanda bir cilt hücresi, bir kan hücresi, bir kemik hücresi vb. olarak birer kimlik taşır.) ICE farelerinin biyolojik yaşını belirlemek ve aynı kronolojik yaşı paylaşan ICE olmayan farelerin biyolojik yaşını karşılaştırmak için bir hesaplama modeli kullanan araştırmacılar epigenetik değişiklikler olmayan aynı kronolojik yaşa sahip farelerin biyolojik yaşını ICE farelerinin biyolojik yaşıyla karşılaştırdıklarında, ICE farelerinin daha fazla yaşlandığını buldular.
Deneyin ek bir bileşeni olarak araştırmacılar, ICE farelere kök hücrelerinde aktif olan Oct4, Sox2 ve Klf4'ün bir kombinasyonu olan OSK adı verilen bir geni vererek (gen terapisi) tedavinin ICE farelerinin yaşlanma süreci üzerindeki etkilerini gözlemlediler. Gen tedavisi verildiğinde hücrelerin kaybettikleri epigenetik bilgiyi geri kazandıkları görülse de araştırmacılar bu süreci neyin nasıl teşvik ettiğinden emin değil. Ancak memelilerin hücreleri, uygun koşullar altında epigenetik işlevi sıfırlamaya veya geri yüklemeye yardımcı olabilecek epigenetik bilgiye benzer bir yedekleme sistemi olduğu teorisi üzerinde durulmaktadır.
Sinclair'in çalışması yaşam süresini uzatma üzerine yaptığı bu çalışma epigenom manipülasyonunun hem yaşlanmayı hızlandırabileceğini hem de tersine çevirebileceğini göstermektedir. Bu konudaki daha fazla bilgi Tip 2 diyabet, kardiyovasküler hastalık, bilişsel bozulma gibi yaşa bağlı süreçleri ve hastalıkları önleme veya tersine çevirme yolları bulmaya yardımcı olabileceği düşünülmektedir. Bu gelişmelerle yaşam süresini uzatmanın yanı sıra yaşlılık yıllarında yaşam kalitesini de arttırılabilir. Farelerde yapılan bu ön çalışmanın ışığında epigenetik manipülasyonun insanlarda potansiyel olarak nasıl uygulanabileceğini belirlemek için daha fazla araştırmaya ihtiyaç vardır.
Jae-Hyun Yang, Motoshi Hayano, Patrick T. Griffin, et al. Loss of epigenetic information as a cause of mammalian aging. Cell 12 Jan 2023






