Yumurtalık (over) Kanseri: Etkili İmmünoterapi, Yeni T Hücre Çalışmasıyla Daha da Yakınlaşıyor
Bir kadının yaşamı boyunca yumurtalık (over) kanserine yakalanma riski ABD istatistiklerine göre 75'te 1 civarındadır. Ülkemizde ise yumurtalık kanseri, kadınlarda 7. sıklıkta gözükmektedir. Tanı alan kadınların yaklaşık yarısı 63 yaş ve üzerindedir. Erken evrelerde nadiren bulgu verdiği için çoğunlukla 3. ve 4. evrede tanı konulan ve tedavi sonrası tekrarlama eğiliminin daha belirgin olduğu bu hastalıkta, ameliyat ve kemoterapi tedavinin temelini oluşturmaktadır. Son yıllarda PARP inhibitörü olarak adlandırılan DNA tamir mekanizması üzerine etkili biyolojik ilaçlar da tedavi sahnesine girmiştir. Bununla birlikte, kanser alanının çığır açan tedavileri olan immünoterapilerin yumurtalık kanserinde etkili olup olmadığına dair az sayıda bilgi mevcuttur.
İmmünoterapi, kanser tedavisinde umut verici sonuçları olan nispeten yeni bir tıp alanıdır. Bu tedavide temel prensip, hastalığa karşı savaşmak için hastanın kendi bağışıklık sistemini kullanılmasıdır. Amerikan Kanser Araştırmaları Derneği'nin (AARC) bu yılki toplantısında dikkat çeken başlıklardan biri de yumurtalık kanseri tedavisinde immünoterapi uygulamalarıydı. Bununla birlikte immünoterapiler tek çeşit değildir.
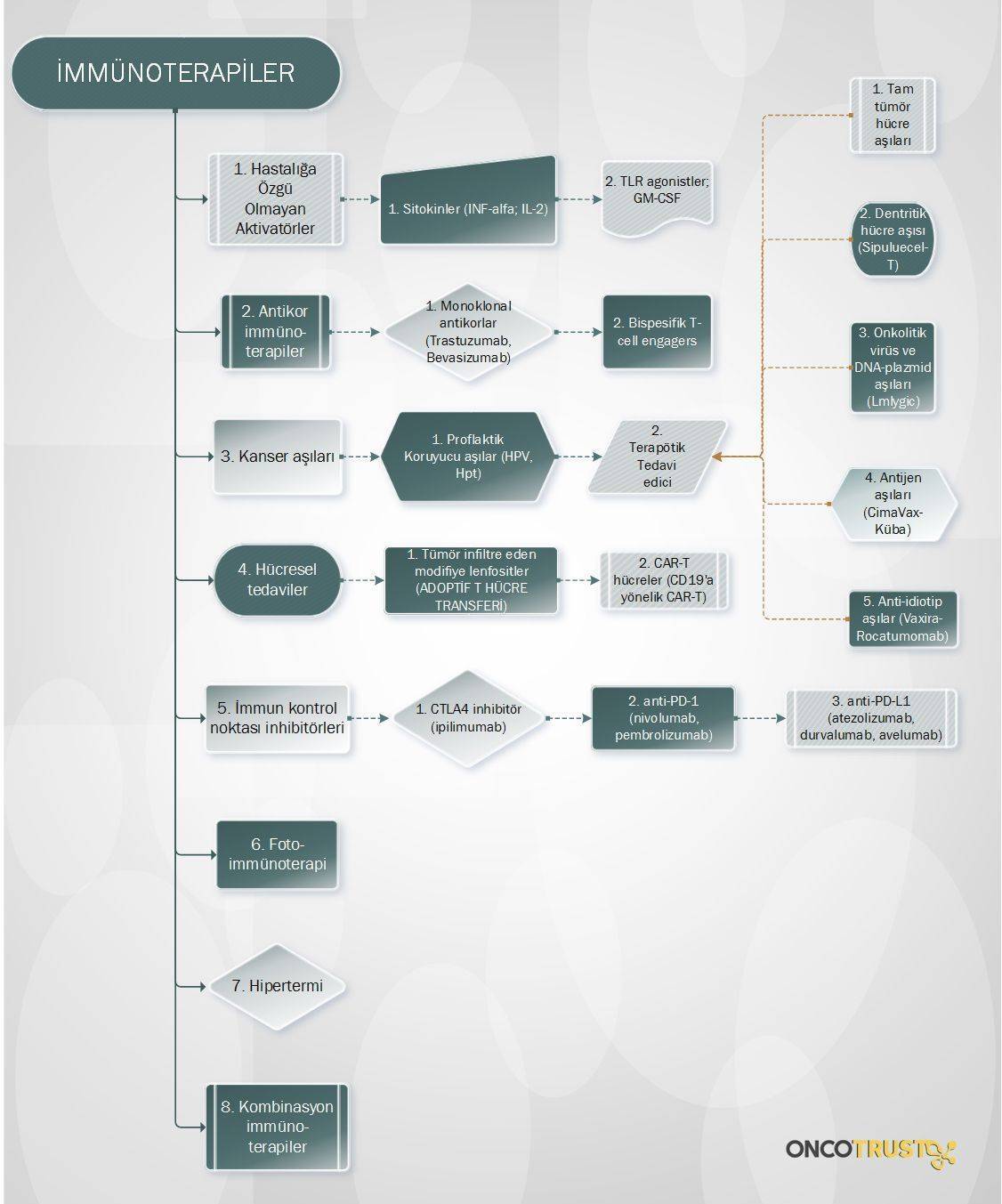
Yumurtalık Kanseri İçin Umut Veren Bir İmmünoterapi Çeşidi: Adoptif T Hücre Transferleri
Kanserleri “solid” ve “solid olmayan” olarak iki gruba ayırırız. Solid tümörlerden kasıt, belli organların (akciğer, meme, kalın bağırsak, prostat gibi) kanserleridir. Solid olmayan kanserler ise hemato-onkolojinin konusudur, ve kan ve lenf organlarının kanserlerini (lösemi, lenfoma gibi) ifade etmektedir.
Yeni bir çalışmaya göre adoptif T hücre transferi olarak adlandırılan bir yöntem solid bir tümör olan yumurtalık kanseri tedavisinde etkili olabilir. Hücresel immünoterapi çeşitlerinden biri olan adoptif T hücre tedaviside; T hücreleri olarak isimlendirilen savunma hücreleri hastanın kendi kanından alınır ve kanser hücrelerini hedeflemesi için modifiye edilir. Ardından, laboratuvarda çoğaltıldıktan sonra işlemden geçirilmiş hücreler hastanın vücuduna geri verilerek kanser hücreleri yok edilmeye çalışılır.
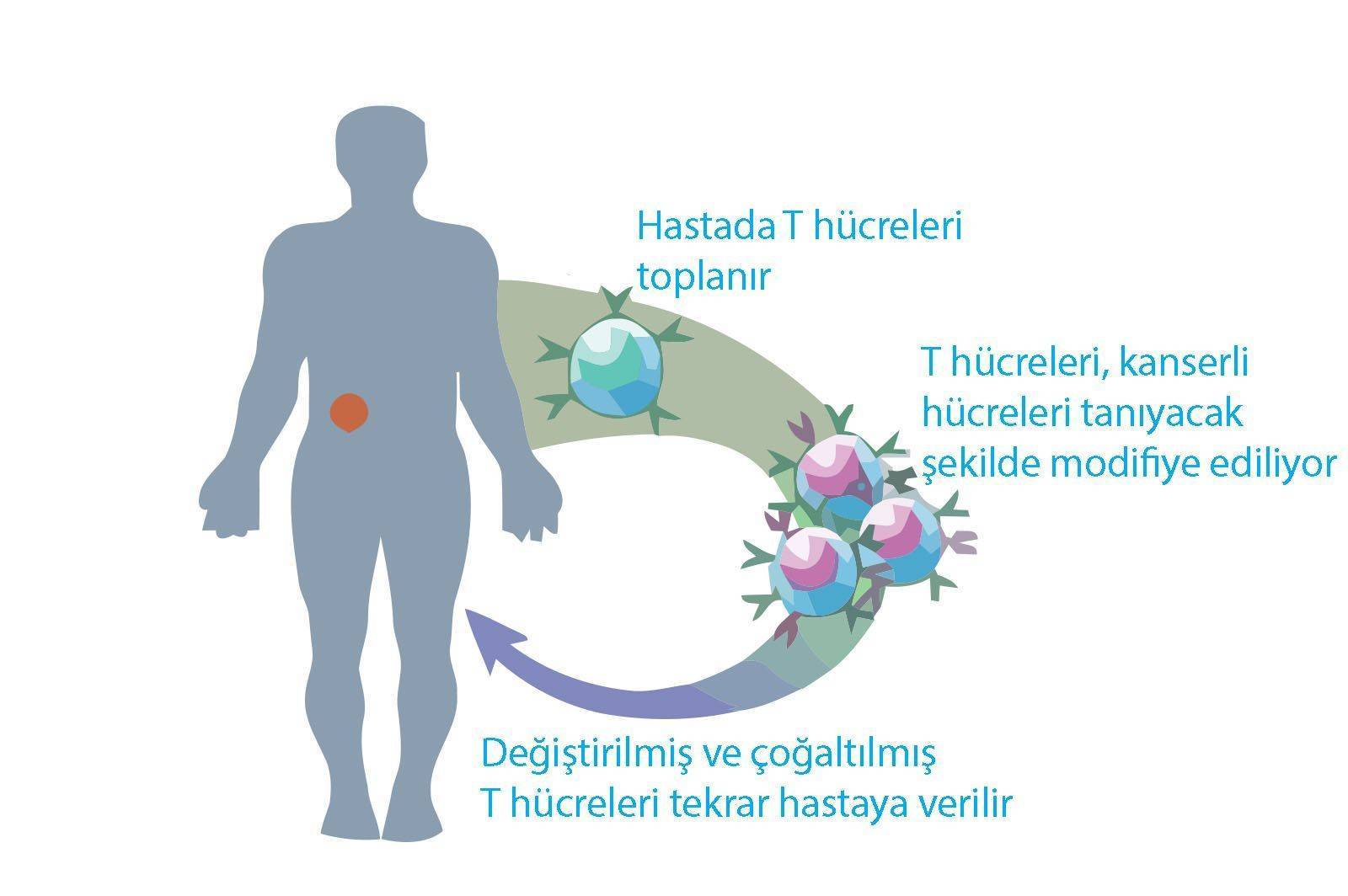
Araştırmacı ekip solid olmayan kanserlerden biri olan lösemi tedavisi için adoptiv T hücre transferi yönteminde başarılı olduklarını bildirmiştir. Aynı zamanda bu çalışmadan edinilen tecrübeler doğrultusunda solid tümörlere bu tedavinin uygulanmasında da ilerlemeler kaydedilmiştir.
Bağışıklık sistemi hücrelerimiz, tümörlerden salınan özel proteinleri hedef alacak şekilde yeniden programlanabilir mi?
Yumurtalık kanseri hücrelerinin iki proteini - WT1 ve mezotelin - aşırı ürettiği tespit edilmiştir. Bu proteinleri hedefleyecek şekilde tasarlanmış T hücrelerinin laboratuvarda fare ve insan yumurtalık kanseri hücrelerini öldürülebileceğini keşfetmişlerdir. Fakat adoptif T hücresi aktarımının insanlarda klinik araştırmalara hazır hale gelmesi için daha fazla çalışmaya ihtiyaç vardır.
Bununla birlikte kan kanserlerinin tedavisine kıyasla meme, yumurtalık, akciğer ve pankreas kanseri gibi solid tümörlere T hücre tedavisi uygulamanın daha zor olduğunu belirtmek gerekir.
Lösemi ve lenfomada, işleme uğramış T hücreleri doğrudan kan dolaşımına verilerek kanserli hücreler hedeflenir. Fakat, organların içinde bulunan solid tümörlere erişim bu kadar kolay değildir ve çeşitli zorluklar barındırmaktadır. Solid tümörlere tedavi edici ajanların ulaştırılmasındaki en önemli engellerden biri, tümör mikroçevresi olarak adlandırılan, onlarca farklı hücre çeşidi ve kompleks etkileşimler barındıran tümör yakın dokusudur.
Kanser Tedavisinde Şimdiye Kadar Hesaba Katılmayan Faktör: Tümör Mikroçevresi
Tümör mikroçevresi, solid tümörler için adoptif T hücre tedavilerini 3 şekilde zorlaştırmaktadır:
- Mikroçevre olarak adlandırılan tümör yakın dokusundaki hücreler ve protein yapıları T hücrelerine sinyal yollayarak, T hücrelerinin inaktif hale gelmesini ya da tümörü yok saymasını sağlar. Hali hazırda kullanımda olan “bağışıklık sistemi kontrol noktası inhibitörleri” olarak adlandırılan immünoterapi ilaçları bu problemin çözülmesini sağlayabilir. Diğer bir yöntem ise bu sinyalleri bloke eden T hücrelerinin genetik teknikler aracılığıyla üretilmesidir.
- Yumurtalık kanseri hücreleri veya tümör çevresindeki kan damarları, gönderdikleri sinyaller ile T hücrelerinin kanser hücresine saldıramadan kendilerini yok etmesine neden oldukları bulunmuştur. Buna karşılık T hücreleri bu sinyali aldığında pasif hale geçmemeleri için, özel tedavi edici proteinler geliştirilmektedir.
- Tümör mikroçevresinde şeker miktarı oldukça azdır. Bunun sebebi, kanser hücrelerinin kontrolsüz çoğalması için fazla miktarda şekere ihtiyaç duymasıdır. Aynı zamanda T hücreleri de çoğalmak ve kansere karşı atak yapabilmek için enerji kaynağı olarak şekere ihtiyaç duymaktadır. Bu da kanserin enerji kaynağını kesecek tedavilerin geliştirilmesinde sorun yaratmaktadır. Bu sorunu çözmek adına T hücreleri genetik tekniklerle değiştirilerek şeker yerine farklı bir enerji kaynağı kullanması denenmektedir.
Sonuç olarak, adoptive T hücre tedavileri, kansere karşı bilinçli savaşçı hücreler geliştirmeyi amaçlar. Ancak, geliştirilen T hücrelerin kendi hücrelerimize saldırma riski bulunmaktadır. Bir genetik mühenddisliği tekniği olan CRISPR ile T hücreleri daha özgül / hedefe yönelik hale getirilerek, sadece kanser hücrelerine saldırması hedeflenmektedir. Özellikle solid olmayan tümörlerde, yani kan lanserleri ve lenfomalarda büyük umut vaad eden bu yöntem, tümör mikroçevresinde karşılaşılan sorunların giderilmesiyle birlikte solid tümörlerde de etkili bir tedavi sunacaktır.
Kristin G. Anderson, Breanna M. Bates, Edison Y. Chiu et al.
Engineering adoptive T cell therapy for efficacy in ovarian cancer.
AACR Annual Meeting 2017. Session MS.IM02.01 - Adoptive Cellular Therapy for Cancer
4980