
Akciğer Kanseri için Ameliyat Öncesi ve Sonrası Pembrolizumab FDA Onayı Aldı
16 Ekim 2023'te, ABD Gıda ve İlaç İdaresi (FDA), cerrahi olarak çıkarılabilir küçük hücreli dışı akciğer kanseri (tümör çapı ≥4 cm veya lenf düğümü pozitif) olan hastaların tedavisi için, pembrolizumab (Keytruda) adlı immünoterapiyi, platin içeren kemoterapiyle birlikte neoadjuvan (cerrahi öncesi) ve cerrahi sonrası adjuvan (destekleyici) tek ajan olarak onayladı.
Bu onay, erken evre akciğer kanserinde immünoterapi tedavisi için 4. FDA onayını temsil etmektedir. Bununla birlikte akciğer kanseri tedavisi için ilk perioperatif (neoadjuvan + adjuvan) immünoterapi onayıdır.
Erken evre akciğer kanserinde önceki immünoterapi onayları şu şekildedir:
- 15.10.2021'de Atezolizumab (Tecentriq): PD-L1 ≥ % 1, evre II – IIIA KHDAK adjuvan tedavisi olarak platin bazlı kemoterapi sonrası. 1005 hastalık IMpower010 çalışmasında adjuvan atezolizumab kullanımının, kanserin tekrarlama riskini %44 azalttığı görüldü.
- 04.03.2022'de Nivolumab (Opdivo): Evre IB – IIIA ameliyat edilebilir KHDAK neoadjuvan tedavisi olarak kemoterapi ile kombine onay aldı. Nivolumab kolunda patolojik tam yanıt %24, sadece kemo ile %2,2 idi.
- 26.02.2023'te Pembrolizumab (Keytruda): Evre IB (T2a ≥4 cm), II veya IIIA KHDAK için ameliyat ve platin-bazlı kemoterapiyi takiben adjuvan tedavi olarak onay aldı. Kemoterapi alanlarda hastalıksız sağkalım 58,7 aya karşı 34,9 ay (HR=0,73). Adjuvan KT almayanlar fayda görmedi.
KEYNOTE-671 Çalışması ile Gelen FDA Onayı
Perioperatif pembrolizumabın etkililiği, daha önce tedavi edilmemiş ve cerrahi olarak çıkarılabilir Evre II, IIIA veya IIIB (N2) küçük hücreli dışı akciğer kanserli (KHDAK) 797 hastanın değerlendirildiği, çok merkezli, randomize, çift kör, plasebo-kontrollü KEYNOTE-671 adlı bir faz-3 klinik çalışmada değerlendirildi.
Hastalar, platin temelli kemoterapi ile birlikte, ya pembrolizumab ya da plasebo alacak şekilde gruplara ayrıldı ve her 3 haftada bir, 4 döngü boyunca tedavi gördüler (bu aşamaya neoadjuvan tedavi denir). Bu tedavi döneminden sonra hastalar ameliyat edildi. Daha sonra hastalar ya yalnızca pembrolizumab alarak tedaviye devam ettiler ya da plasebo alarak tedaviye devam ettiler, her 3 haftada bir olmak üzere toplamda 13 döngüye kadar (bu aşamaya adjuvan tedavi denir).
Sonuçlar
Ana etkililik sonuç ölçütleri genel sağkalım (Overall Survival= OS) ve araştırmacı tarafından değerlendirilen olaysız sağkalım (Event Free Survival= EFS) idi.
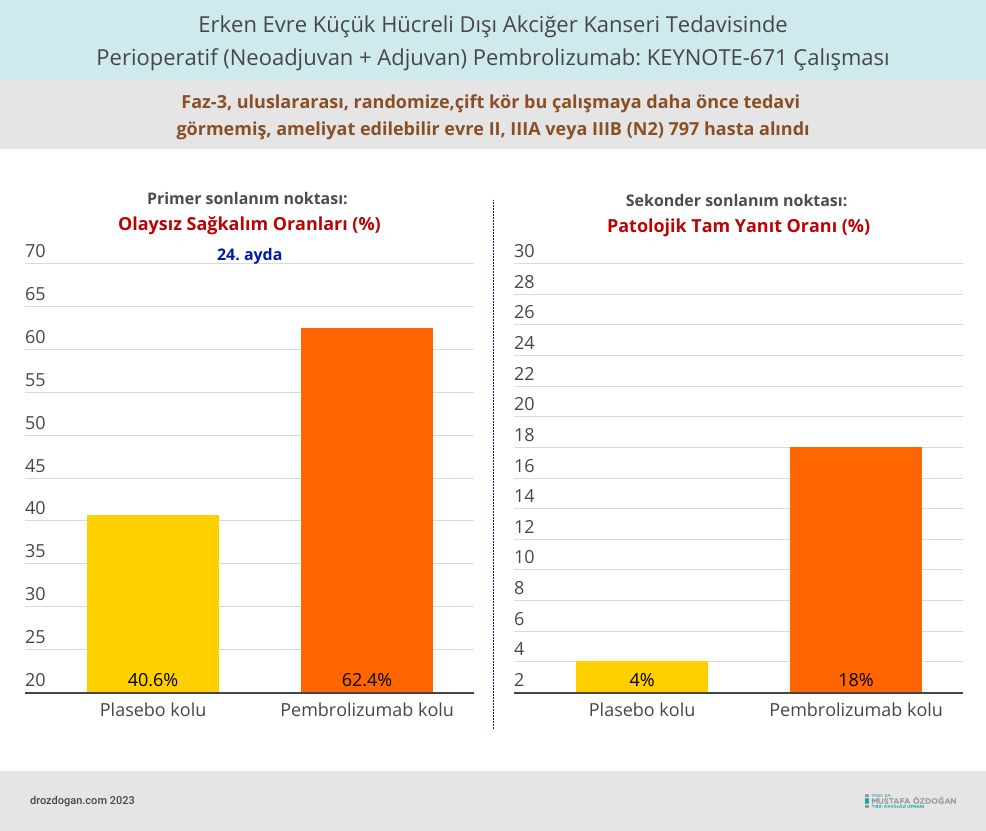
- Perioperatif (neoadjuvan + adjuvan) tedavi olarak pembrolizumab kullanmanın, kanserin ilerlemesi, kanser tekrarı veya yaşam kaybı riskini %42 azalttığı bulundu.
- Pembrolizumab kolunda ortanca genel sağkalıma ulaşılmadı (%95 GA: tahmin edilemez [NE], NE), bu süre plasebo alanlarda 52,4 ay (%95 GA: 45,7, NE) (hazard oranı [HR] 0.72 [%95 GA: 0.56, 0.93]; p-değeri=0.0103) idi.
- Pembrolizumab kolunda ortanca EFS ulaşılmadı (%95 GA: 34,1 ay, NE) ve plasebo kolunda 17 ay (%95 GA: 14,3, 22,0) (HR 0.58 [%95 GA: 0.46, 0.72]; p-değeri=<0.0001) idi.
KEYNOTE-671'de, %20'den fazla hastada bildirilen en yaygın advers reaksiyonlar bulantı, yorgunluk, nötropeni, anemi, kabızlık, iştah azalması, beyaz kan hücresi sayısında azalma, kas iskelet ağrısı, döküntü, öksürük, kusma, ishal ve nefes darlığı idi. Pembrolizumab kolunda neoadjuvan tedavi alan hastaların %6'sı advers reaksiyonlar nedeniyle ameliyat edilemedi, plasebo kolunda bu oran %4,3 idi. Ayrıca, pembrolizumab kolunda neoadjuvan tedavi ve cerrahi olan hastaların %3,1'i, plasebo kolunda ise %2,5'i advers reaksiyonlar nedeniyle cerrahide gecikmeler yaşadı.
Önerilen pembrolizumab dozu, her 3 haftada bir 200 mg veya her 6 haftada bir 400 mg'dir. Pembrolizumab'ı, aynı gün verildiğinde kemoterapi öncesinde uygulayın.
1. FDA approves neoadjuvant/ adjuvant pembrolizumab for resectable non-small cell lung cancer. 16 Oct 2023. https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-neoadjuvant-adjuvant-pembrolizumab-resectable-non-small-cell-lung-cancer
2. Wakelee H, Liberman M, Kato T, Tsuboi M, Lee SH, Gao S, Chen KN, Dooms C, Majem M, Eigendorff E, Martinengo GL, Bylicki O, Rodríguez-Abreu D, Chaft JE, Novello S, Yang J, Keller SM, Samkari A, Spicer JD; KEYNOTE-671 Investigators. Perioperative Pembrolizumab for Early-Stage Non-Small-Cell Lung Cancer. N Engl J Med. 2023 Aug 10;389(6):491-503. doi: 10.1056/NEJMoa2302983. Epub 2023 Jun 3. PMID: 37272513.






