HER2-Pozitif Akciğer Kanserinde Tedavi Devrimi: Seçici TKI’lar ve ADC’lerin Yükselişi
Onkoloji dünyasının saygın yayınlarından Frontiers in Oncology’nin Mart 2026 sayısında, ekibimle birlikte kaleme aldığımız kapsamlı derleme makalemizin yer almasının gururunu yaşıyoruz. Uzun yıllardır akciğer kanserinin en zorlu ve dirençli hedeflerinden biri olarak kabul edilen HER2 değişimleri, artık "isabetli" tıp yaklaşımımızla kontrol altına alınabilir bir noktaya ulaştı.
Bu çalışmamızda; nadir ama agresif bir seyir izleyen HER2 mutasyonlarını, biyolojik restorasyon felsefemiz ışığında ve en güncel literatür verileriyle yeniden tanımlıyoruz.
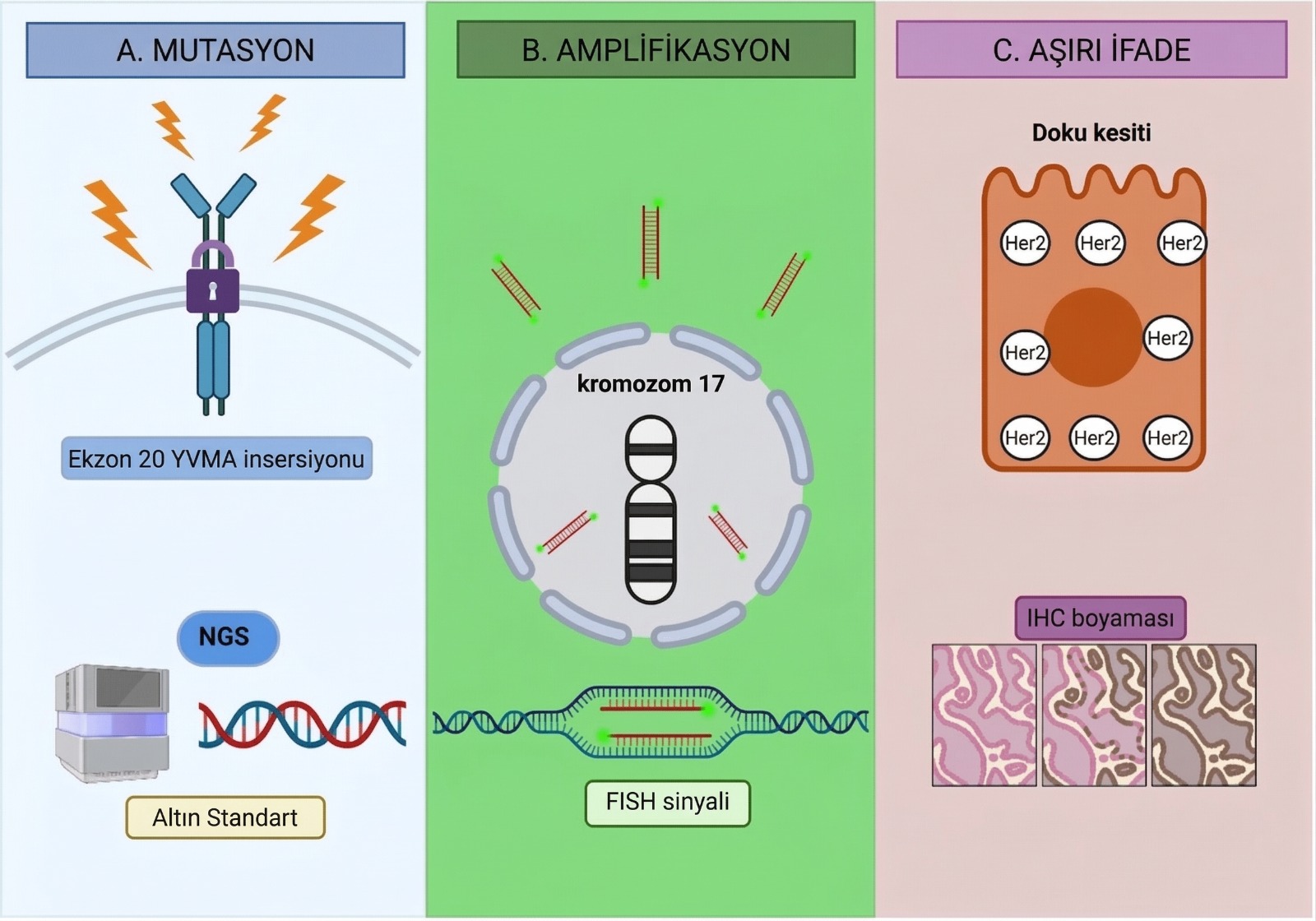
HER2 Aktivasyon Mekanizmaları: Üç Farklı Yüz
Akciğer kanserinde HER2, üç temel yolla tümörü besler. Her bir mekanizma, tedavinin "isabet" oranını doğrudan belirleyen biyolojik ipuçları taşır:
Sıklık: KHDAK'lı hastaların yaklaşık %2 ila %4'ünde görülür.
Detay: KHDAK'ta en sık görülen ve tedaviye en iyi yanıt veren "sürücü" (driver) HER2 değişikliğidir. Özellikle Exon 20 insertion (YVMA) varyantı, tüm HER2 mutasyonlarının %70-80'ini (bazı çalışmalarda metindeki gibi "yarısından fazlasını") oluşturur. Genellikle sigara içmeyen genç kadınlarda ve adenokarsinom tipinde görülür.
Sıklık:
Birincil Sürücü Olarak: KHDAK hastalarının yaklaşık %2 ila %4'ünde tanı anında bulunur.
EGFR Direnç Mekanizması Olarak: EGFR hedefe yönelik ilaçları (TKI) kullanan hastalarda direnç geliştiğinde, bu oran %10 ila %12'ye kadar çıkabilir.
Detay: Genin kopya sayısının artmasıdır. Mutasyonlara göre daha nadir bir birincil sürücüdür ancak EGFR ilaçlarına karşı gelişen önemli bir direnç yoludur.
Ayrıca Protein Aşırı İfadesi (Overexpression), hücre yüzeyinde HER2'nin yoğunlaşmasıdır. Meme kanserindeki başarının aksine, akciğer kanserinde tek başına "aşırı ifade", tedavinin başarısını öngörmede zayıf kalmıştır; asıl belirleyici mutasyonun varlığıdır.
- Sıklık: Çalışmalarda kullanılan kriterlere ve yöntemlere (IHC) göre %2 ila %38 arasında çok geniş bir aralıkta bildirilmiştir.
- Önemli Skor Sıklığı (IHC 3+): Tedaviye yanıtla daha ilişkili olan yüksek düzeyde aşırı ifade (IHC 3+ skoru), hastaların sadece yaklaşık %2 ila %6'sında görülür.
- Detay: Hücre yüzeyinde HER2'nin yoğunlaşmasıdır. Meme kanserindeki başarının aksine, akciğer kanserinde tek başına "aşırı ifade" (özellikle IHC 2+ gibi düşük skorlar), tedavinin başarısını öngörmede zayıf kalmıştır; asıl belirleyici mutasyonun varlığıdır.
Tanı Standartları: NGS Neden Vazgeçilmez?
HER2 mutasyonlarını tespit etmek için geleneksel yöntemler yetersiz kalabilir. Çalışmamız, tanı sürecinde Yeni Nesil Dizileme (NGS) teknolojisinin "altın standart" olduğunu vurgulamaktadır:
- NGS: Exon 20 (YVMA ve non-YVMA) eklemelerini, nokta mutasyonlarını ve kopya sayısı değişimlerini tek seferde ve yüksek duyarlılıkla yakalar.
- FISH: Gen amplifikasyonunu doğrulamak için hala referans yöntemdir.
- IHC: Protein seviyesini ölçer ancak "HER2-Low" kavramı akciğer kanserinde henüz klinik olarak valide edilmemiştir.
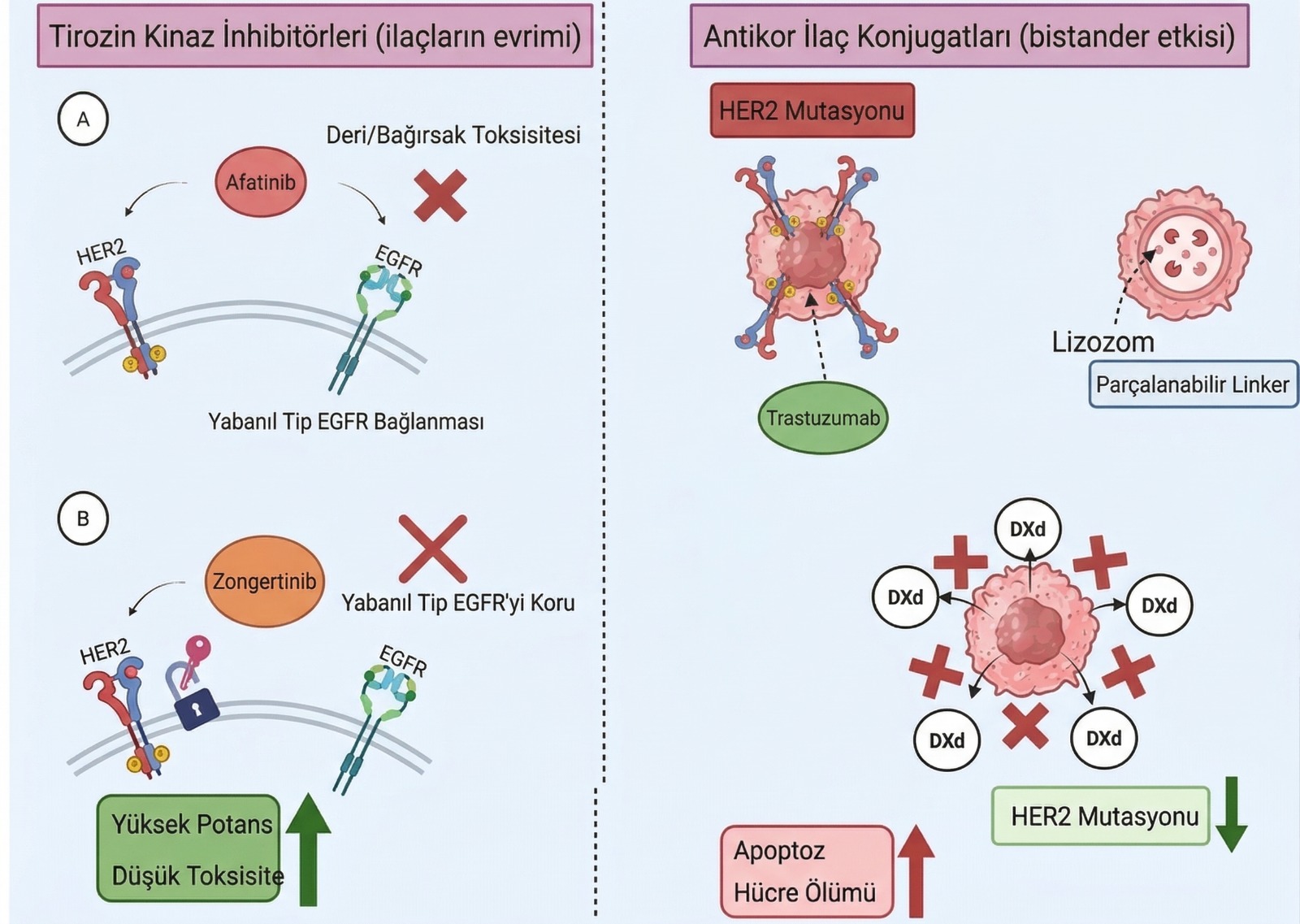
Tedavi Paradigmasında Büyük Sıçrama: ADC ve Yeni Nesil TKI'lar
Eskiden kullanılan afatinib veya poziotinib gibi ilaçlar, hem düşük etkinlikleri hem de "vahşi tip EGFR"yi de baskılamaları nedeniyle şiddetli deri ve bağırsak yan etkileriyle hastaları zorluyordu. Bugün ise iki devrimsel sınıf öne çıkmaktadır:
1. Antikor-İlaç Konjugatları (ADC): Biyolojik Füzeler
Trastuzumab Derukstekan (T-DXd): 2022'de onaylanan bu ajan, "bystander effect" (komşu hücreleri de öldürme) özelliği sayesinde HER2 mutasyonu olan hücreleri cerrahiye yakın bir hassasiyetle temizleyebilir. DESTINY-Lung çalışmalarında %50 civarı yanıt oranları ve dikkat çekici sağkalım verileri sağlamıştır.
2. Yeni Nesil Seçici TKI'lar (Daha Güçlü, Daha Az Yan Etki)
2025 ve 2026'ya damgasını vuran iki yeni molekül, ağızdan alınan haplarla tedaviyi çok daha konforlu hale getirdi:
| İlaç | Özellik | Yanıt Oranı (ORR) | Klinik Avantaj |
|---|---|---|---|
| Zongertinib | Exon 20 seçici, irreversible TKI | %77 | Wild-type EGFR'yi korur; döküntü ve ishal minimaldir. |
| Sevabertinib | Reversible dual HER2/EGFR TKI | %64 - %71 | ADC sonrası dirençli vakalarda bile etkindir. |
Beyin Metastazlarında "Bariyerleri" Aşmak
HER2 mutasyonlu akciğer kanseri hastalarının %30-50'si süreç içinde beyin metastazı geliştirmektedir. Geçmişte bu bir "son durak" olarak görülürken, yeni ajanlar kan-beyin bariyerini yüksek başarıyla aşmaktadır:
- Zongertinib: Beyin metastazı olan hastalarda %41 intrakraniyal yanıt oranı sağlamıştır.
- T-DXd (ADC): %50'ye varan intrakraniyal objektif yanıt ile beyindeki tümörleri geriletme gücüne sahiptir.
Bu veriler, beyin metastazı yönetiminde radyoterapiyi öteleyebilecek "isabetli" sistemik seçeneklerin elimizde olduğunu kanıtlamaktadır.
Güncel Tedavi Algoritması (2026)
Şu an sürmekte olan DESTINY-Lung04 ve Beamion LUNG-2 çalışmalarıyla, bu hedefe yönelik ilaçların çok yakında 1. basamak tedaviye (ilk seçenek olarak) yükselmesi beklenmektedir.
DROZDOGAN Akademi Yorumu
Akciğer kanserinde HER2 mutasyonlarını yıllarca "sessiz bir tehdit" olarak izledik. Ancak biyolojik restorasyon felsefemiz gereği; asıl mesele, o sessizliğin içindeki genetik çığlığı doğru duymak ve "isabetli" karşılığı vermektir. Bu derleme, sadece yeni ilaçları listelemiyor; aynı zamanda kanserli hücrenin DNA'sındaki o küçük Exon 20 sapağını nasıl kapatacağımızı anlatıyor.
Yeni nesil seçici TKI'lar ve akıllı ADC'ler, hastalarımıza artık kemoterapinin yıkıcı yan etkileri olmadan, daha uzun ve kaliteli bir yaşam vaat ediyor. Geleceğin onkolojisi, hastayı bir bütün olarak koruyan, bariyerleri (beyin) aşan ve biyolojinin derinliğini kavrayan bu isabetli rehberlik üzerine inşa edilmektedir. Şifa, bilimin şefkatli ve keskin ışığında yükseliyor.
Bilimsel Referanslar
- 1. Balli S, Basoglu T, Ozdogan M. "Evolving treatment strategies for HER2-altered non-small-cell lung cancer: the rise of TKIs and ADCs." Frontiers in Oncology. 2026;16:1771869. doi:10.3389/fonc.2026.1771869
- 2. Heymach JV, et al. "Zongertinib in previously treated HER2-mutant non-small-cell lung cancer." N Engl J Med. 2025.
- 3. Li BT, et al. "Trastuzumab deruxtecan in HER2 mutant non-small-cell lung cancer." N Engl J Med. 2022.