Kanserde Doğru Genetik Testi Seçmek: WGS, WES ve Hedefe Yönelik Dizileme
Yeni nesil dizileme (NGS), genetik materyali hızlı, hassas ve yüksek doğrulukla analiz etmeye olanak tanıyan devrim niteliğinde bir teknolojidir. Geleneksel yöntemlere kıyasla daha kısa sürede daha fazla veri üreten NGS, genetik varyantların belirlenmesi, hastalık mekanizmalarının anlaşılması ve kişiselleştirilmiş tedavilerin geliştirilmesinde kritik bir rol oynar. Özellikle onkoloji gibi alanlarda, kanserin genetik kökenine dair derinlemesine bilgiler sunarak hedefe yönelik tedavi stratejilerinin temelini oluşturur.
Son yıllarda yeni nesil dizileme (NGS) maliyetlerindeki dramatik düşüşle birlikte, tüm genom dizilemesi (WGS) geniş çaplı genetik bilgi sağlayabilmesi sayesinde giderek daha cazip hale gelmiştir. Ancak, yeterince derin okumalar elde etmek ve devasa miktarda veriyi yönetmek gibi zorluklar bu yöntemin önündeki en büyük engellerdir. Hedef zenginleştirme yaklaşımları, genomun belirli alt kümelerini prob hibridizasyonu yoluyla izole edip dizilemeye olanak tanır ve WGS'ye kıyasla daha düşük maliyetli alternatifler sunar. Özellikle, derinlemesine dizileme gerektiren durumlarda, tüm ekzon dizilemesi (WES) ve özelleştirilmiş hastalık spesifik paneller gibi yöntemler, yalnızca en kritik genomik bölgelerin analizine odaklanarak maliyet ve hassasiyet dengesini sağlar. Bununla birlikte, bu hedefe yönelik yaklaşımlar, hedeflenen bölgeler dışında kalan önemli varyantları kaçırma riski taşır.
Bu yazıda, WGS, WES ve hedefe yönelik dizileme yaklaşımlarının avantajları ve dezavantajlarını ayrıntılı şekilde ele alıyoruz. Doğru yaklaşımı seçmek büyük ölçüde araştırma veya klinik sorunun doğasına bağlıdır. Özellikle onkolojide, moleküler hedeflerin tespiti ve kişiselleştirilmiş tedavi tasarımı için bu teknolojilerin seçimi kritik öneme sahiptir.

Tanımlar
WGS, WES ve Hedefe Yönelik Dizileme Nedir?
- WGS (Whole Genome Sequencing: Tüm Genom Dizilemesi): DNA'nın tüm genomunun, yani kodlayan (ekzon) ve kodlamayan (intron) tüm bölgelerinin dizilenmesidir. Bu yöntem, genomun tamamını kapsadığı için en geniş kapsamlı ve detaylı genetik bilgi sağlar.
- WES (Whole Genome Sequencing: Tüm Ekzon Dizilemesi): Sadece protein kodlayan genlerin ekzonlarını diziler ve genomun yaklaşık %1’ini kapsar. Daha odaklı olduğu için maliyet ve veri analizi açısından WGS’ye göre avantajlıdır.
- Hedefe Yönelik Dizileme (Targeted Sequencing): Belirli genleri veya gen bölgelerini dizilemek için özelleştirilmiş paneller kullanır. Bu yöntem, özellikle hastalıklarla ilişkili spesifik mutasyonları araştırmak için tercih edilir.
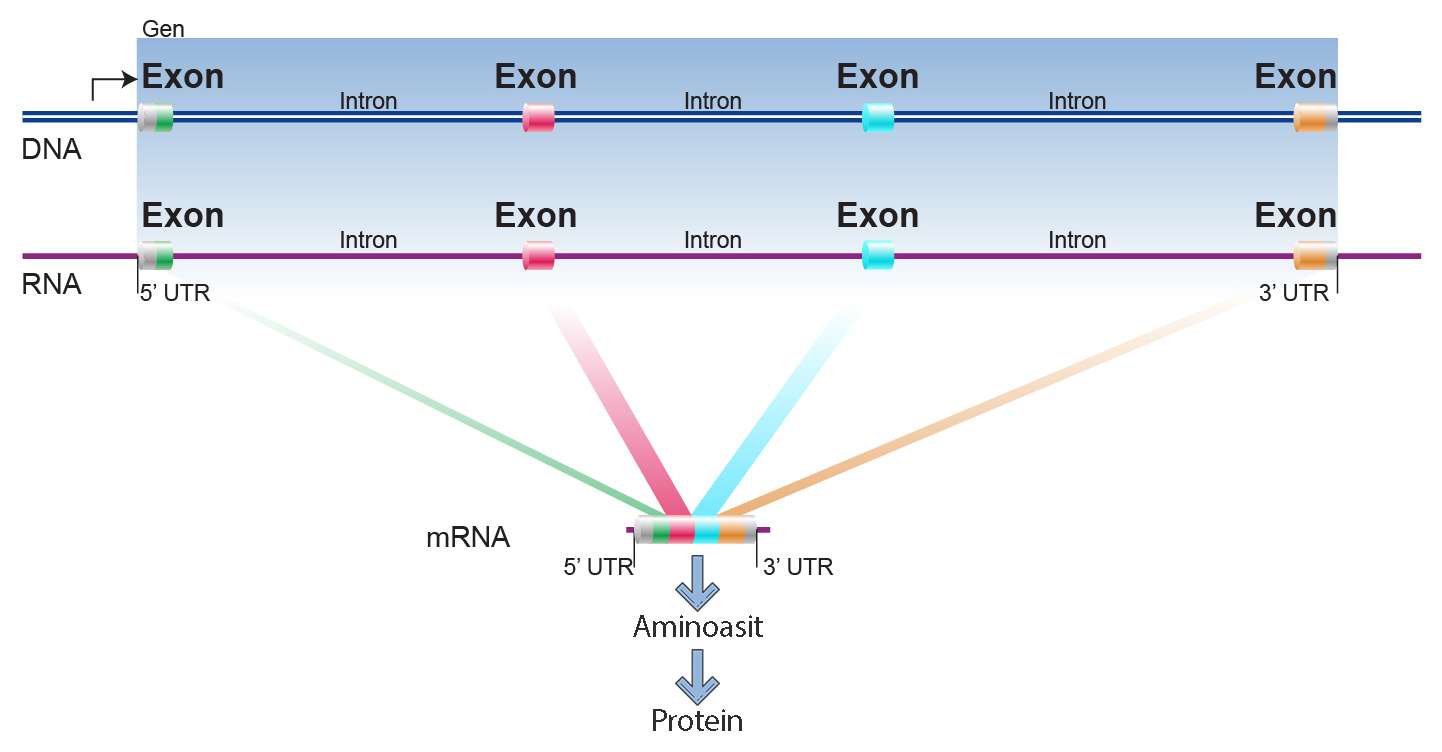
Ekzon ve İntron Kavramları
-
Ekzon: DNA üzerinde, genetik bilgiyi proteine dönüştürmek için kullanılan, RNA’ya çevrilip protein üretiminde aktif rol alan bölgelerdir. Ekzonlar birleşerek ekzomu oluşturur ve tüm ekzom, genomun sadece %1’ini oluşturmasına rağmen biyolojik işlevlerin gerçekleşmesi için kritik öneme sahiptir.
-
İntron: Genetik bilginin protein üretimine dahil olmayan, RNA’ya çevrildikten sonra uzaklaştırılan gen bölümleridir. İntronlar, gen düzenlemesi ve alternatif ekzon kullanımında rol oynayarak genetik çeşitlilik sağlar.
WGS, WES ve RNAseq'in Onkolojide Hedefe Yönelik Dizileme ile Karşılaştırılması
Hedefe yönelik tedavi, onkolojide kişiselleştirilmiş tıp anlayışının temel taşıdır ve kanserin oluşum mekanizmalarını ve direnç yollarını aydınlatmayı hedefler. Ancak tarihsel olarak, bu yaklaşımlar beklenenden düşük başarı oranlarıyla sonuçlanmıştır. Bu durumun başlıca nedenleri şunlardır:
- Eksik veya uygun olmayan panel kullanımı: Örneğin, RNA dizilemesinin DNA dizilemesine eklenmesi, hedef tanımlama oranını %10 veya daha fazla artırabilir.
- Kanıt eksikliği ve tedavi önerilerinin uzman görüşüne dayalı olması: Uluslararası standartlar yerine, bireysel uzman görüşüne dayalı tedavi önerileri yaygındır.
- İlaç ve hedef uyumsuzluğu: Kullanılan ilaçlar genellikle hedefe özgü olmayan inhibitörlerdir.
- Hastaların tedavi öncesi fazla aşınmış olması: Çoğu çalışma, dirençli tümörlere sahip hastaları içermektedir.
Bu engeller zamanla aşılmıştır ve günümüzde:
- Daha geniş kapsamlı ve uygun NGS teknolojileri,
- ESCAT, OncoKB gibi eylemsellik ölçekleri,
- Seçici ilaçların artan erişimi ve
- Moleküler testlerin hastalığın erken evrelerine uygulanması yaygınlaşmıştır.
Güncel NGS Manzarası: Neredeyiz?
Bugün, hedefe yönelik NGS, terapötik hedeflerin belirlenmesi, kişiselleştirilmiş tedavi tasarımı ve direnç mekanizmalarının anlaşılması konularında giderek daha fazla doğrulanmaktadır. Örneğin:
- ESMO (Avrupa Tıbbi Onkoloji Derneği) tarafından akciğer kanseri, over kanseri, prostat kanseri ve kolanjiokarsinoma için NGS'nin rutin kullanımı önerilmektedir.
- SAFIR02-BREAST gibi klinik çalışmalar, genomik profillemeye dayalı tedavi yaklaşımının progressyonsuz sağkalımı artırdığını göstermiştir.
Kapsamlı panel dizilemesi, genellikle spesifik genlerin veya mutasyonların tespiti için tasarlanmış paneller kullanır. Bu yöntem, belirli gen bölgelerini derinlemesine inceleme olanağı sağlar (500 ila 20.000 kat kapsama). Bununla birlikte, bu yaklaşımlar tüm-genom duplikasyonları, fokal kopya kazançları, mikrosatellit instabilitesi (MSI) gibi geniş ölçekli genetik olayların algılanmasında yetersiz kalabilir.
WGS ve WES ile Yeni Ufuklar
WGS ve WES'in avantajları arasında şunlar yer alır:
- Daha yüksek hassasiyet: Tüm-genom mutasyon imzalarının tespiti ve genomik yeniden düzenlenmelerin algılanması,
- Hedefe yönelik panellerde yer almayan predispozan varyantların belirlenmesi,
- Tümör mikroçevresinin gen ekspresyon profillemesi ve biyobelirteçlerin tespiti.
Ancak bu yöntemlerin uygulanmasında karşılaşılan zorluklar şunlardır:
- Artan maliyet ve uzun analiz süreleri,
- FFPE örneklerinden elde edilen düşük kaliteli DNA'nın hata oranlarını artırması,
- Tümör saflığı gereksinimlerinin daha sıkı olması.
Onkolojide Gelecek Perspektifleri
NGS teknolojileri arasında bir seçim yapmak, yalnızca maliyet ve veri hacmine değil, aynı zamanda klinik bağlama ve araştırma sorusunun doğasına dayanır:
- Hedefe yönelik NGS, bilinen varyantların hızlı tespiti ve hedeflenen gen bölgelerinin derinlemesine analizi için uygundur.
- WGS ve WES, daha geniş genetik varyantları keşfetmek ve araştırma odaklı soruları yanıtlamak için idealdir.
- RNAseq, füzyon genleri ve ekson atlama gibi olayları belirleme konusunda standart kabul edilir.
Gelecekte, WGS ve WES'in daha yaygın hale gelmesi, bu teknolojilerin daha geniş çapta kullanılabilirliği ve maliyetlerin düşmesiyle mümkün olacaktır. Ancak, bu yöntemlerin klinik rutine entegrasyonu, hasta merkezli bakım için moleküler tümör kurulları gibi uzmanlık merkezlerini gerektirecektir.
Sonuç ve Yorum
Sonuç olarak, yeni nesil dizileme (NGS) teknolojileri arasında doğru yöntemi seçmek, klinik bağlam ve araştırma ihtiyaçlarına göre değişir. WES (tüm ekzon dizilemesi), genetik varyantların geniş bir yelpazesini hızlıca taramak için ideal bir yöntemdir; bu nedenle geniş bir genetik görünüm sunar. Ancak, WES genellikle daha düşük hassasiyete sahiptir ve hedefe yönelik dizileme kadar yüksek çözünürlük sağlamaz. Hedefe yönelik dizileme (target sequencing), özellikle somatik veya germline onkolojik incelemelerde altın standart olarak kabul edilir ve kritik gen bölgelerini derinlemesine analiz etmek için eşsiz bir hassasiyet sunar.
Bu farkı, genetik bilgisi olmayan bireyler için şu şekilde açıklayabiliriz: WES ile bir kütüphanedeki tüm kitapları tarayıp hızlı bir şekilde dijital olarak yeniden yazdırabilirsiniz, ancak kitapların içindeki resimleri tam anlamıyla analiz edemezsiniz. Öte yandan, hedefe yönelik dizileme, tıpkı bir resmi yüksek çözünürlüklü bir kamerayla çekmek gibidir. Bu yaklaşım, görüntüyü büyüttüğünüzde bile netliği korur. Eğer WES'i 5 megapiksel bir kamera olarak düşünürsek, hedefe yönelik dizileme 100 megapiksel bir kamera gibi çalışır; daha derin, daha net ve daha detaylı bir analiz sağlar.
Bu nedenle, NGS teknolojileri arasında seçim yaparken, hem hedefe yönelik dizilemenin yüksek çözünürlük avantajları hem de WES'in daha geniş kapsam sağlayan doğası dikkate alınmalıdır. Bu teknolojilerin bir arada kullanımı, hem geniş genetik perspektiflere ulaşmak hem de yüksek hassasiyetle spesifik varyantları hedeflemek için güçlü bir strateji sunar.
Aldea, M. et al. WGS/WES-RNAseq compared to targeted NGS in oncology: is there something to unlock? Annals of Oncology, December 2023, Volume 34, Issue 12, 1090 - 1093