Kaplan–Meier Eğrisi Nedir ve Nasıl Okunur? Kanserde Yaşam Süresi Verilerini Yorumlama Rehberi
Klinik araştırmalarda bir kanser tedavisinin başarısını belirleyen temel unsurlardan biri, seçilen sonlanım noktası (endpoint)dır. Erken dönem klinik çalışmalarında objective response rate (ORR) gibi tümör hacmine dayalı göstergeler ön plandayken, geç faz çalışmalarda sağkalım süreleri (progression-free survival ve overall survival) daha belirleyici hale gelmiştir. Ancak modern onkolojide yalnızca yaşam süresi değil, tedavinin yaşam kalitesine, tolerabilitesine ve uzun vadeli faydasına etkisi de giderek önem kazanmaktadır.
Bu nedenle, özellikle immünoterapiler, antikor-ilaç konjugatları (ADC’ler) ve hedefe yönelik tedaviler çağında; Hastalık Kontrol Oranı (DCR), Klinik Fayda Oranı (CBR), Sağlıkla İlgili Yaşam Kalitesi (HRQoL), Time to Next Treatment (TTNT) ve Duration of Response (DoR) gibi ek sonlanım parametreleri, klasik PFS ve OS’nin ötesinde klinik etkinliğin daha rafine bir ölçümünü sunmaktadır.
Klinik onkoloji tarihine bakıldığında, tedavi etkinliğini ölçmek için başlangıçta yalnızca ölüm oranı temel alınmaktaydı. Ancak bu yaklaşım, özellikle yavaş seyirli veya uzun takip gerektiren kanserlerde tedavi farklarını erken saptamakta yetersiz kaldı. Bu nedenle, 1958 yılında Edward L. Kaplan ve Paul Meier tarafından geliştirilen “Kaplan–Meier metodu”, zamana bağlı olayların istatistiksel analizi için çığır açıcı bir yöntem olarak onkolojide devrim yarattı.
Kaplan–Meier eğrisi, her hastanın yaşam süresini veya olay gerçekleşene kadar geçen süreyi bireysel olarak değerlendirir ve “sensörleme (censoring)” adı verilen kavramı kullanır. Bu kavram, hâlâ olay gerçekleşmemiş (örneğin hasta yaşıyor veya progresyon olmamış) bireylerin analiz dışında kalmamasını sağlar. Böylece klinik çalışmalar, tüm katılımcıların verilerini zamana bağlı şekilde değerlendirerek daha doğru sağkalım tahminleri üretebilir.
Bu istatistiksel yaklaşım, zaman içinde farklı klinik sorulara yanıt verebilecek yeni sonlanım noktalarının geliştirilmesini sağladı. 1980’lerde kemoterapi çağında Overall Survival (OS) “altın standart” kabul edilirken, 1990’lardan itibaren hedefe yönelik tedavilerle birlikte Progression-Free Survival (PFS) ve Time to Progression (TTP) gibi ara sonlanımlar öne çıktı. Günümüzde ise immünoterapiler ve biyolojik ajanlar sayesinde, hastalık tamamen yok olmasa bile uzun süre stabil seyir gösterebilen olguların varlığı, Disease Control Rate (DCR), Clinical Benefit Rate (CBR) ve Duration of Response (DoR) gibi yeni ölçütlerin doğmasına yol açtı.
Böylece “etkinlik” kavramı yalnızca yaşam süresiyle değil; hastalığın kontrol altında kalma süresi, yaşam kalitesi ve tedavi tolerabilitesiyle de tanımlanır hâle geldi. Bu evrim, klinik araştırmalarda hasta odaklı bakış açısına geçişin temel kilometre taşlarından biridir.
Günümüzde ileri istatistik modelleri, yalnızca tek bir sonlanımı değil, birden fazla sonlanım noktasını birlikte değerlendirerek joint survival modeling veya multi-endpoint analysis gibi yöntemlerle bütüncül klinik etkiyi hesaplamaktadır. Bu sayede tedavinin hastaya kattığı gerçek değeri daha kapsamlı biçimde ölçmek mümkün hale gelmiştir.
Klinik Sonlanım Noktaları, Klinik Örnekleri
- 1. Disease Control Rate (DCR) — Hastalık Kontrol Oranı:
Bir tedaviye yanıt olarak tam yanıt, kısmi yanıt veya stabil hastalık gösteren hasta oranıdır. Örneğin, KEYNOTE-158 çalışmasında pembrolizumab alan mikrosatellit instabilite yüksek (MSI-H) solid tümörlerde DCR %33 olarak bildirilmiştir. - 2. Clinical Benefit Rate (CBR) — Klinik Fayda Oranı:
Tam veya kısmi yanıtla birlikte en az 24 hafta stabil seyir gösteren hastaların oranını ifade eder. Bu ölçüt, özellikle hormon reseptör pozitif metastatik meme kanserinde endokrin tedavilerin etkinliğini tanımlamakta kullanılır. - 3. Health-Related Quality of Life (HRQoL) — Sağlıkla İlgili Yaşam Kalitesi:
EORTC QLQ-C30 veya FACT-G gibi anketlerle ölçülür. Örneğin, CheckMate-214 çalışmasında nivolumab + ipilimumab kombinasyonu, sunitinib’e göre anlamlı HRQoL iyileşmesi sağlamıştır. - 4. Landmark Overall Survival — Belirli Bir Zamandaki Hayatta Kalma:
12. veya 24. ayda hayatta kalan hasta oranını gösterir. Özellikle erken dönem faz II çalışmalarda hızlı etkinlik göstergesi olarak değerlendirilir. - 5. Time to Treatment Failure (TTF) — Tedavi Başarısızlığına Kadar Geçen Süre:
Progresyon, toksisite, hasta isteği veya ölüm gibi nedenlerle tedavi kesilene kadar geçen süredir. Gerçek yaşam verilerinde tedavi tolere edilebilirliğini ölçmek için kullanılır. - 6. Time to Next Treatment (TTNT) — Bir Sonraki Tedaviye Kadar Zaman:
Bir tedaviden bir sonrakine geçilene kadar geçen süredir. Örneğin, indolent lenfomalarda veya metastatik kolorektal kanserde, idame tedavilerin klinik dayanıklılığını göstermek için önemlidir. - 7. Duration of Clinical Benefit (DoCB) — Klinik Faydanın Süresi:
Hastalığın uzun süreli stabil kaldığı veya yanıtın sürdüğü dönemdir. İmmünoterapi sonrası “plateau etkisi” görülen hastalarda uzun dönem faydayı yansıtır. - 8. Duration of Response (DoR) — Yanıt Süresi:
Tam veya kısmi yanıt elde edildikten sonra progresyona kadar geçen süredir. Örneğin, DESTINY-Breast03 çalışmasında trastuzumab deruxtecan kolunda medyan DoR 25,1 ay olarak bildirilmiş ve kemoterapiye kıyasla belirgin avantaj sağlamıştır.
Sağkalım analizi, modern klinik araştırmaların temel istatistiksel araçlarından biridir ve Kaplan–Meier (K–M) yöntemi, 1958 yılında Edward Kaplan ve Paul Meier tarafından tanımlandığından bu yana klinik onkolojide standart haline gelmiştir. Bu yöntem, bir hasta grubunda belirli bir olayın (örneğin progresyon, rekürrens veya ölüm) zaman içinde gerçekleşme olasılığını adım adım hesaplayarak, “hayatta kalma olasılığı”nın görsel temsili olan eğriler oluşturur.
K–M eğrisi, klasik istatistik analizlerden farklı olarak tüm hastaların verilerini hesaba katar. Eğer bir hasta olay gerçekleşmeden (örneğin takip dışı kalma, başka nedenle ölüm, ya da çalışmadan erken ayrılma) izlemden çıkarsa, bu hasta “sensörlenmiş (censored)” olarak tanımlanır. Sensörleme, çalışmanın sağkalım analizini bozmaz; çünkü Kaplan–Meier yöntemi, bu bireylerin o ana kadarki katkısını korur. Bu yönüyle, gerçek yaşam koşullarına en yakın istatistiksel modeldir.
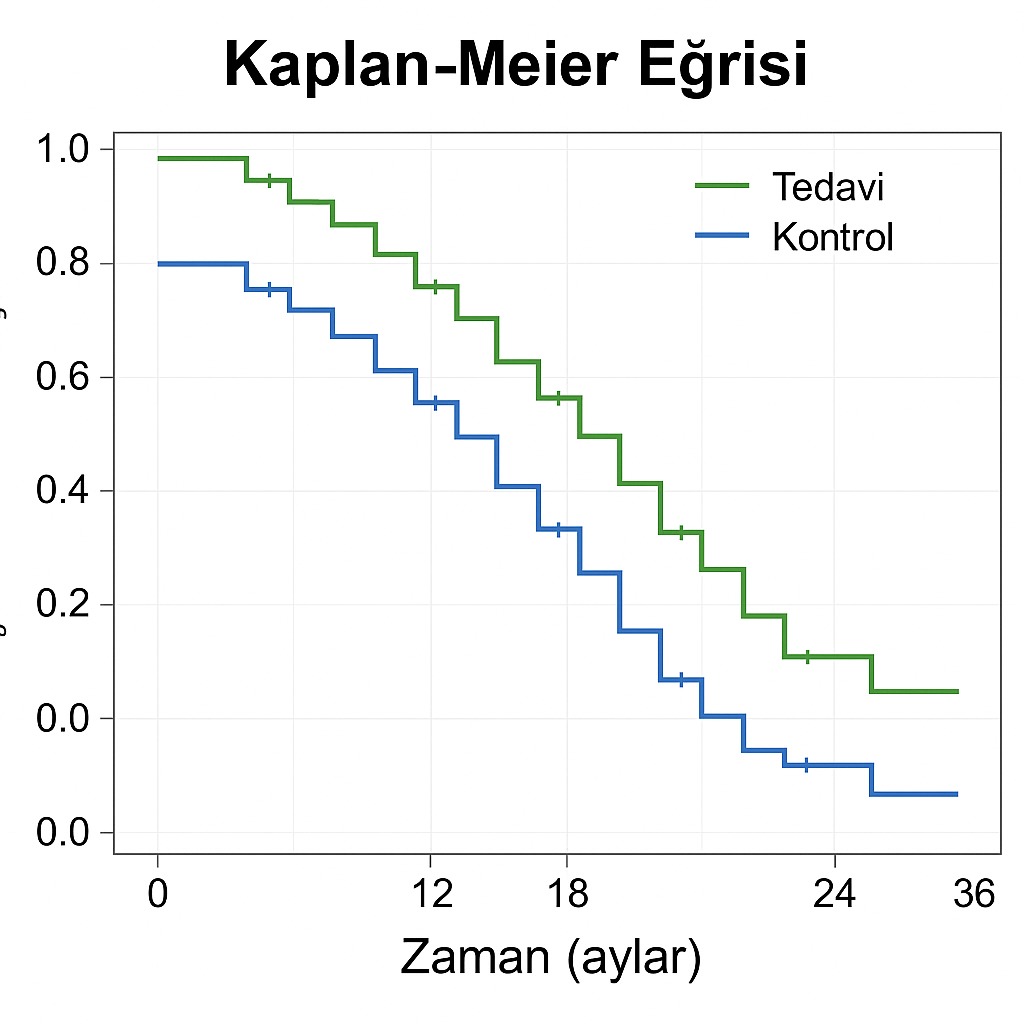
1. Eğrinin Yapısı ve Yorumlanması
Kaplan–Meier eğrisi genellikle dik basamaklar şeklinde ilerler. Her bir basamak, bir hastada olayın gerçekleştiği anı temsil eder. Zaman ekseninde ilerledikçe eğri kademeli olarak aşağı iner, bu da olay gerçekleşme olasılığının artığını gösterir. Eğrinin %50 seviyesine ulaştığı nokta, medyan sağkalım süresi olarak tanımlanır. Bu değer, “popülasyonun yarısının hâlâ olaydan etkilenmeden yaşadığı süreyi” belirtir.
2. İki Eğrinin Karşılaştırılması: Log-Rank Testi ve Hazard Ratio
Klinik araştırmalarda iki farklı tedavi kolunun sağkalım eğrileri karşılaştırılırken en sık kullanılan yöntem log-rank testi’dir. Bu test, iki grup arasındaki olay gerçekleşme hızının zaman boyunca anlamlı biçimde farklı olup olmadığını analiz eder. Elde edilen p-değeri 0.05’in altındaysa, gruplar arasında istatistiksel olarak anlamlı fark olduğu kabul edilir.
Buna ek olarak, sağkalım analizlerinde hazard ratio (HR) kavramı kullanılır. HR değeri, tedavi kolunda olayın (örneğin ölüm veya progresyon) meydana gelme riskini kontrol koluna oranla gösterir:
- HR = 1 → İki grup arasında fark yok.
- HR < 1 → Tedavi kolunda olay riski azalmış (örneğin HR=0.70 → %30 risk azalması).
- HR > 1 → Tedavi kolunda olay riski artmış.
3. Kaplan–Meier Eğrilerinin Klinik Değeri
Kaplan–Meier eğrileri yalnızca istatistiksel bir gösterim değil, aynı zamanda tedavi etkinliğinin zaman içindeki dinamiklerini anlamak için klinik bir araçtır. Özellikle immünoterapilerde eğrilerde gözlenen “plateau etkisi” (uzun süre stabil kalan yüksek sağkalım oranı) bazı hastalarda uzun dönem hastalık kontrolünün sağlandığını gösterir. Bu durum, klasik kemoterapilerde nadiren görülür ve immünoterapilerin “uzun yanıt veren hasta alt grubu” varlığını işaret eder.
Ayrıca Kaplan–Meier eğrileri, ara analizler (interim analysis) ve alt grup analizlerinde de sıklıkla kullanılır. Örneğin PD-L1 pozitif ve negatif alt grupların ayrı eğrilerde karşılaştırılması, tedavinin hangi moleküler profilde daha etkin olduğunu ortaya koyabilir.
4. Görsel Temsil
Klinik sonlanım noktaları yalnızca bilimsel araştırmaların değil, aynı zamanda ilaç onay süreçlerinin de merkezinde yer alır. Bir sonlanım noktası, tedavinin hastaya “gerçek klinik fayda” sağladığını gösterebiliyorsa, bu veri hem regülasyon otoriteleri (FDA, EMA) hem de sağlık ekonomisi açısından en yüksek düzeyde kanıt değeri taşır.
1. FDA Perspektifi: "Surrogate Endpoint" Kavramı
ABD Gıda ve İlaç Dairesi (FDA), 1992 yılından itibaren onkoloji ilaçlarının hızlandırılmış onayında surrogate endpoint (dolaylı sonlanım noktası) kavramını resmi olarak tanımlamıştır. Buna göre, bir sonlanım noktası doğrudan yaşam süresini ölçmese bile (örneğin tümör küçülmesi, PFS veya DoR), genel sağkalım (OS) ile yüksek düzeyde korelasyon gösteriyorsa klinik faydayı “makul ölçüde öngörme” yeteneğine sahiptir.
Bu prensip sayesinde, accelerated approval (hızlandırılmış onay) mekanizması devreye girer. Örneğin:
- Pembrolizumab (Keytruda®) — MSI-H veya TMB-high solid tümörlerde objective response rate (ORR) ve DoR verilerine dayanarak hızlandırılmış onay almıştır.
- Trastuzumab deruxtecan — DESTINY-Breast01 çalışmasında yüksek DoR ve DCR oranları nedeniyle erken dönemde onaylanmış, daha sonra OS verileriyle tam onaya dönüştürülmüştür.
- Lenvatinib + Pembrolizumab kombinasyonu — endometrial kanserde PFS ve CBR üzerinden değerlendirilerek onay sürecine alınmıştır.
FDA bu tür onayları “intermediate clinical benefit” olarak nitelendirir ve tam onay için OS veya yaşam kalitesi gibi “hard endpoint” sonuçlarının olgunlaşmasını şart koşar.
2. EMA Yaklaşımı: "Conditional Marketing Authorization"
Avrupa İlaç Ajansı (EMA), benzer şekilde 2006’dan bu yana conditional marketing authorization (şartlı ruhsatlandırma) sistemini yürütmektedir. EMA, küçük hasta popülasyonlarında veya acil karşılanmamış ihtiyaç durumlarında, PFS, DoR veya HRQoL gibi erken sonlanım verilerini yeterli görerek ilacı piyasaya sürebilir. Ancak üretici firma belirli bir süre içinde nihai OS veya uzun dönem güvenlilik verilerini sunmakla yükümlüdür.
Örneğin:
- Nivolumab — 2015’te metastatik renal hücreli karsinomda PFS ve HRQoL verileriyle EMA tarafından şartlı onay almış, 2017’de OS verileriyle tam onaya dönüştürülmüştür.
- Sacituzumab govitecan — TNBC’de yüksek DoR oranı nedeniyle 2021’de EMA’dan hızlandırılmış onay almıştır.
3. Güncel Eğilimler: Kombine Sonlanım Noktaları ve Gerçek Yaşam Verisi
Regülasyon otoriteleri artık tek bir sonlanım noktasından ziyade çok boyutlu etki ölçütlerini tercih etmektedir. Composite endpoints olarak adlandırılan bu yaklaşımda PFS, HRQoL ve toksisite verileri birlikte değerlendirilir. Ayrıca Real-World Evidence (RWE) ve Time to Next Treatment (TTNT) gibi parametreler, randomize klinik çalışmaların ötesinde gerçek yaşam etkinliği hakkında değerli bilgi sunmaktadır.
Örneğin KEYNOTE-091 çalışmasında, adjuvan pembrolizumab tedavisi alan hastalarda PFS üstünlüğü gösterilmiş, OS verileri henüz olgunlaşmamış olmasına rağmen, uzun süreli HRQoL stabilitesi karar sürecine dâhil edilmiştir.
4. Klinik Uygulamalara Etkisi
Bu gelişmeler, onkologların tedavi seçiminde artık yalnızca “kaç ay yaşatıyor” sorusuna değil, “nasıl yaşatıyor” sorusuna da yanıt aramasını sağlamıştır. Özellikle palyatif ve ileri evre kanserlerde, yanıt süresi (DoR) veya tedaviler arası süre (TTNT) gibi göstergeler, hastanın yaşam kalitesi ve tedavi yükü arasındaki dengeyi optimize etmede klinik olarak değer taşır.
Ayrıca, sağlık politikaları açısından da bu parametreler geri ödeme kararlarını etkileyen kritik göstergelerdir. Türkiye’de Sosyal Güvenlik Kurumu (SGK), özellikle immünoterapi ve hedefe yönelik ajanlarda, uluslararası regülasyonların dayandığı klinik sonlanım verilerini referans olarak kullanmaktadır.
Kaplan–Meier eğrileri ve klinik sonlanım noktaları, onkolojik tedavilerin etkinliğini anlamamızda yalnızca sayısal araçlar değil, aynı zamanda hastalığın biyolojik davranışını zamansal olarak okumamızı sağlayan bir “dil”dir. Modern onkoloji artık sadece “kaç hastada tümör küçüldü?” sorusuna değil, “hangi hastalar ne kadar süreyle kontrol altında kaldı ve bu sürede yaşam kalitesi nasıldı?” sorusuna da yanıt aramaktadır. Bu nedenle PFS, OS, DoR, CBR ve HRQoL gibi göstergeler, klinik kararların merkezine yerleşmiştir.
Klinik verilerin Kaplan–Meier eğrileriyle değerlendirilmesi, bir tedavinin etkisinin zaman içindeki kalıcılığını görselleştirir. Eğrilerin erken dönemde ayrışması ilacın hızlı etkinliğini, geç dönemde uzun süre paralel seyretmesi ise immünoterapilerde görülen “plateau etkisi”ni, yani uzun yanıt süren hasta alt grubunu yansıtır. Bu görsel analiz, sadece istatistiksel bir gösterge değil; aynı zamanda biyolojik mekanizmaların klinik izdüşümüdür.
Günümüzde FDA ve EMA, onay süreçlerinde tek boyutlu “yaşatıyor mu?” sorusundan çok daha fazlasını aramaktadır. “Ne kadar süreyle hastalık kontrol altında tutuldu?”, “Yaşam kalitesi korundu mu?”, “Yanıt sürdürülebilir mi?” gibi çok boyutlu klinik fayda göstergeleri artık regülasyonun yeni dili haline gelmiştir. Bu yaklaşım, kanser tedavisinde hasta merkezli paradigmanın istatistiksel temele oturmasını sağlamaktadır.
Bununla birlikte, gerçek yaşam verilerinin (RWE) artması ve dijital hasta takibi sistemlerinin gelişmesi, klasik klinik sonlanım noktalarının ötesine geçmemizi sağlamaktadır. Artık elektronik sağlık kayıtlarından türetilen time-to-next-treatment (TTNT) veya real-world progression-free survival (rwPFS) gibi metrikler, klinik araştırma verilerini tamamlayıcı nitelikte değerlendirilmektedir.
Etik açıdan da bu dönüşüm önemlidir. Çünkü istatistiksel anlamlılık artık tek başına yeterli görülmemekte, “hastanın yaşam kalitesine yansıyan klinik anlamlılık” kavramı öne çıkmaktadır. Bu yaklaşım, klinik araştırmaları salt sayısal değil, insani bir bakış açısıyla yorumlamayı mümkün kılar.
Kaynakça
- FDA Oncology Center of Excellence. Clinical Trial Endpoints for the Approval of Cancer Drugs and Biologics. 2024 Update.
- Broglio KR et al. “Understanding clinical trial endpoints and their implications for clinical practice.” J Clin Oncol. 2023;41(2):115–124.
- Schwartz LH et al. RECIST 1.1 — “Response Evaluation Criteria in Solid Tumors.” Eur J Cancer 2022;163:20–28.
- EMA Guidelines on the Evaluation of Anticancer Medicinal Products in Man. EMEA/CHMP/205/95 Rev.6, 2023.