Kişiselleştirilmiş Yeni Bir Kanser Aşısıyla 3.-4. Evre Böbrek Kanserinde Etkili Sonuçlar
Böbrek kanserinin en yaygın alt tipi olan berrak hücreli böbrek hücreli karsinom (bhBHK), ileri evrelerde (Evre III ve IV) tekrarlama riski yüksek olan bir hastalıktır. Standart tedavi, tümörün cerrahi olarak çıkarılması ve takiben pembrolizumab gibi immün kontrol noktaları inhibitörleri ile immünoterapi uygulanmasını içerir. Ancak bu hastaların %67’sinde hastalık tekrar edebilir ve mevcut tedavi seçenekleri sınırlıdır.
Dana-Farber Kanser Enstitüsü liderliğinde gerçekleştirilen ve 5 Şubat'ta Nature dergisinde yayımlanan yeni bir çalışma, cerrahi sonrası uygulanan kişiselleştirilmiş kanser aşısının, hastalarda güçlü bir anti-kanser immün yanıt oluşturduğunu ve hastalığın tekrarlamasını önleyebileceğini gösterdi.
Kişiselleştirilmiş Neoantijen Kanser Aşısı Nedir?
Neoantijen kanser aşısı, her hastanın kendi tümöründen elde edilen moleküler belirteçlere dayalı olarak özel olarak tasarlanan kişiseleştirilmiş kanser tedavisidir.
Neoantijenler, kanser hücrelerinde bulunan ancak normal hücrelerde bulunmayan mutasyonel protein parçacıklarıdır. Araştırmacılar, bu neoantijenleri belirleyerek immün sistemi tümörü hedef alacak şekilde eğiten özel bir aşı geliştirdi.
Aşı, hastalara cerrahi sonrası bir dizi başlangıç dozuyla uygulandı ve takiben iki takviye dozu ile desteklendi. Bu yeni yaklaşım, vücudun kalan tümör hücrelerini tanıması ve yok etmesini sağlamaya yöneliktir.
NeoVax Kanser Aşısının Çalışma ve Üretim Mekanizması
NeoVax olarak adlandırılan bu kişiselleştirilmiş kanser aşısının üretimi, her hastanın tümör dokusundan elde edilen genetik ve moleküler bilgilere dayanır. Süreç şu adımlardan oluşur:
-
Tümör Dokusu Toplanması ve Analizi:
-
Cerrahi işlem sırasında hastadan alınan tümör dokusu analiz edilir.
-
Tümör hücrelerinden, normal hücrelerden farklılaşan mutasyonlar belirlenir.
-
-
Neoantijenlerin Tanımlanması:
-
Genetik analizler ve biyoinformatik algoritmalar kullanılarak, kanser hücrelerine özgü neoantijenler belirlenir.
-
Bu neoantijenler, immün sistemin güçlü bir yanıt oluşturabileceği hedefler olarak seçilir.
-
-
Aşı Bileşenlerinin Hazırlanması:
-
Seçilen neoantijenler, sentetik peptidler olarak üretilir.
-
Bu peptidler, bağışıklık sistemini harekete geçirmek için uygun taşıyıcı moleküllerle birleştirilir.
-
Aşı, hastanın bağışıklık sisteminin tümör hücrelerini spesifik olarak hedef almasını sağlayacak şekilde formüle edilir.
-
-
Aşının Hastaya Uygulanması:
-
Aşı, deri altına veya kas içine enjeksiyon yoluyla hastaya uygulanır.
-
Aşının uygulanması birkaç doz halinde gerçekleştirilir ve belirli aralıklarla takviye dozları verilir.
-
-
Bağışıklık Yanıtının Takibi:
-
Aşılanan hastaların bağışıklık tepkisi düzenli olarak izlenir.
-
Kan örnekleri alınarak T hücrelerinin aktivitesi ve sayısı ölçülür.
-
Gelişen immün yanıt, kalan tümör hücrelerinin ortadan kaldırılıp kaldırılmadığını belirlemek için değerlendirilir.
-
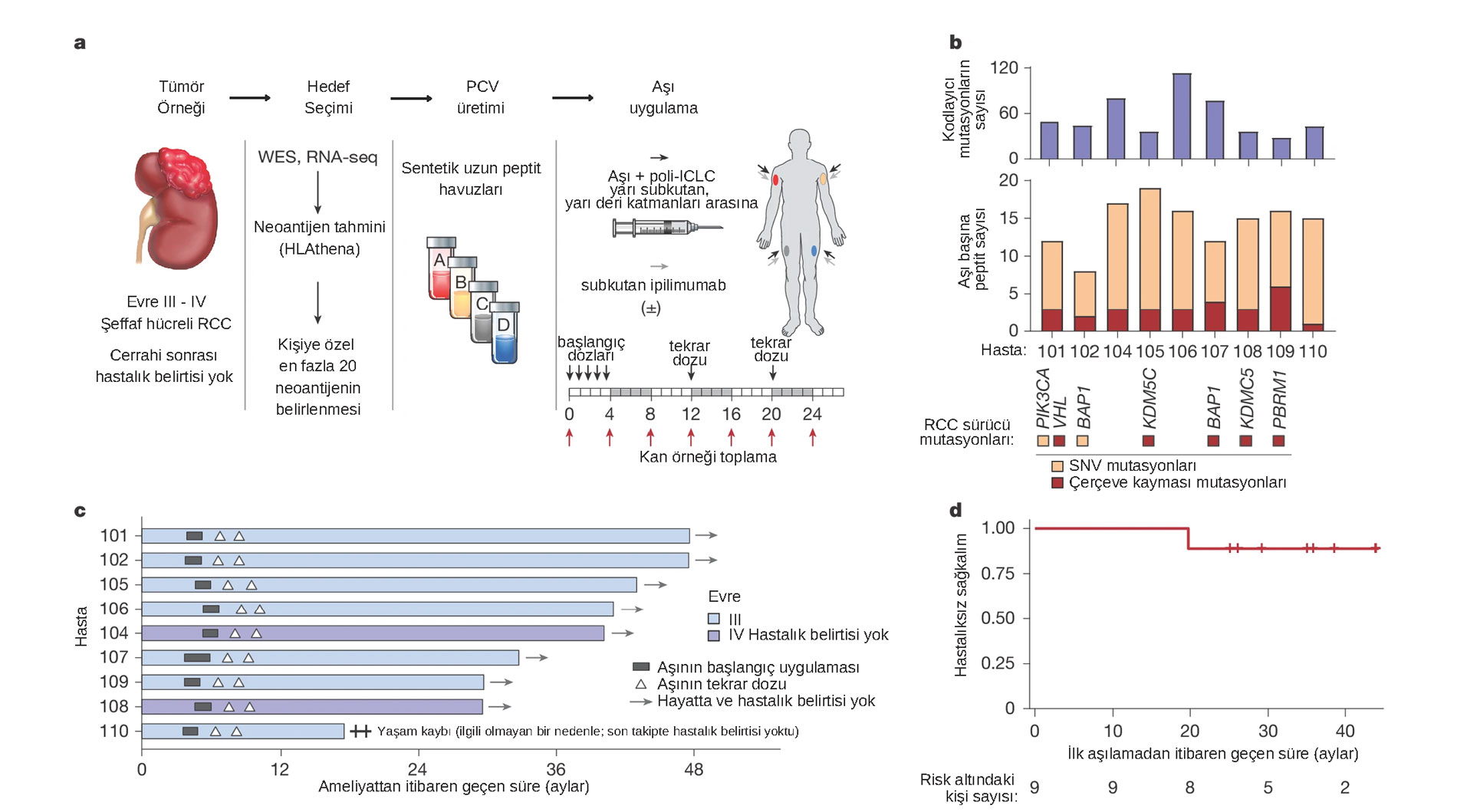
GÖRSEL: Berrak Hücreli Renal Hücreli Karsinom (bhBHK) için Neoantijen Hedefli Kişiselleştirilmiş Kanser Aşısının (PCV) Üretimi ve Uygulama Süreci
a. Neoantijen Hedefli Kanser Aşısının Tasarımı ve Uygulama Süreci
Bu şemada, bhBHK için geliştirilen kişiselleştirilmiş kanser aşısının (PCV) tasarım ve uygulama süreci gösterilmektedir.
- Tümör Örneği: Evre III-IV BHK hastalarından alınan tümör örnekleri kullanılmıştır.
- Genetik Analiz: Tümör örneklerinden tüm ekzon dizileme (WES) ve RNA dizileme (RNA-seq) yapılarak neoantijenler tahmin edilmiştir (HLAthena kullanılarak).
- Hedef Seçimi: Kişiye özel en fazla 20 neoantijen belirlenmiştir.
- Aşı Üretimi: Neoantijenlere özgü sentetik uzun peptit havuzları oluşturulmuştur.
- Aşı Uygulaması:Aşı, poli-ICLC (immün yanıt güçlendirici) ile birlikte uygulanmıştır.
- Aşının yarısı subkutan (deri altı), diğer yarısı intradermal (deri katmanları arasında) verilmiştir.
- Bazı hastalara ayrıca subkutan ipilimumab immünoterapisi uygulanmıştır.
- Kan Örnekleri Toplama: 24 hafta boyunca belirli zaman noktalarında kan örnekleri alınmıştır (kırmızı oklarla gösterilmiştir).
b. Aşı Üretimi ve Neoantijen Seçimi
Bu grafik, aşı üretim sürecinin özetini sunmaktadır:
- Üst Grafik: Her tümörde bulunan yüksek kaliteli kodlayıcı mutasyonların sayısı.
- Orta Grafik: Hastalara verilen neoantijen aşı peptitlerinin sayısı.
- Alt Grafik: Aşıda hedeflenen BHK'ye özgü sürücü mutasyonlar. Bunlar arasında PIK3CA, VHL, BAP1, KDM5G, KDM5C, PBRM1 gibi gen mutasyonları bulunmaktadır.
- SNV (tek nükleotid varyantı) ve çerçeve kayması mutasyonları, mutasyon türüne göre ayrı gösterilmiştir.
c. Hastaların Takip Süreci (Swimmer's Plot)
Bu grafik, her hastanın nefrektomi sonrası takip sürecini ve klinik durumlarını göstermektedir:
- Çubuklar: Hastaların ameliyat sonrası takip sürelerini göstermektedir.
- Renkler: Hastaların Evre III veya IV olup olmadığını belirtmektedir.
- Semboller:
- Kare (■): Aşı uygulamasının başlangıcı.
- Üçgen (△): Aşının tekrar dozu.
- Oklar (→): Hastanın hayatta olduğunu ve hastalık belirtisi taşımadığını göstermektedir.
- Artı (✚): İlgili olmayan bir nedenle yaşam kaybı, ancak son takipte hastalık belirtisi bulunmamıştır.
d. Hastalıksız Sağkalım (Kaplan–Meier Eğrisi)
Bu Kaplan–Meier sağkalım analizi, aşının ilk dozunun uygulanmasından itibaren hastalıksız sağkalım oranlarını göstermektedir.
- X Ekseni: İlk aşılamadan itibaren geçen süre (ay).
- Y Ekseni: Hastalıksız sağkalım oranı.
- Kırmızı çizgi: Takip edilen hastaların zaman içindeki hastalıksız sağkalımını göstermektedir.
- Alt kısımda yer alan sayılar: Risk altındaki kişi sayısını göstermektedir.
Bu çalışma, kişiselleştirilmiş kanser aşılarının RCC hastalarında hastalık nüksünü önleme potansiyelini değerlendirmek için yapılmıştır.
Nature Çalışmasının Detayları ve Sonuçlar
Bu erken aşama (faz I) klinik çalışma kapsamında, Evre III veya IV bhBHK tanısı alıp cerrahi ile tümörü alınan dokuz hasta değerlendirilmiştir. Bu hastalardan beşi, aşı ile birlikte ipilimumab (bir başka immün kontrol noktaları inhibitörü) almıştır.
En çarpıcı sonuçlar:
-
34,7 aylık takip süresinin sonunda, tüm hastalar hastalıktan arınık kalmıştır (kanser tekrarı olmamıştır).
-
Aşı, hastaların immün sistemini 3 hafta içinde harekete geçirerek kanserle sıkı şekilde ilişkilendirilmiş T hücrelerini 166 kat artırma kapasitesine sahip olmuştur.
-
T hücreleri, hastalığın başlangıcından 3 yıl sonrasına kadar yüksek seviyelerde kalmıştır.
-
Aşı, kanser hücrelerine karşı özel immün yanıt oluşturduğunu göstermiştir.
-
Tüm hastalarda immün yanıt oluştuğu belirlenmiştir ve yedi hastada aşının kanser süreci ile ilişkilendirilen özel gen mutasyonlarına (örneğin VHL, PBRM1, BAP1) karşı etki ettiği gözlemlenmiştir.
-
Ciddi yan etkilere rastlanmamış, yan etkiler yerel deri reaksiyonları ve gribal semptomlar ile sınırlı kalmıştır.
Sonuç ve Gelecek Perspektifler
Bu çalışmanın sonuçları oldukça umut vericidir; aşı, düşük mutasyonel yüke sahip böbrek kanseri gibi tümörlere karşı etkili bir tedavi seçeneği sunabilir.
Ayrıca, bu kişiselleştirilmiş aşı yaklaşımı, daha önce melanoma gibi yüksek mutasyon yükü olan kanserlerde başarılı bulunmuştu. Ancak bhBHK gibi daha az mutasyona sahip kanserlerde de etkili olabileceği bu çalışmayla kanıtlandı.
Kod adı V940 olan ve aynı zamanda mRNA-4157 olarak da bilinen bir başka kişiselleştirilmiş kanser aşısının büyük ölçekli, uluslararası ve randomize faz II çalışmasında (NCT06307431) aşı, pembrolizumab ile kombinasyon halinde adjuvan tedavi olarak değerlendirilmektedir.
Eğer bu ileri düzey denemeler de başarılı olursa, kişiselleştirilmiş kanser aşıları, böbrek kanseri ve diğer düşük mutasyonel yükteki tümörler için yeni bir standart tedavi seçeneği haline gelebilir.
Braun, D.A., Moranzoni, G., Chea, V. et al. A neoantigen vaccine generates antitumour immunity in renal cell carcinoma. Nature (2025). https://doi.org/10.1038/s41586-024-08507-5