
KRAS G12C Mutasyonlu Teedaviye Dirençli Kolorektal Kanserde Sotorasib ve Panitumumab
KRAS G12C mutasyonu, metastatik kolorektal kanserli hastaların yaklaşık %3-4'ünde görülür. KRAS G12C inhibitörleri ile yapılan tekli tedaviler, bu hasta grubunda sınırlı etkililik göstermiştir. Epidermal büyüme faktörü reseptörü (EGFR) inhibitörü panitumumab ile KRAS G12C inhibitörü sotorasib kombinasyonunun, yeni ve etkili bir tedavi stratejisi olduğu, sonuçları 7 Aralık 2023'te NEJM dergisinde yayımlanan CodeBreaK 300 çalışmasında gösterildi.
Kolorektal Kanserde KRAS G12C Mutasyonunu Hedef Almak
Kolorektal kanser tedavisinde, hedef odaklı yaklaşımların önemi her geçen gün artmaktadır. KRAS G12C mutasyonu, bu alandaki yenilikçi tedavi stratejilerinin öncüsü haline gelmiştir.
CodeBreaK 300 çalışması, kolorektal kanserde KRAS G12C mutasyonunu hedef alan ilk randomize çalışma olma özelliğini taşıyor.
RAS, "Rat Sarcoma" virüsünün kısaltmasıdır ve bu isim, bu gen ailesinin ilk kez sıçan sarkom virüslerinde keşfedilmesinden gelmektedir. İnsanlarda RAS gen ailesi, hücre büyümesi, farklılaşması ve hayatta kalması gibi temel işlevleri düzenleyen proteinleri kodlar. İnsanlarda bu aile, özellikle üç önemli onkogeni içerir: HRAS, KRAS ve NRAS.
RAS sinyal yolu, karsinogenezdeki 10 önemli sinyal yolağından biridir. RAS genleri, normal hücre işlevlerinde hayati öneme sahip olmasına rağmen, mutasyona uğradığında onkojenik özellikler kazanırlar ve kanser gelişimini tetikleyebilirler. Mutasyona uğramış RAS genleri, özellikle kolorektal kanser, pankreatik kanser, akciğer kanseri ve melanom dahil olmak üzere birçok farklı kanser türüyle ilişkilendirilmiştir.
KRAS G12C Mutasyonuna Sahip Hücrelerde Sinyalleşme

Yukarıdaki şema, KRAS G12C mutasyonuna sahip hücrelerdeki sinyalizasyonu göstermektedir.
- Panel A: Görselin bu kısmı, bir sinyalizasyon ağının basit bir örneğini gösterir. Burada, hücrelerin dışındaki sinyalleri alıp yanıt veren bir enzim olan ekstrasellüler sinyal ilişkili kinazın (ERK) tüm aktivasyonunun, Kirsten rat sarkoma viral onkojen homoloğu (KRAS) adı verilen bir genin aktivasyonu ile tetiklendiği anlatılır. Bu, KRAS'ın hücre içi sinyalizasyon mekanizmalarında ne kadar merkezi bir rol oynadığını vurgular.
- Panel B: Bu kısımda, kolon ve rektumun epitel dokusu (iç astarı) gibi bazı dokularda bulunan reseptör tirozin kinazların (RTK) işlevi gösterilir. Aktive edilmiş ERK, RTK sinyalizasyonunu engelleyen negatif geri besleme döngüleri yaratır. Bu, ERK'nin aktivasyonunun, RTK sinyalizasyonunu baskıladığı bir mekanizmayı temsil eder.
- Panel C: Bu kısım, KRAS genindeki belirli bir mutasyon olan KRAS G12C'nin tedavisi sırasında nasıl davrandığını gösterir. Bu mutasyonda, KRAS geninin 12. kodonunda glisin amino asidi sistin ile değiştirilmiştir. Bu mutasyonun tedaviye özgü inhibisyonu, ERK'nin inhibe edilmesiyle sonuçlanır ve bu da negatif geri besleme döngülerinin kaldırılmasına yol açar. Sonuç olarak, RTK sinyalizasyonu ve ardışık sinyalizasyon mekanizmaları aktive olur. Buna karşın, bu süreç aynı zamanda, tedaviye rağmen ERK sinyalizasyonunun yeniden başlamasına ve ilaca dirençli RAS protein varyantlarının oluşumuna neden olabilir. Bu, kanser tedavisindeki bazı zorlukları ve potansiyel direnç mekanizmalarını gösterir.
Kısaltmalar: Epidermal büyüme faktörü reseptörü (EGFR), guanozin difosfat (GDP), guanozin trifosfat (GTP), mitojen aktive protein kinaz (MEK) ve nöroblastoma ras viral onkojen homoloğu (NRAS). Okların kalınlığı, sinyalin göreceli gücünü gösterir.
CodeBreaK 300 Çalışmasının Detayları
Faz 3, çok-merkezli, açık etiketli, randomize CodeBreaK 300 çalışmasına, daha önceki kemoterapilere direnç gelişmiş metastatik kolorektal kanserli hastalar alındı.
Hastalar şu tedavileri aldı:
- Sotorasib 960 mg + panitumumab (53 hasta)
- Sotorasib 240 mg + panitumumab (53 hasta)
- Standart bakım (trifluridin-tipirasil/regorafenib) (54 hasta)
Çalışmada ölçülmesi hedeflenen birincil sonlanım noktası, kör bağımsız inceleme tarafından değerlendirilen progresyonsuz (ilerlemesiz) sağkalım (PFS) idi. İkincil son noktalar, genel sağkalım, objektif yanıt oranı idi.
Sonuçlar
- Ortanca takip süresi: 7.8 ay
- PFS:
- Sotorasib 960 mg + panitumumab: 5.6 ay
- Sotorasib 240 mg + panitumumab: 3.9 ay
- Standart tedavi: 2.2 ay
- Standart bakıma göre hastalık riskinde azalma: 960 mg için %51 (HR: 0.49 %95 GA 0.30-0.80), 240 mg için %42 (HR 0.58 %95 GA 0.36-0.93).
- Genel sağkalım verileri henüz olgunlaşmadı
- Objektif yanıt oranları:
- Sotorasib 960 mg + panitumumab: %26.4
- Sotorasib 240 mg + panitumumab: %5.7
- Standart tedavi: %0
- Derece 3/4 yan etkiler:
- Sotorasib 960 mg + panitumumab: %35.8
- Sotorasib 240 mg + panitumumab: %30.2
- Standart tedavi: %43.1
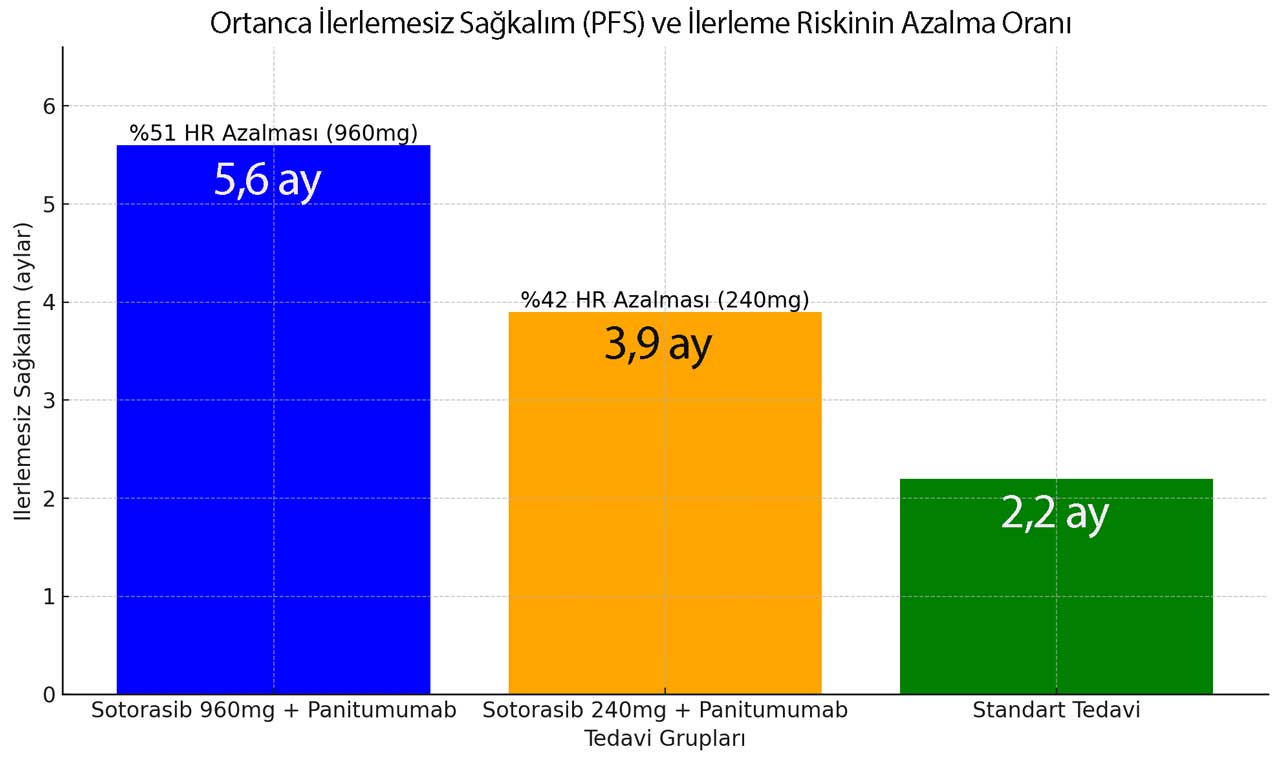
Sonuç olarak her iki sotorasib dozu da, panitumumab ile kombinasyon halinde, kemoterapiye dirençli KRAS G12C mutasyonlu metastatik kolorektal kanserli hastalarda standart tedaviye göre PFS'yi önemli ölçüde iyileştirdi. Toksisite yönetilebilir seviyede olup, her ajanın bireysel profilinde tutarlılık göstermektedir.
Çalışmanın Editör Yorumu
Bu çalışmada, Fakih ve arkadaşları CodeBreaK 300 adlı faz 3 deneyinin sonuçlarını bildiriyorlar. Bu deney, metastatik kolorektal kanseri olan ve KRAS G12C mutasyonuna sahip hastalarda, seçici Kirsten rat sarkoma viral onkojen homoloğu (KRAS) glisin'den sistin'e mutasyonu üzerinde etkili bir inhibitör olan sotorasib ile epidermal büyüme faktörü reseptörü (EGFR) inhibitörü panitumumab kombinasyonunu test etti. Bu deneyde, tam doz sotorasib (günde bir kez 960 mg) ile panitumumab alan ve daha düşük doz sotorasib (günde bir kez 240 mg) ile panitumumab alan iki araştırma grubu, standart 3. ve 4. basamak tedavisi alan bir grupla karşılaştırılmıştır. İki sotorasib–panitumumab grubunda ilerlemesiz sağkalım süresi, standart bakım grubuna göre önemli ölçüde daha uzundu. Bu, kolorektal kanser hastalarında KRAS hedefli tedavinin kullanımını destekleyen veriler sunan ilk randomize deneydir.
Neden Kombine Ajan?
CodeBreaK 300 deneyinde, araştırma grupları aktive onkogen olan mutasyonlu KRAS G12C ve EGFR inhibitörü ile kombinasyon tedavisi aldılar. Bu kombinasyon yaklaşımını destekleyen veriler, BRAF V600E veya KRAS G12C inhibitörlerinin preklinik ve klinik çalışmalarından gelmektedir ve bu çalışmalar, sadece onkogeni hedef almanın kolorektal kanserli hastalarda yetersiz olduğunu göstermiştir. BRAF V600E mutasyonuna sahip tümörler, kombinasyon tedavisinin neden gerektiğini anlamada iyi bir model sunar. BRAF V600E mutasyonuna sahip bazı kanserler, BRAF V600E'nin inhibisyonunun ekstrasellüler sinyal ilişkili kinaz (ERK) sinyalizasyonunu derinden bastırdığı daha basit bir sinyal ağına sahiptir. Ancak bağırsakta, özellikle EGFR olmak üzere, reseptör tirozin kinazları (RTK'lar) daha yüksek düzeyde ifade edilir. Bu reseptörler, BRAF V600E ile ilişkili yüksek ERK aktivitesinin reseptör sinyalizasyonunu bastıran negatif geri besleme döngülerini aktive ettiği için, mutasyona uğramış BRAF V600E ile kolorektal kanserde önemli ölçüde sinyalizasyona katkıda bulunmaz.
Tedavi başlatıldığında ve ERK inhibe edildiğinde, reseptörler bu negatif geri besleme döngüsünden serbest bırakılır, bu da ERK yolunun aktivasyonuna, tedaviye rağmen ERK sinyalizasyonunda bir geri tepmeye ve ilaca dirençli RAF dimerlerinin oluşumuna yol açar. Bu kombinasyon tedavisindeki EGFR inhibitörü, bu geri besleme reaktivasyonunu inhibe etmek için kullanılır. KRAS G12C inhibitörlerinin varlığında, EGFR inhibitörleri benzer bir şekilde EGFR'nin negatif geri besleme döngülerinden serbest bırakılmasını hedef alır ve EGFR'nin akış aşağısında ilaca dirençli sinyalizasyonun (yani, wild tip KRAS ve nöroblastoma ras viral onkojen homoloğu [NRAS]) oluşumunu önler.
Kolorektal kanserlerle ilişkili olmayan epitelyal tümörlerde RTK'ları hedef almanın KRAS G12C inhibitörlerine yanıt oranını artırıp artırmayacağı bilinmiyor; KRAS G12C inhibitörlerinin EGFR antikorları ile birlikte akciğer ve pankreas kanserli hastalarda değerlendirildiği bir klinik deneme devam etmektedir.
Neden Daha Yüksek Doz?
Kolorektal kanserle ilişkili olarak görülen yüksek düzeyde RTK'lar, tümör küçülmesini sağlamak için ERK yolunu yeterince inhibe etmek için gereken eşiği etkili bir şekilde yükseltir. ERK aktivasyonunun tümünü inhibe etmek için daha yüksek bir ilaç dozu gereklidir. CodeBreaK 300 deneyinin sonuçları, klinik dozlarda mevcut KRAS G12C inhibitörlerinin, daha güçlü ilaçların veya daha yüksek ilaç dozlarının yanıt oranını gerçekten değiştirdiği eşikte olduklarını göstermektedir. Küçük örnek boyutuna rağmen, daha yüksek doz sotorasib ile daha düşük doz sotorasibden daha yüksek bir yanıt oranı ve daha uzun ilerlemesiz sağkalım süresi gözlemleyebiliyoruz.
Daha az belirgin bir RTK ağı içeren kanserlerde, farklı KRAS G12C inhibitörleri arasında ve sotorasibin farklı dozları arasında tedavi yanıtında bu kadar belirgin farklar yoktur. Bu sonuçlar, moleküler olarak hedeflenmiş ajanların doz seviyelerinin, etkinliği ve güvenliği en üst düzeye çıkarmak için uygun olabileceğini belirlemek için tasarlanmış FDA'nın Optimus Projesi için önemlidir. Hedeflenen tedavilere yanıt almak için derin hedef inhibisyonu gereklidir, ancak bu yanıtı elde etmek için gereken doz tümör tipleri arasında değişiklik gösterir. Toksik etkileri yönetmek için ilaç dozunun düşürülmesi, ilacın bazı kanserlere karşı etkinliğini sınırlayabilir.
KRYSTAL-10 Denemesi Sonuçları Önemli
CodeBreaK 300 deneyinde, ilerlemesiz sağkalım birincil son noktaydı. Kemoterapilere dirençli metastatik kolorektal kanserli bu hasta grubunda nihai genel sağkalım sonuçlarını görmek önemli olacaktır. Bu deneyden elde edilen olgun veriler ve KRYSTAL-10'dan elde edilen veriler, çok ihtiyaç duyulan içgörüleri sağlayacaktır. KRYSTAL-10, ileri evre solid tümörlerde KRAS G12C mutasyonu olan hastalarda, ikinci basamak tedavi olarak KRAS G12C inhibitörü adagrasib ile EGFR antikoru setüksimabın standart kemoterapi ile karşılaştırıldığı faz 3 randomize bir deneydir.
Sonuç olarak CodeBreaK 300 deneyi, kolorektal kanserde KRAS genini hedef almanın önemli ve heyecan verici bir başlangıcıdır. Bu deney, KRAS G12C mutasyonuna sahip kanserler için özel olarak geliştirilen inhibitörlerin etkinliğini test etmiş ve bu alandaki araştırmaları önemli ölçüde ilerletmiştir. KRAS G12C inhibitörleri gibi yeni RAS inhibitörlerinin geliştirilmesi ve tedaviye direnç mekanizmalarının daha iyi anlaşılması sayesinde, KRAS mutasyonu taşıyan kolorektal kanser hastaları için daha etkili terapötik stratejiler geliştirme umudu artmaktadır.
1. Fakih MG, Salvatore L, Esaki T, Modest DP, Lopez-Bravo DP, Taieb J, Karamouzis MV, Ruiz-Garcia E, Kim TW, Kuboki Y, Meriggi F, Cunningham D, Yeh KH, Chan E, Chao J, Saportas Y, Tran Q, Cremolini C, Pietrantonio F. Sotorasib plus Panitumumab in Refractory Colorectal Cancer with Mutated KRAS G12C. N Engl J Med. 2023 Dec 7;389(23):2125-2139. doi: 10.1056/NEJMoa2308795. Epub 2023 Oct 22. PMID: 37870968.
2. Yaeger R. Combination Therapy and Appropriate Dosing to Target KRAS in Colorectal Cancer. N Engl J Med. 2023 Dec 7;389(23):2197-2199. doi: 10.1056/NEJMe2311611. PMID: 38055257.






