
Tedaviye dirençli kabul edilen akciğer kanseri KRAS G12C mutasyonunda ilk tedavi onaylandı
28 Mayıs 2021'de FDA (ABD Gıda ve İlaç İdaresi), tümörleri KRAS G12C adı verilen özel bir genetik mutasyona sahip olan ve önceden en az bir sistemik tedavi almış olan küçük hücreli dışı akciğer kanseri (KHDAK) olan yetişkin hastalar için ilk tedavi olarak sotorasib (Lumakras, Amgen) adlı akıllı ilaca onay verdi. Bu, küçük hücreli olmayan akciğer kanserlerindeki mutasyonların yaklaşık %25'ini oluşturan herhangi bir KRAS mutasyonuna sahip tümörler için onaylanmış ilk hedefli tedavidir. KRAS G12C mutasyonları, küçük hücreli dışı akciğer kanserlerindeki mutasyonların yaklaşık %13'ünü temsil eder.
FDA ayrıca, KRAS G12C mutasyonunu test etmek için, QIAGEN therascreen® KRAS RGQ PCR kitini (doku) ve Guardant360® CDx'i (plazma) yardımcı teşhis olarak onayladı. Plazma örneğinde mutasyon saptanmazsa, tümör dokusu test edilmelidir.
KRAS G12C mutasyonu nedir?
KRAS, insan kanserlerinde en sık mutasyona uğrayan onkogenlerden (kanser genleri) biri olmuştur ve yakın zamana kadar ilaçlarla hedeflenemez olarak görülmüştür. Fakat KRAS-baskılayıcı sotorasib, yaygın bir KRAS mutasyonu olan G12C pozitif tümörler için umut oldu.

Şekil 1 açıklaması: KRAS proteini, normal hücre büyümesinde görev alan önemli moleküllerden biridir. KRAS geni tarafından üretimi sağlanan protein, dış ortamdan alınan sinyallerin hücre çekirdeğine iletiminde rol oynar. Mutasyona uğraması durumunda hücre "agresif" bir büyüme gerçekleştirir. Mutasyonlu KRAS, hücre dış ortamdan sinyal almasa bile sürekli "çoğal " komutunu gönderir. KRAS, akıllı ilaçlara karşı gelişen ilaç dirençliliğinden de sorumludur.
KRAS’ın 30 yıldır kanser gelişiminde kritik bir role sahip olduğu biliniyordu, bununla birlikte, KRAS mutasyonlarının kendine özgü biyolojisi nedeniyle bir antikanser ajanla hedeflenip susturulamamıştı.
KRAS G12C mutasyonunu etkili bir şekilde hedef alan ajanların keşifleri sadece bir başlangıçtır ve yalnızca diğer KRAS mutasyonlarını değil, aynı zamanda daha önce başarısız olduğu düşünülen diğer mutasyonları da hedefleme yeteneğinin ulaşılabilir olabileceği umudunu verir.
KRAS p.G12C mutasyonu en sık olarak küçük hücreli dışı akciğer kanserlerinde (KHDAK) bildirilmekle birlikte başta kolorektal kanserler olmak üzere diğer solid tümörlerde de görülmektedir. KHDAK’da görülme sıklığı %13, kolorektal kanserler için %1-7 arasıdır.
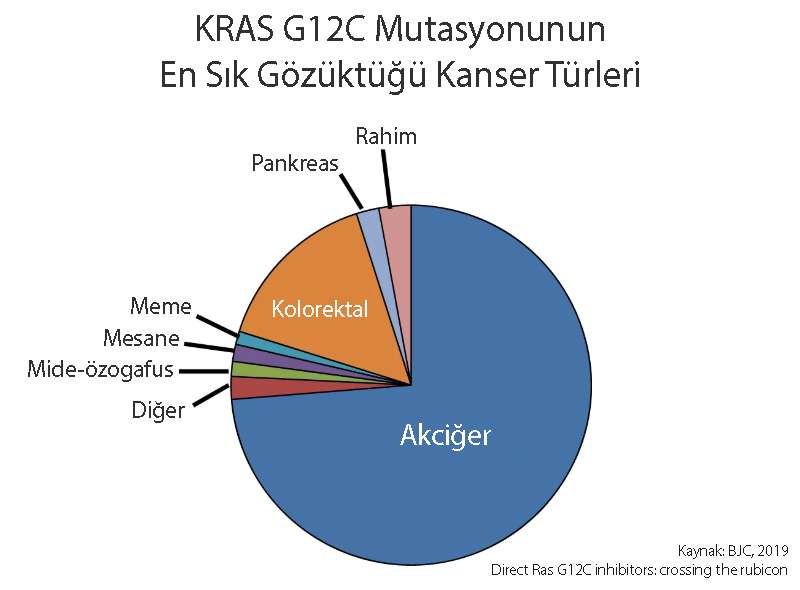
Şekil 2 açıklaması: KRAS G12C mutasyonu en sık olarak KHDAK'da, daha sonra kolorektal kanserlerde görülür. Sotorasibin FDA onayı sonrası, bu mutasyon, birçok solid (organ) kanserinin ileri evreleri için yeni bir biyobelirteç olarak klinik ortamda kullanılacaktır.
Yaşam kaybı oranı en yüksek olan en yaygın kanser türü olan akciğer kanserleri (bakınız Dünya Kanser İstatistikleri 2020), büyük ölçüde ona neden olan genetik mutasyonlara göre sınıflandırılabilir.
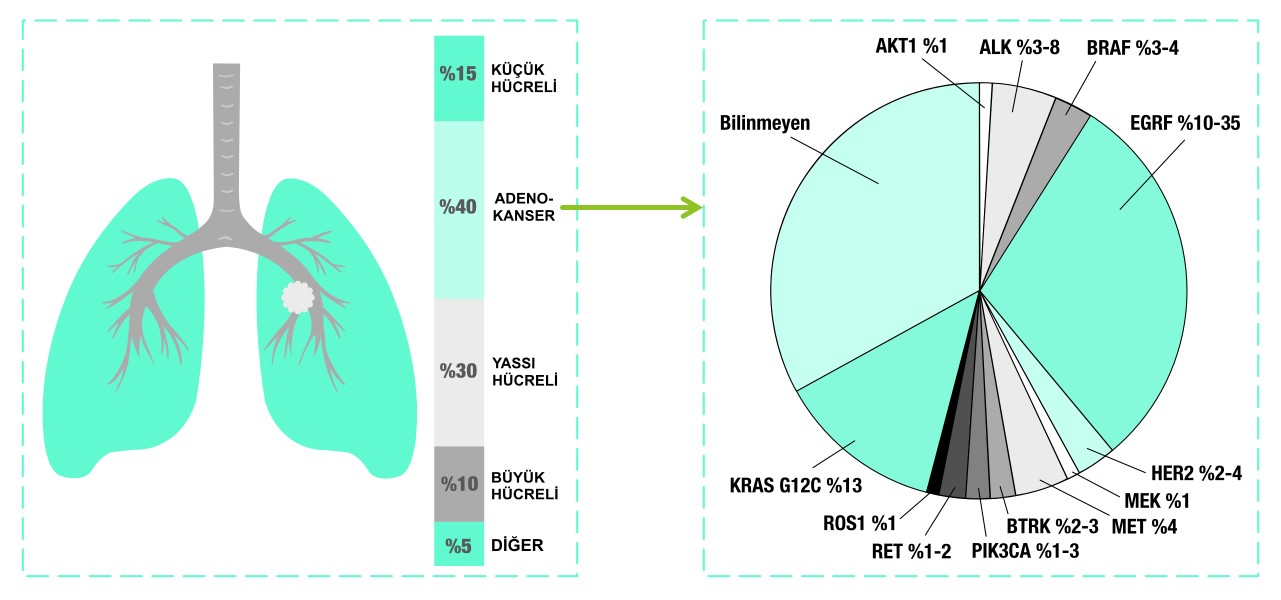
Şeklin 3 açıklaması: Yukarıda solda akciğer kanserlerinin histolojik olarak 5 ana türü olduğu görülebilir. Genetik olarak bakıldığında ise küçük hücreli dışı akciğer kanserlerinin bir alt türü olan akciğer adenokanserinin 12'den fazla türü olduğu görülebilir (sağdaki pasta grafik). Bu alt türlerden biri de KRA G12C mutasyonu pozitif akciğer kanserleridir.
CodeBreaK 100 çalışması
Araştırmacılar, bir immün kontrol noktası inhibitörü ve / veya platin bazlı kemoterapi aldıktan sonra hastalığın ilerlemesi olan lokal olarak ilerlemiş veya metastatik KRAS G12C mutasyona uğramış küçük hücreli olmayan akciğer kanseri olan 124 hastayı kapsayan bir çalışma olan CodeBreak 100 adlı klinik araştırmada Lumakras'ın etkinliğini değerlendirdiler. Ölçülen ana sonuçlar, objektif yanıt oranı (tümörü yok edilen veya küçülen hastaların oranı) ve yanıt süresiydi.
Objektif yanıt oranı %36 idi ve bu hastaların %58'inin yanıt süresi altı ay veya daha uzundu.
Onaylanmış 960 miligram doz, mevcut klinik verilere ve ayrıca onaylanmış dozu destekleyen farmakokinetik ve farmakodinamik modellemeye dayanmaktadır. Bu hızlandırılmış onay değerlendirmesinin bir parçası olarak, FDA, daha düşük bir dozun benzer bir klinik etkiye sahip olup olmayacağını araştırmak için bir pazarlama sonrası deneme talep ediyor.
Lumakras'ın en yaygın yan etkileri arasında ishal, kas-iskelet ağrısı, bulantı, yorgunluk, karaciğer hasarı ve öksürük bulunur. Hastalarda interstisyel akciğer hastalığı semptomları gelişirse Lumakras verilmemeli ve interstisyel akciğer hastalığı doğrulanırsa kalıcı olarak kesilmelidir. Doktorlar, Lumakras'ı kullanmaya başlamadan önce ve kullanırken hastanın karaciğer fonksiyon testlerini izlemelidir. Bir hastada karaciğer hasarı gelişirse, Lumakras kesilmeli, doz azaltılmalı veya kalıcı olarak kesilmelidir. Hastalar Lumakras alırken asit azaltıcı ajanları, karaciğerdeki belirli enzimleri indükleyen veya substratı olan ilaçları ve P-glikoprotein substratı olan ilaçları almaktan kaçınmalıdır.
FDA Approves First Targeted Therapy for Lung Cancer Mutation Previously Considered Resistant to Drug Therapy. fda.gov 28 May 2021






