
2025 Nobel Tıp Ödülü: İmmün Tolerans Keşfi ile Brunkow, Ramsdell ve Sakaguchi'ye Verildi
2025 Nobel Ödülü: Bağışıklık Sisteminin Gizli Dengesi
Vücudumuzun bağışıklık sistemi bir mucizedir: Her gün binlerce virüs, bakteri ve mikroba karşı bizi korur. Ancak bu güçlü sistemin dikkatle kontrol edilmesi gerekir. Aksi halde kendi organlarımıza saldırabilir ve otoimmün hastalıklar gelişebilir. İşte bu kritik denge, 2025 yılında Nobel Tıp Ödülü’ne konu oldu.
🏆 Ödülü Kimler Aldı?
Bu yıl Nobel Fizyoloji veya Tıp Ödülü Mary E. Brunkow, Fred Ramsdell ve Shimon Sakaguchi’ye verildi. Ödülün nedeni: “Periferik bağışıklık toleransına dair keşifleri”.
Bu üç bilim insanı, bağışıklık sistemimizin “güvenlik görevlileri” olan düzenleyici T hücrelerini (Treg) tanımlayarak yepyeni bir araştırma alanı başlattılar.
🔹 Kanser tedavilerinde daha etkili immünoterapilerin geliştirilmesi,
🔹 Otoimmün hastalıkların tedavisi için yeni yollar,
🔹 Kök hücre nakillerinden sonra ciddi komplikasyonların önlenmesi...
Hepsi bu keşiflerin sağladığı bilginin ürünü.
🛡️ Bağışıklık Sistemi Neden Bu Kadar Önemli?
Eğer bağışıklık sistemimiz olmasa, basit bir grip virüsü veya sıradan bir bakteri bile yaşamımızı tehdit edebilirdi. Bu sistemin en büyük başarısı, istilacı mikropları tanıyıp onları vücudun kendi hücrelerinden ayırt edebilmesidir.
Mikroplar tek tip değildir, farklı farklı şekillere sahiptir. Hatta bazıları kamuflaj yaparak insan hücrelerine benzemeye çalışır. Buna rağmen bağışıklık sistemi her gün milyonlarca hücreyi tarayarak “dost” ve “düşman” ayrımı yapar.
Bilim insanları uzun süre bu denetimin sadece “merkezi bağışıklık toleransı” sayesinde olduğunu düşünmüştü. Ancak Brunkow, Ramsdell ve Sakaguchi’nin çalışmaları, sistemin bundan çok daha karmaşık bir yapıya sahip olduğunu gösterdi.
🔬 1990’larda T Hücreleri: Bağışıklığın Ön Cephe Savaşçıları
1990’larda bilim insanlarının bildiği kadarıyla, bağışıklık sisteminin merkezinde T hücreleri yer alıyordu. Bu hücreler vücudun ön cephe savaşçıları gibiydi. Farklı tipleri vardı ve her biri bağışıklık savunmasında kritik görev üstleniyordu:
- Yardımcı T hücreleri (CD4⁺): Mikropları fark ettiklerinde diğer bağışıklık hücrelerini alarma geçirir, adeta komutan rolü oynar.
- Katil T hücreleri (CD8⁺): Virüsle enfekte olmuş veya tümörleşmiş hücreleri yok eder. Cerrah gibi hedefe odaklanır.
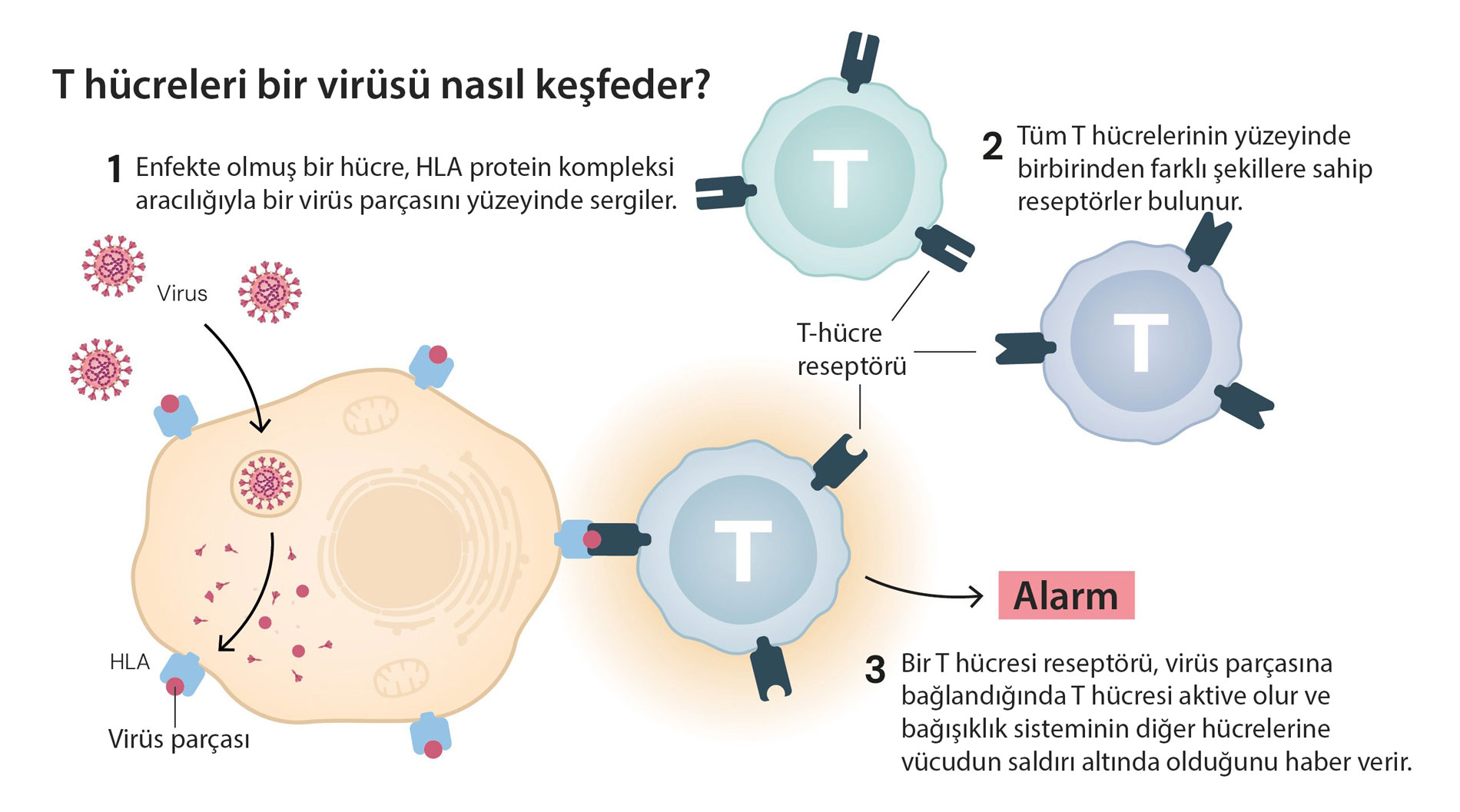
🧩 T Hücre Reseptörleri: Bağışıklığın Sensörleri
Tüm T hücrelerinin yüzeyinde T hücre reseptörleri bulunur. Bu reseptörler kilit-anahtar sistemi gibi çalışır. Her biri farklı bir şekle sahiptir ve adeta mikroskobik sensörler gibi düşünebiliriz.
Genetik kombinasyonların çeşitliliği sayesinde, teorik olarak 1015 farklı T hücre reseptörü üretilebilir. Bu muazzam çeşitlilik sayesinde bağışıklık sistemi, daha önce hiç karşılaşmadığı bir virüsü bile tanıyabilir. Nitekim 2019’da ortaya çıkan COVID-19 virüsü gibi yeni tehditlere karşı da bu mekanizma çalışmıştır.
⚖️ Merkezi Bağışıklık Toleransı: İlk Güvenlik Testi
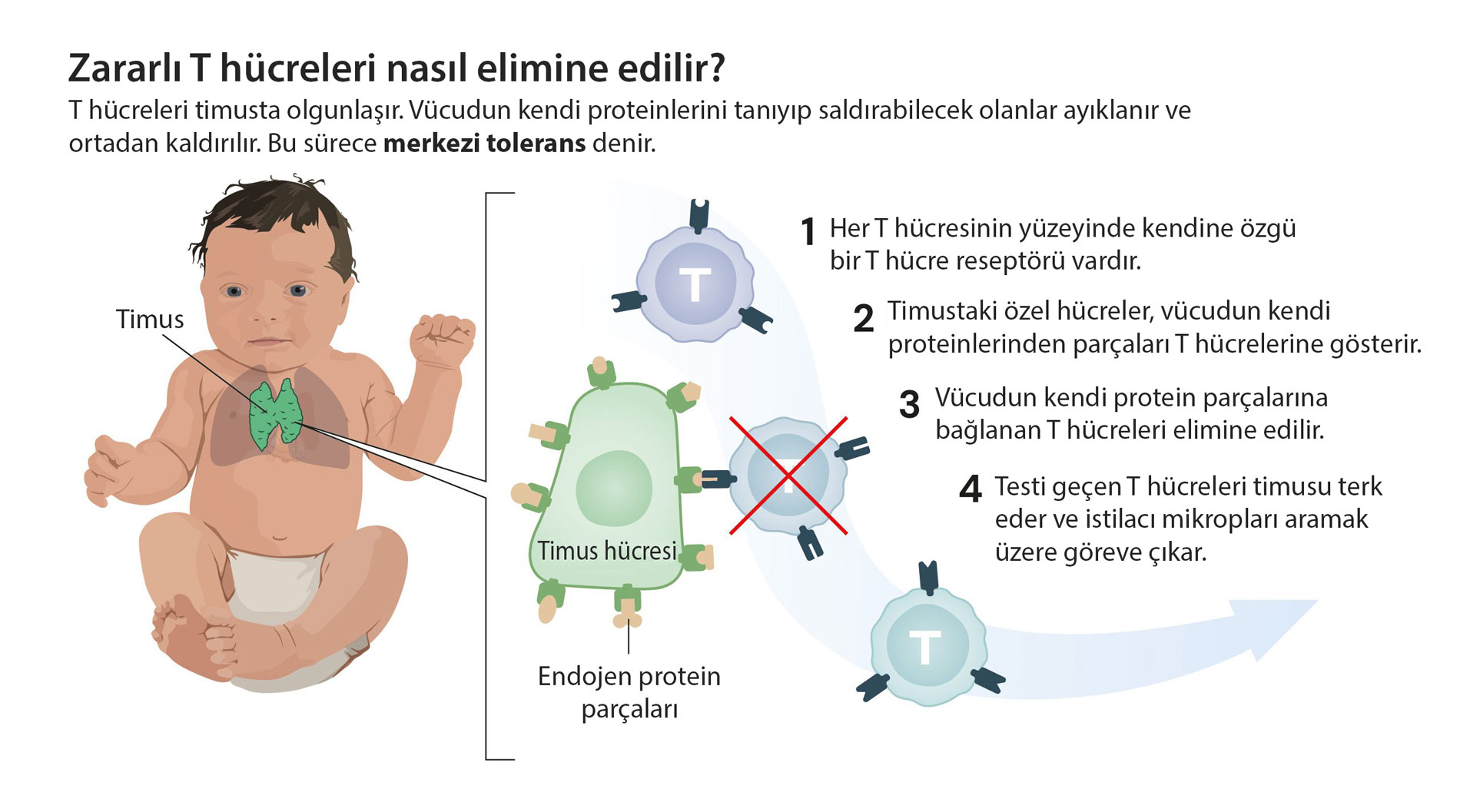
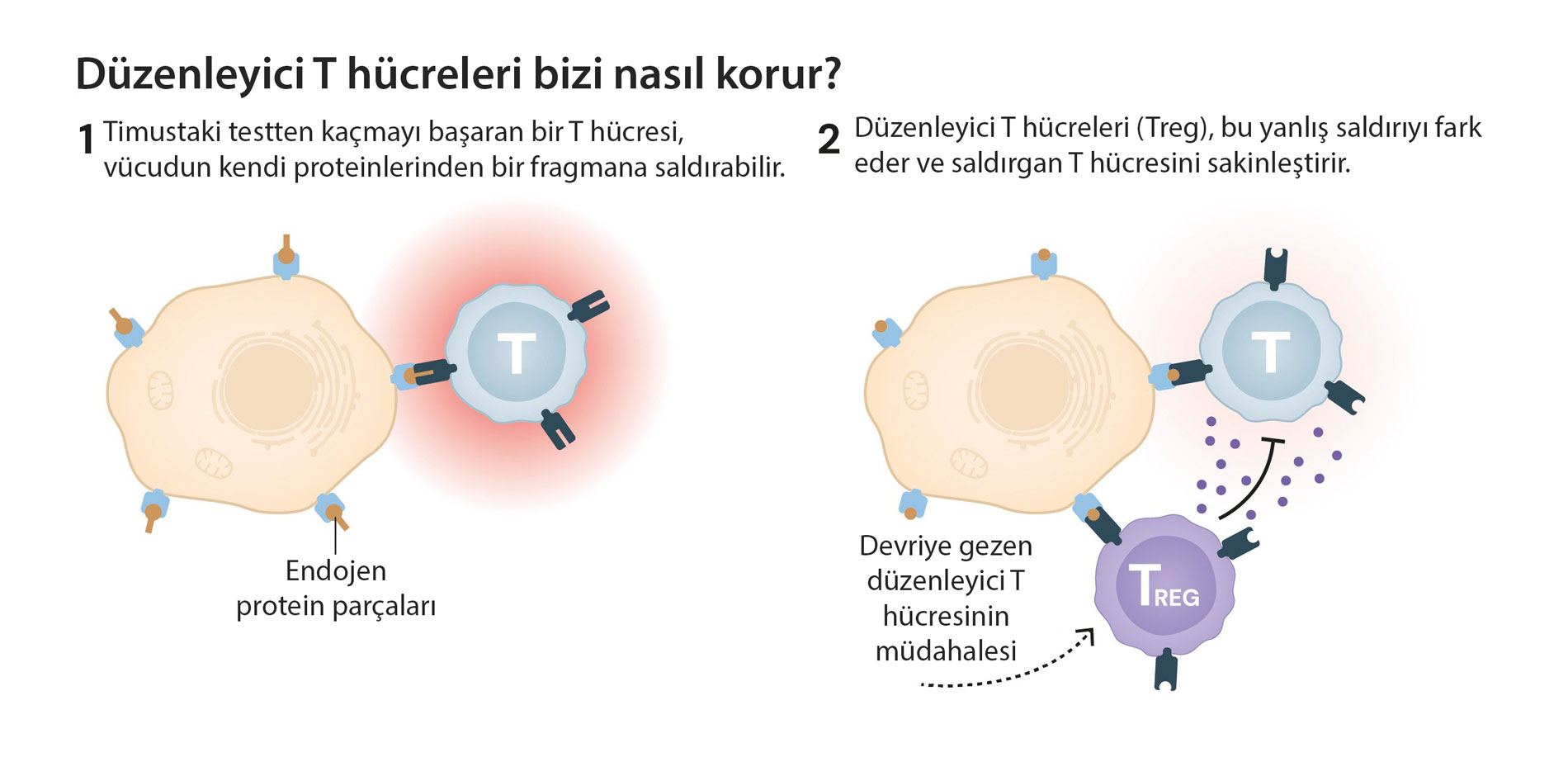
Bu çeşitlilik aynı zamanda risk taşır: Bazı T hücreleri yanlışlıkla vücudun kendi dokularını tanıyabilir. İşte bu yüzden bağışıklık sistemi, timus adı verilen organda bir tür test uygular. Buna “merkezi bağışıklık toleransı” denir.
Timusta olgunlaşan T hücreleri sıkı bir sınavdan geçer: kendi dokularını tanıyanlar yok edilir. Böylece otoimmün saldırıların önüne geçilir.
Ancak her zaman bazı hücreler bu testten kaçmayı başarır. İşte bu noktada bilim insanları uzun süre baskılayıcı T hücreleri
adı verilen bir hücre tipinin varlığını tartıştı. Fakat 1980’lerde sahte deney sonuçları yüzünden bu teori terk edildi ve araştırma alanı unutuldu.
❗ Ancak Shimon Sakaguchi bu akıntıya karşı kürek çekti. 1980’lerde yaptığı deneyler, bağışıklık sisteminin gerçekten de bir “güvenlik görevlisine” sahip olması gerektiğini düşündürdü.
Sakaguchi’nin Çıkış Noktası: “Bağışıklığın Güvenlik Görevlisi Olmalı”
1980’lerde baskılayıcı T hücreleri hipotezi, hatalı deneyler nedeniyle bilim dünyasında neredeyse tamamen terk edilmişti. Ancak Shimon Sakaguchi (Aichi Kanser Merkezi, Nagoya), akıntıya karşı giderek şu fikri savundu: Bağışıklık sistemi, timustaki elemeden kaçan hücreleri sakinleştirecek bir güvenlik görevlisine sahip olmalı.
Deneysel İpucu: Timus Çıkınca Ne Oluyor?
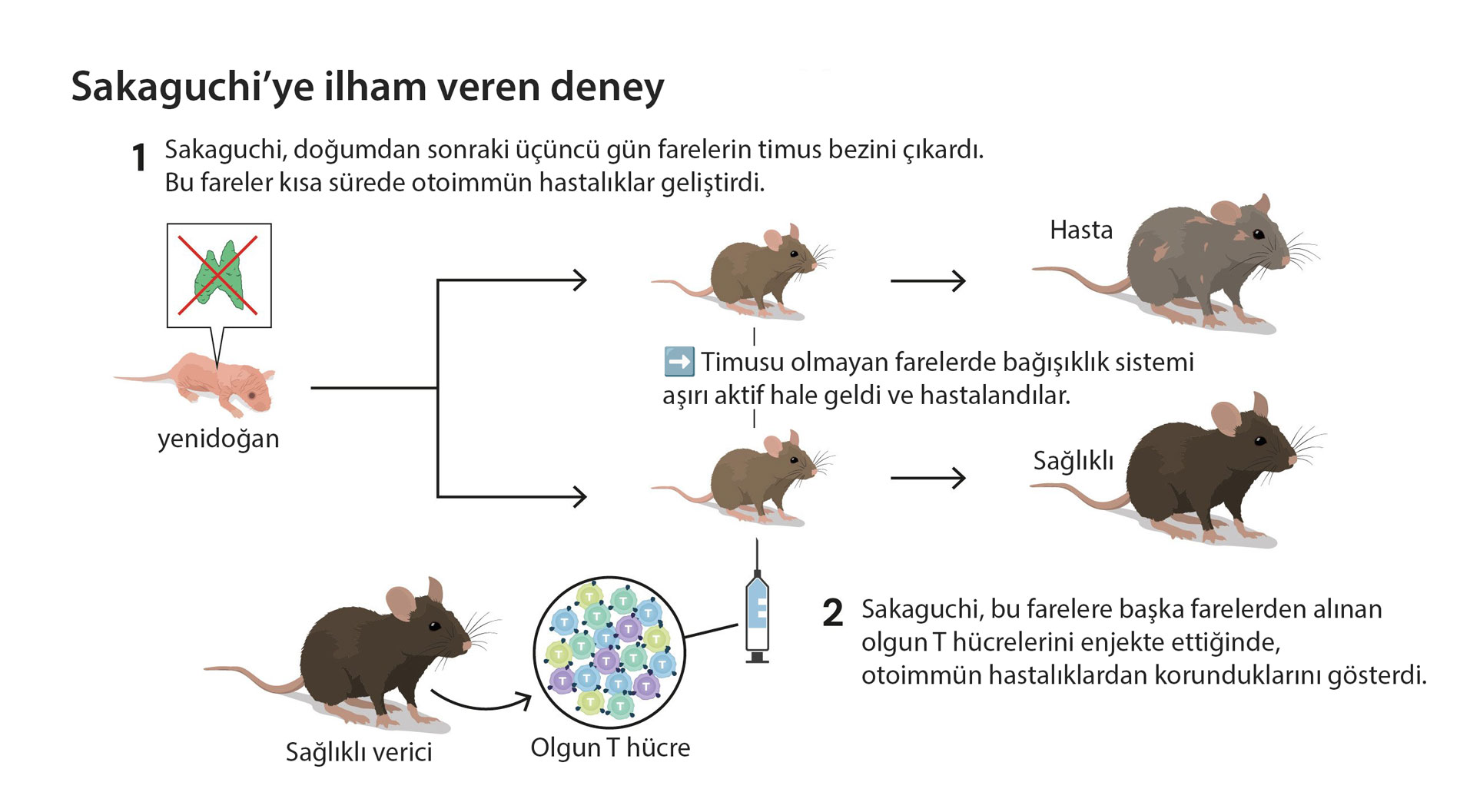
Araştırma çizgisini belirleyen gözlemlerden biri şuydu: Doğumdan kısa süre sonra timusu çıkarılan yavru farelerde bağışıklık sistemi aşırı aktif hale geliyor, çoklu otoimmün belirtiler ortaya çıkıyordu. Buna karşın, bağışıklık sistemi olgun T hücreleriyle desteklenen modellerde otoimmün fenotip baskılanıyordu. Bu, periferide frenleyici bir T hücresi alt grubunun varlığına işaret etti.
Çıkarım: Timustaki merkezi tolerans tek başına yeterli değil; periferide çalışan düzenleyici bir katman daha olmalı.
🧩 1995’te Kırılma: CD4⁺CD25⁺ Düzenleyici T Hücreleri
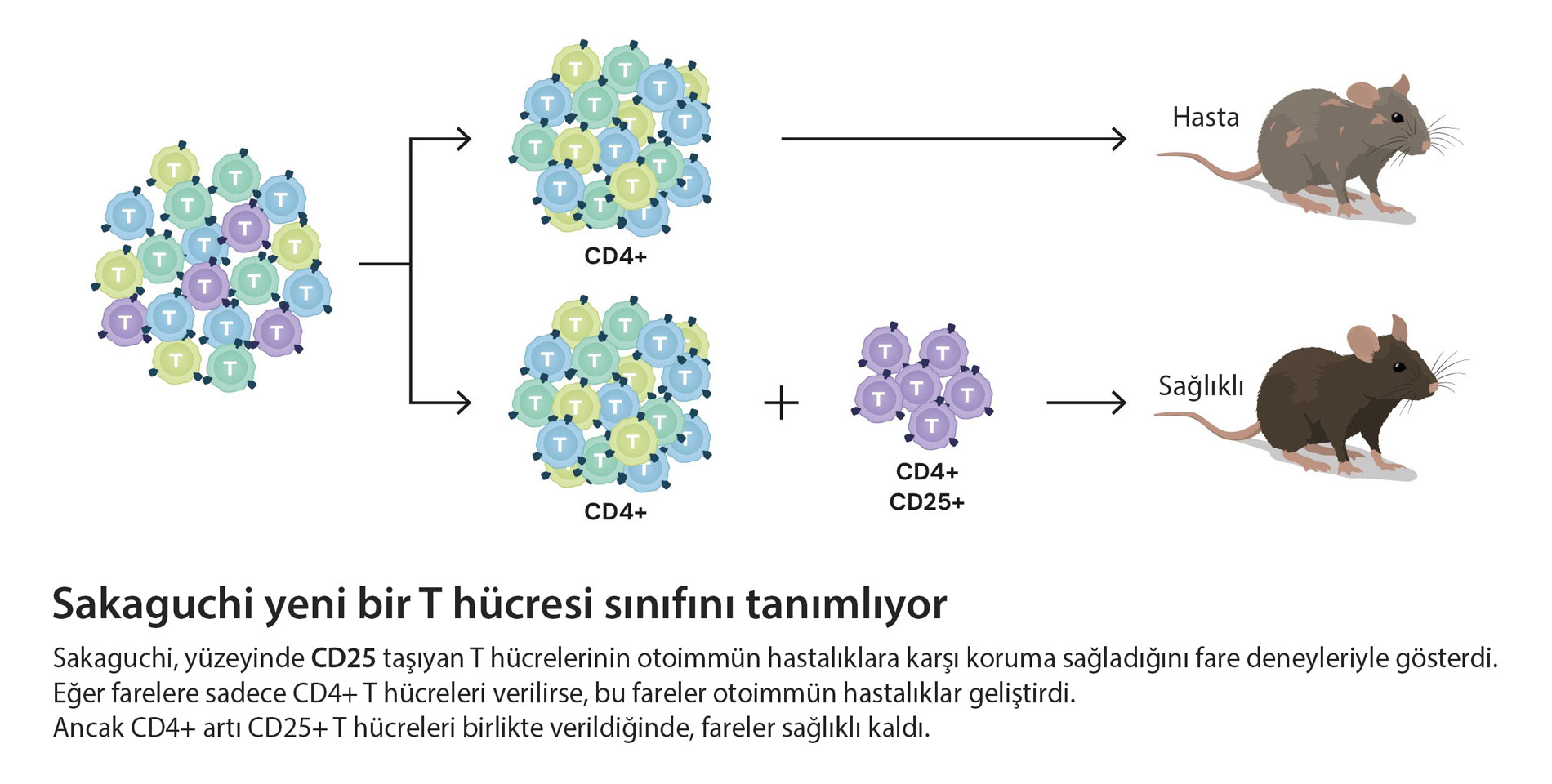
Uzun ve titiz bir ayrımlama sürecinden sonra Sakaguchi, CD4⁺ T hücrelerinin içinde CD25 taşıyan özel bir alt grup tanımladı: düzenleyici T hücreleri (Treg). Bu hücreler, klasik yardımcı T hücrelerinden farklı olarak immün yanıtı frenliyor, aşırılığı yatıştırıyor ve “kendine saldırı” riskini azaltıyordu (J Immunol, 1995).
- Fenotip: CD4⁺CD25⁺
- Temel işlev: Aşırı aktive T hücrelerini baskılayarak periferik toleransı sürdürmek
- Klinik ima: Otoimmünitenin baskılanması, greft reddinin azaltılması, tümör bağışıklığı dengesinde rol
🧭 Şüpheden Kabul’e: Treg’lerin Alanı Açılıyor
İlk tanımlama sonrası “gerçekten yeni bir alt grup mu?” sorusu sıkça soruldu; alan, ikna edici ek kanıtlar arıyordu. Bunu sağlayan dönüm noktalarından biri, FOXP3 adlı transkripsiyon faktörünün Treg gelişiminin ana düzenleyicisi olduğunun gösterilmesiydi (2003). Böylece hem fenotipik hem genetik çerçeve tamamlandı ve Treg biyolojisi sağlam bir zemine oturdu.
Laboratuvardan Kliniğe Köprü
Treg’lerin varlığı ve işlevinin netleşmesi, periferik tolerans kavramını bağışıklık tıbbının merkezine taşıdı: kanserde tümörlerin Treg biriktirerek kendini koruması; otoimmünitede Treg artırma stratejileri; nakillerde Treg ile tolerans indüksiyonu gibi çok sayıda klinik uygulama hattı doğdu.
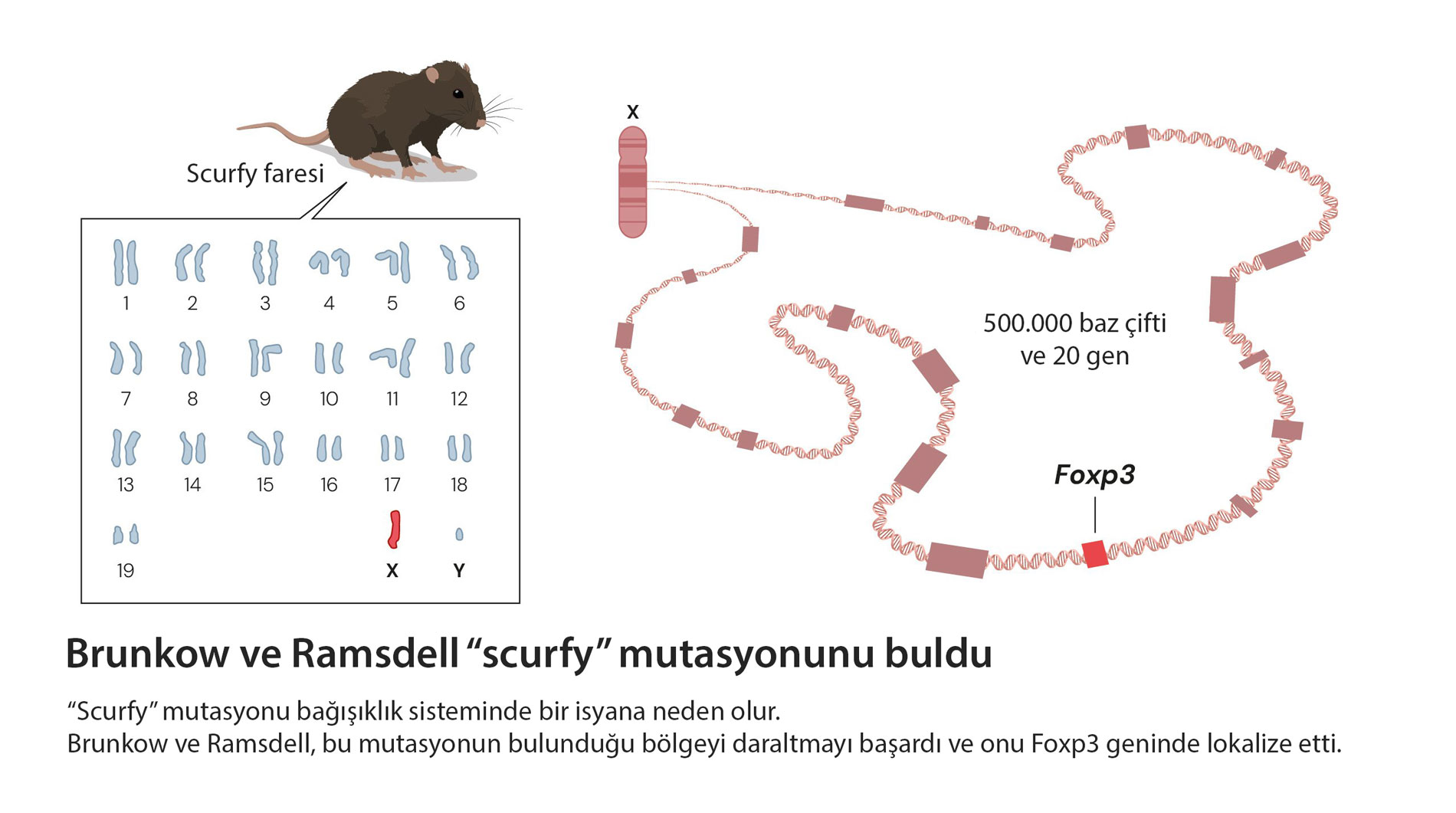
🧬 Scurfy Fareler: Mutasyondan Doğan İpucu
1940’larda Tennessee’deki Oak Ridge laboratuvarında, araştırmacılar beklenmedik bir mutasyonla karşılaştı. Erkek farelerin bir kısmı pullu deri, büyümüş dalak ve lenf bezleri ile doğuyor, sadece birkaç hafta yaşıyordu. Bu farelere “scurfy” adı verildi.
Araştırmacılar bunun X kromozomu üzerinde bir mutasyondan kaynaklandığını fark ettiler. Erkek fareler tek X kromozomuna sahip oldukları için hastalanıyor, dişiler ise taşıyıcı olabiliyordu.
🔎 Brunkow & Ramsdell: Otoimmünitenin Şifresini Aramak
1990’larda Mary Brunkow ve Fred Ramsdell, Washington’daki Celltech Chiroscience adlı biyoteknoloji şirketinde otoimmün hastalıklar üzerine çalışıyordu. Scurfy farelerdeki mutasyonun, insan otoimmün hastalıklarının mekanizmasını anlamak için bir anahtar olabileceğini düşündüler.
X kromozomundaki 170 milyon baz çiftini taramak samanlıkta iğne aramak gibiydi. Yıllar süren titiz bir çalışmadan sonra mutasyonu Foxp3 adını verdikleri yeni bir gende buldular.
📌 Keşif: Foxp3, forkhead box (FOX) gen ailesine ait bir transkripsiyon faktörüydü ve T hücrelerinin gelişimini kontrol ediyordu.
👶 İnsan Hastalığına Bağlantı: IPEX Sendromu
Brunkow ve Ramsdell, bu bulgunun insanlardaki nadir fakat ölümcül bir otoimmün hastalık olan IPEX sendromu (Immune dysregulation, Polyendocrinopathy, Enteropathy, X-linked) ile ilişkili olabileceğini fark ettiler.
Dünyanın dört bir yanındaki pediatristlerle iş birliği yaparak IPEX’li çocuklardan DNA örnekleri topladılar. Analizlerde FOXP3 geninde zararlı mutasyonlar bulundu. 2001’de Nature Genetics dergisinde yayımladıkları makale, hem scurfy farelerdeki hastalığın hem de insanlardaki IPEX’in aynı genetik kökene dayandığını kanıtladı.
💡 Bu bulgu, FOXP3’ün düzenleyici T hücrelerinin gelişiminde kilit rol oynadığını gösteren sonraki çalışmaların önünü açtı.
⚕️ Düzenleyici T Hücreleri: Laboratuvardan Kliniğe
Düzenleyici T hücreleri (Treg), bağışıklık sisteminin aşırılığını frenleyerek vücudu kendi kendine saldırıdan korur. Nobel ödüllü bu keşif, klinik tıpta üç büyük alanda devrimsel uygulamalara yol açtı:
- Kanser: Tümörler, çevrelerinde Treg hücrelerini biriktirerek bağışıklık sisteminin saldırısından korunur.
- Otoimmün Hastalıklar: Eksik veya yetersiz Treg fonksiyonu otoimmüniteye yol açar; bu yüzden tedavi hedefi Treg artırmak.
- Organ Nakilleri: Treg hücreleri tolerans oluşturarak organ reddini önleyebilir.
🎯 Kanser ve Treg Hücreleri
Kanser hücreleri adeta bir “kalkan” gibi Treg hücrelerini kendilerine çeker. Bu sayede bağışıklık sistemi tümörü fark etse bile, Treg hücreleri baskılayıcı sinyaller göndererek saldırıyı engeller.
📌 Klinik araştırmalarda amaç, bu Treg bariyerini ortadan kaldırmak ve bağışıklık hücrelerinin tümöre erişimini sağlamaktır.
🌀 Otoimmün Hastalıklarda Treg’in Rolü
Otoimmün hastalıklarda bağışıklık sistemi dost-düşman ayrımını kaybeder. İşte burada Treg hücrelerinin artırılması kritik bir tedavi stratejisi olabilir.
Klinik çalışmalarda düşük doz interlökin-2 (IL-2) verilerek Treg hücrelerinin çoğalması sağlanmaya çalışılıyor. Böylece bağışıklık sistemi frenleniyor ve hasar azaltılıyor.
🧪 Pilot çalışmalar, IL-2’nin organ reddini önlemede de kullanılabileceğini gösteriyor.
💉 Organ Nakillerinde Treg Stratejileri
Organ nakillerinde en büyük sorun, bağışıklık sisteminin yeni organı reddetmesidir. Bu nedenle araştırmacılar, hastadan alınan Treg hücrelerini laboratuvarda çoğaltıp yeniden hastaya vermeyi deniyorlar.
Hatta bazı çalışmalarda bu hücreler antikorlarla yönlendirilerek spesifik olarak nakledilen organa gönderiliyor. Böylece adeta bir “adres etiketi” sayesinde organ, bağışıklık saldırısından korunuyor.
🌟 Bu stratejiler sayesinde gelecekte immün baskılayıcı ilaçların azaltılması ve uzun süreli tolerans mümkün olabilir.
🔑 Sonuç: Bilimden İnsanlığa Büyük Katkı
Brunkow, Ramsdell ve Sakaguchi’nin keşifleri sayesinde bugün biliyoruz ki düzenleyici T hücreleri bağışıklık sisteminin denge noktasını belirliyor. Bu bilgi, kanserden otoimmün hastalıklara, organ nakillerinden kök hücre tedavilerine kadar modern tıbbın birçok alanını dönüştürme potansiyeline sahip.
İşte bu yüzden 2025 Nobel Fizyoloji veya Tıp Ödülü, yalnızca üç bilim insanına değil; insanlığın bağışıklık sistemini anlamasına atılmış en büyük adımlardan birine verilmiş oldu.






