4. Evre ALK Pozitif Akciğer Kanseri Tedavisi İçin Brigatinib FDA Onayı Aldı
28.04.2017 tarihinde FDA, metastatik (4. evre), ALK pozitif küçük hücre dışı akciğer kanseri tedavisinde brigatinibe (piyasa adı Alunbrig) hızlandırılmış onay verdi. Bu onay, anaplastik lenfoma kinaz (ALK) pozitif olan, krizotinib tedavisini altında hastalığı kötüye giden (progrese olan) veya krizotinibe yan etkileri nedeni ile devam edemeyen, 4. evre küçük hücre dışı akciğer kanserli hastalar için verilmiştir.
Brigatinib etki mekanizması nasıldır?
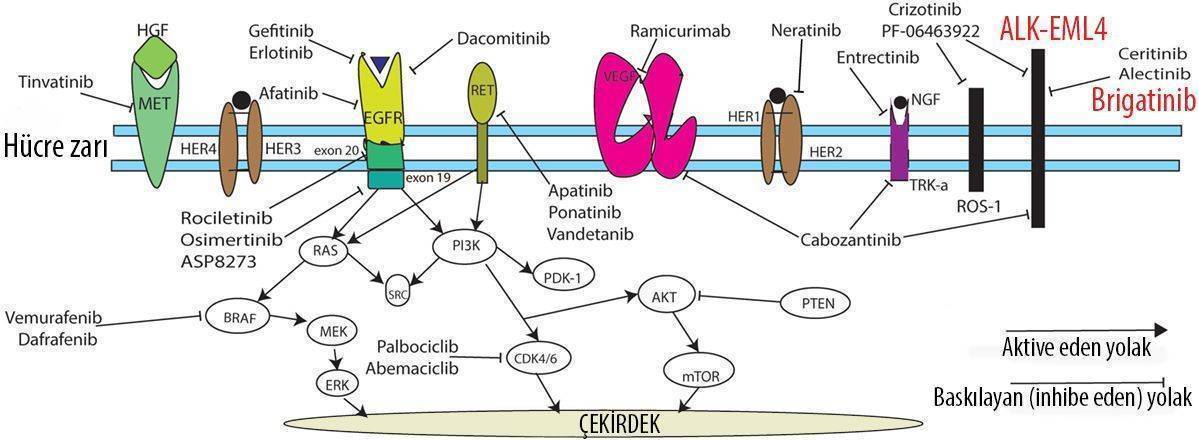
Kanser hücreleri geçirdikleri bazı değişimlerle, normal bir hücreye göre, çok daha hızlı çoğalma özelliğine kavuşur. Yeni geliştirilen ilaçların önemli bir kısmı bu değişiklikleri tanıma ve hedef alma özelliğine sahiptir. Bunlar akıllı veya hedefe yönelik ilaç olarak adlandırılır. Yukarıda karmaşık gözüken şekilde, kanserli hücreleri sahip olduğu hedeflerin ve bu hedeflere karşı geliştirilen ilaçların az bir kısmı şematize edilmiştir. Bunlardan biri de şeklin sağ tarafında görebileceğiniz ALK-EML4 reseptörü ve bu reseptörü hedef alan Brigatinib'tir.
Brigatinib, ALK (anaplastik lenfoma kinaz) baskılayıcı bir ilaçtır. ALK reseptörü, insanlarda ALK geni tarafından kodlanan büyüme ve çoğalmadan sorumlu bir reseptördür. ALK, EML4 ile füzyona uğradığında (birleşme), akciğer kanserini tetikleyebilir. Sigara içmeyenlerde görülen akciğer kanserinin nedenlerinden biri de bu durumdur. Brigatinib bu füzyona uğramış genin aktivitesi baskılar. EML4-ALK füzyon geni küçük hücre dışı akciğer kanserlerinin yaklaşık %5'inden sorumludur. Bu oran az gelebilir, fakat akciğer kanserinin dünya genelinde en sık görülen kanser olduğu düşünülürse, bu oran yılda 70 bin yeni akciğer kanserli hastaya karşılık gelmektedir.
Hızlandırılmış FDA onayı, bölgesel olarak ilerlemiş (lokal ileri) veya metastatik ALK-pozitif, krizotinib tedavisi altında progrese olan, klinik olarak anlamlı ve uzun süreli genel yanıt oranı gösteren küçük hücreli dışı akciğer kanserli hastalarda yapılan, karşılaştırmalı olmayan, iki kollu, açık etiketli, çok merkezli bir klinik çalışmaya dayandırılmaktadır (ALTA Çalışması). Çalışmadaki tüm hastalar, FDA onaylı bir testle ALK pozitifliği belgelenmiş tümörlere sahiptir.
Brigatinib kullanan hastalarda en sık görülen yan etkiler bulantı, ishal (diyare), yorgunluk, öksürük ve baş ağrısıdır. En sık görülen ciddi yan etki ise zatürredir (pnömoni).
Brigatinib'in önerilen doz rejimi, ilk 7 gün boyunca oral yolla günde bir kez 90 mg'dir, sonra tolere edildiği takdirde, günde bir kez oral yolla 180 mg'a yükseltilebilir.
fda-gov






