Evorpacept: HER2 Pozitif Mide ve Mide-Yemek Borusu Bileşke Kanserinde Yeni Tedavi
Mide ve gastroözofageal bileşke kanserlerinin yaklaşık %15-20'sinin HER2 pozitif olduğu bilinmektedir. Bu, HER2 pozitif tümörlerin, hücre yüzeyinde normalden fazla HER2 proteini ürettiği veya HER2 geninde mutasyonların bulunduğu anlamına gelir. Bu durum, tümörün daha hızlı büyümesi ve metastaz yapma eğilimi ile ilişkilendirilir. HER2 pozitiflik, bu hastalar için özel olarak tasarlanmış HER2 hedefli tedavilerden faydalanma imkânı sunar. Bu tedaviler, tümörün büyümesini engelleyerek yaşam süresini uzatabilir ve hastalık kontrolünü artırabilir. HER2 pozitifliğin saptanması, tedavi planlamasında kritik bir öneme sahiptir.
Yeni Bir Tedavi Seçeneği
HER2 pozitif mide ve mide-özofagus bileşke (MÖB) kanserlerinin tedavisinde, evorpacept adlı yenilikçi tasarıma sahip bir immünoterapi ilavesi ile geliştirilen yeni bir tedavi rejimi, mevcut tedaviye göre önemli ölçüede daha iyi sonuçlar sunuyor.
Yanıtın ortanca süresi evorpacept kolunda 15,7 ay, kontrol kolunda ise 9,1 ay olarak bulundu.
2025 ASCO Gastrointestinal Kanserler Sempozyumu'nda #ASCOGI25 sunulan araştırma bulgularına göre, CD47 hedefli bir tedavi olan evorpaceptin trastuzumab, ramucirumab ve paklitaksel (TRP) kombinasyonuna eklenmesiyle, hastaların yanıt oranları ve progresyonsuz sağkalım (PFS) süresi iyileşmiş görüldü.
Evorpacept Etki Mekanizması Nasıldır?
Evorpacept, kanser hücrelerinin yüzeyinde bulunan CD47 adlı proteini hedef alan bir immünoterapi ajanıdır. CD47, bağışıklık sisteminin fagositik hücreleri tarafından "beni yeme" sinyali olarak algılanır ve bu sinyal, kanser hücrelerinin bağışıklık sisteminden kaçmasına yardımcı olur. Evorpacept, CD47'yi bloke ederek bu sinyali engeller ve böylece bağışıklık sisteminin kanser hücrelerini tanımasını ve yok etmesini sağlar.
Onaylı Bir İlaç mı?
ABD merkezli biyoteknoloji şirketi ALX Oncology tarafından geliştirilen bir immüno-onkoloji ilacı olan evorpacept, çeşitli kanser türlerinin tedavisi için klinik araştırmalarda değerlendirilmektedir. Ancak, mevcut bilgilere göre henüz herhangi bir ülkede resmi onay almamıştır. Gelecekte, klinik deneylerden elde edilecek sonuçlara bağlı olarak onay alması mümkündür.
ASPEN-06 Çalışması: Tedavide Yeni Ufuklar
Faz 2/3 ASPEN-06 çalışması, daha önce birinci veya ikinci basamak tedavi gören ve anti-HER2 tedavisi sonrasında hastalığı ilerleyen HER2 pozitif mide/MÖB kanserli hastaları içeriyordu.
Araştırmada toplam 127 hasta rastgele iki gruba ayrıldı:
-
Evorpacept + TRP grubu (63 hasta)
-
Sadece TRP grubu (64 hasta).
Hastaların Genel Profili
-
Ortanca yaş: Evorpacept grubunda 64 (aralık, 34-81), kontrol grubunda 63 (aralık, 31-86).
-
Hastaların yaklaşık yarısı Asyalıydı (%49.2 ve %48.4).
-
Çoğu hasta mide kanseri tanısına sahipti (%76.2 ve %68.8).
-
Hastaların çoğu daha önce yalnızca bir basamak tedavi almıştı (%77.8 ve %68.8).
Tedavi Etkinliği: Daha Uzun Yanıt Süreleri
Evorpacept + TRP kombinasyonunun tedaviye verdiği yanıt oranları ve yanıt süreleri kontrol grubuna göre daha iyiydi:
-
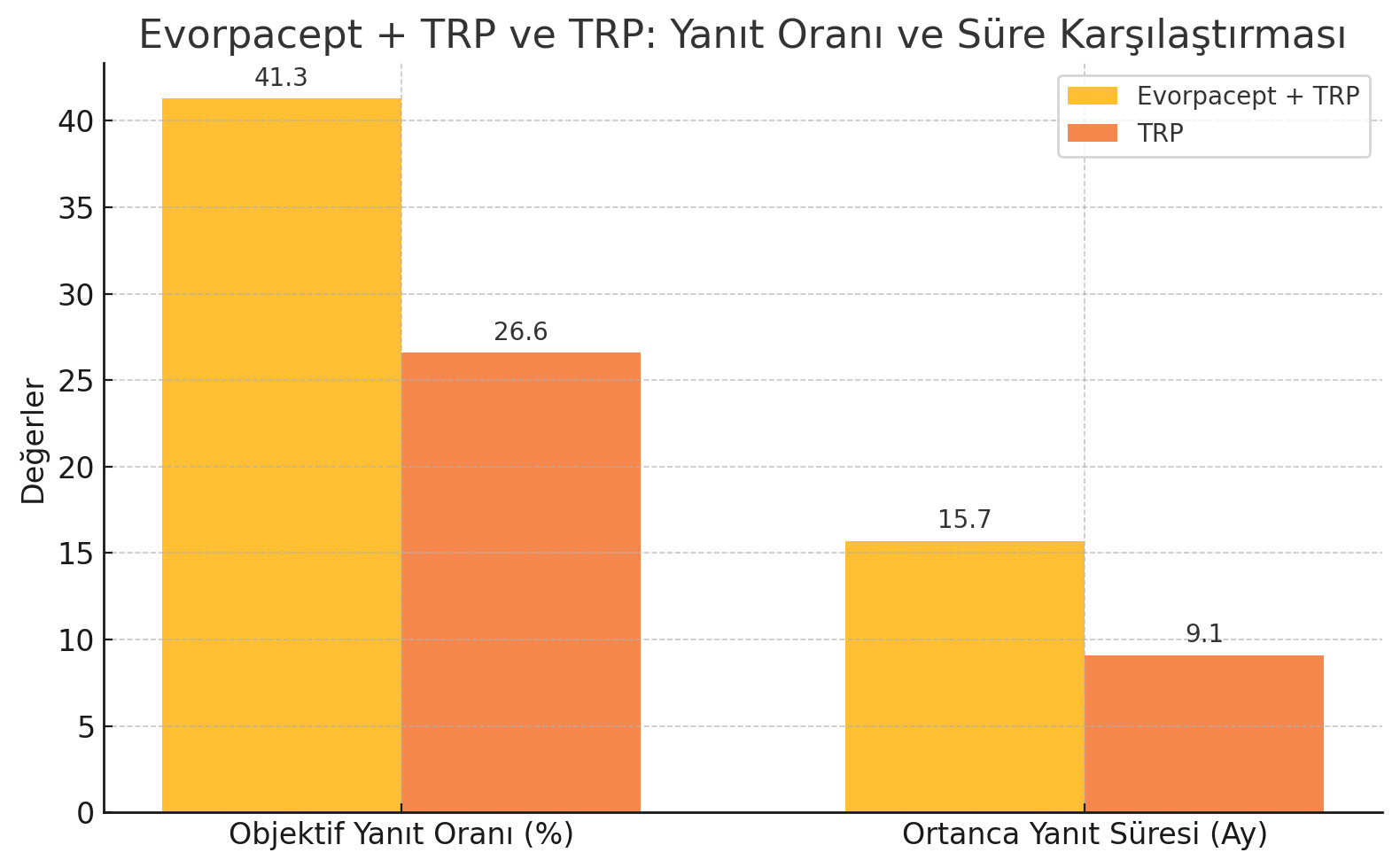
Objektif yanıt oranı: Evorpacept grubu %41.3, TRP grubu %26.6.
-
Her iki grupta da 1 tam yanıt saptandı.
-
Evorpacept grubunda 25 kısmi yanıt, kontrol grubunda ise 16 kısmi yanıt bildirildi.
-
-
Yanıt sürelerinin ortancası: Evorpacept grubu 15.7 ay, TRP grubu 9.1 ay.
Progresyonsuz Sağkalım (PFS): Ufak Bir Avantaj
-
Ortanca PFS: Evorpacept grubu 7.5 ay, TRP grubu 7.4 ay (HR, 0.77; %95 GA, 0.49-1.20).
HER2 Pozitiflik Doğrulaması ile Daha Güçlü Sonuçlar
HER2 pozitifliği taze biyopsi veya dolaşımdaki tümör DNA'sı (ctDNA) ile doğrulanan alt gruplarda tedavi etkinliği daha da belirgindi:
-
HER2 pozitif taze biyopsi alt grubu:
-
Objektif yanıt oranı: Evorpacept grubu %59.1, TRP grubu %23.1.
-
Ortanca yanıt süreleri: 15.7 ay ve 14.5 ay.
-
Ortanca PFS: 9.5 ay ve 7.1 ay (HR, 0.62; %95 GA, 0.28-1.36).
-
-
HER2 pozitif tüm alt grup:
-
Objektif yanıt oranı: Evorpacept grubu %48.9, TRP grubu %24.5.
-
Ortanca yanıt süreleri: 15.7 ay ve 9.1 ay.
-
Ortanca PFS: 7.5 ay ve 6.7 ay (HR, 0.64; %95 GA, 0.39-1.07).
-
Yan Etkiler ve Güvenlik
Evorpacept grubundaki yan etkiler kontrol grubuyla benzerdi ve kabul edilebilir bir güvenlik profili sundu.
-
En yaygın ciddi (Grade 3) yan etkiler:
-
Nötrofil düzeyi düşüklüğü: Her iki grupta %19.
-
Anemi: Evorpacept grubu %22.2, kontrol grubu %17.5.
-
Diğer yaygın etkiler: Beyaz kan hücresi düzeyi düşüklüğü, hipertansiyon, halsizlik ve febril nötropeni.
-
-
Grade 4 yan etkiler: Nötropeni (%6.3 ve %3.2).
Tedaviye Bağlı Yaşam Kaybı Oranları
-
Çalışma boyunca 11 hasta yaşamını kaybetti ve bunların 2'sinin tedavi ilişkili olduğu düşünüldü.
-
Evorpacept grubunda bir hasta yemek borusu perforasyonu nedeniyle, TRP grubunda bir hasta ise pnömopati nedeniyle öldü.
Yorum
Bu bulgular, evorpaceptin kabul edilebilir güvenlik profili ile birlikte mide/MÖB kanseri hastaları için umut vadeden bir tedavi seçeneği olduğunu göstermektedir. Bu sonuçlar, daha ileri çalışmaları desteklemektedir.
Elde edilen veriler, CD47'yi hedefleyerek yeni bir immünoterapi yaklaşımı sunan evorpaceptin HER2 pozitif mide ve MÖB kanserinde standart tedaviye eklenmesiyle daha iyi yanıt oranları ve daha uzun yanıt süreleri sağlanabileceğini gösteriyor. Bu, hastaların yaşam kalitesini ve sağkalımlarını iyileştirebilecek önemli bir gelişme olarak dikkat çekiyor.
Shitara K, Wainberg Z, Tabernero J, et al. Final analysis of the randomized phase 2 part of the ASPEN-06 study: A phase 2/3 study of evorpacept (ALX148), a CD47 myeloid checkpoint inhibitor, in patients with HER2-overexpressing gastric/gastroesophageal cancer (GC). Presented at ASCO GI 2025. January 23-24, 2025. San Francisco, CA. Abstract 332.