
Ramucirumab (Cyramza) Nedir? FDA Onayı, Türkiye Ruhsatı ve Geri Ödeme Durumu
- FDA Onaylı: Evet (İlk onay tarihi: 2014)
- Kutu Adı: Cyramza
- Etken Madde Adı: Ramucirumab
- Uygulama Şekli: İntravenöz (IV) infüzyon
- Sınıfı: Monoklonal antikor, Anti-VEGFR antikoru
- Kategori: Hedeflenmiş ajan, Anti-anjiyogenez ajanı
- Üretici: Eli Lilly
- Türkiye Dağıtımı: Yok. Yurtdışı teminli ilaç
- Onaylı Olduğu Kanserler:
- İleri evre metastatik kolorektal kanser (FOLFIRI ile kombine)
- Metastatik gastrik veya gastroözofageal bileşke adenokarsinomu
- Metastatik küçük hücreli dışı akciğer kanseri (KHDAK, EGFR mutasyonu pozitif)
- Hepatoselüler karsinom (HCC)
Ramucirumab Nedir? Etki Mekanizması Nasıldır?
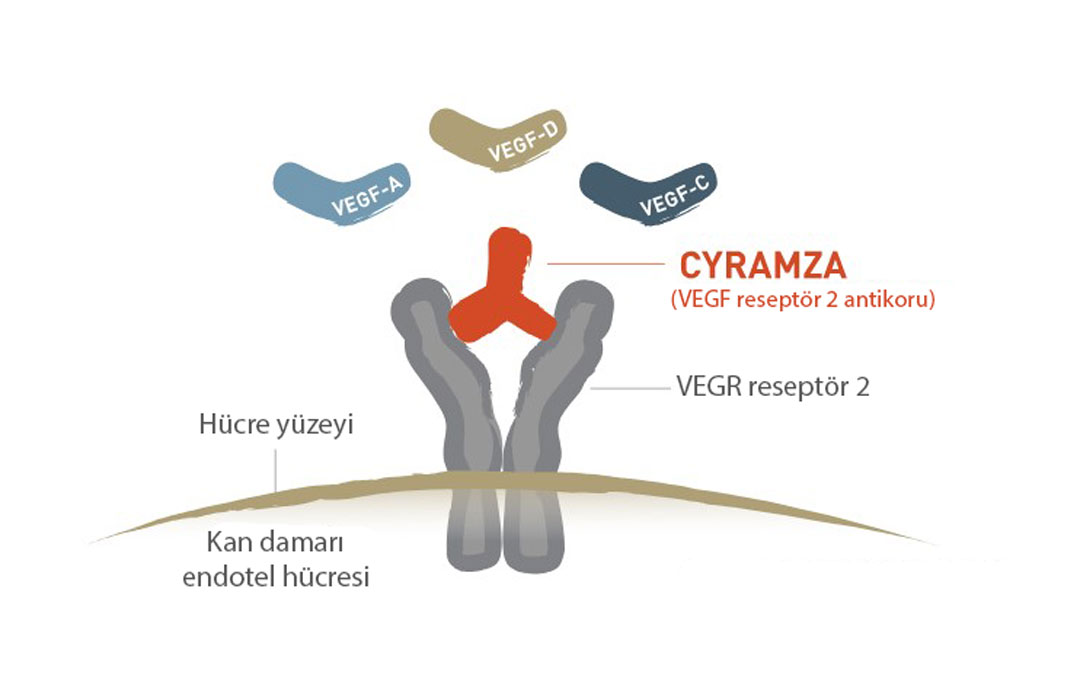
Ramucirumab, VEGFR-2’ye (Vasküler Endotelyal Büyüme Faktörü Reseptörü 2) bağlanan tamamen insan kaynaklı bir IgG1 monoklonal antikordur. VEGF-A, VEGF-C ve VEGF-D ligandlarının bu reseptöre bağlanmasını engelleyerek tümör anjiyogeneziyi (yeni damar oluşumunu) baskılar. Bu, tümör hücrelerinin kan damarlarını oluşturma yeteneğini sınırlandırarak hem primer hem de metastatik tümörlerde yeni kan damarı oluşumunu baskılar. Ayrıca tümör kan damarı geçirgenliğini azaltarak tümör içi basıncı düşürür ve tümör içi kan akışını artırabilir.
FDA (ABD Gıda ve İlaç İdaresi) Onay Tarihçesi:
- 21 Nisan 2014: FDA, Cyramza’yı mide kanseri tedavisi için onayladı.
- 5 Kasım 2014: FDA, Cyramza’yı önceki kemoterapi sonrası ileri evre mide kanseri için paklitaksel ile kombine kullanımını onayladı.
- 12 Aralık 2014: FDA, Cyramza’nın agresif küçük hücreli dışı akciğer kanseri (NSCLC) tedavisinde kullanımını onayladı.
- 24 Nisan 2015: FDA, Cyramza’yı FOLFIRI ile birlikte metastatik kolorektal kanserin ikinci basamak tedavisi için onayladı.
- 13 Mayıs 2019: FDA, Cyramza’yı hepatoselüler karsinom (HCC) tedavisinde ilk FDA onaylı biyomarköre dayalı tedavi olarak onayladı.
- 29 Mayıs 2020: FDA, Cyramza’yı metastatik EGFR-mutasyonlu küçük hücreli dışı akciğer kanseri için birinci basamak tedavi olarak onayladı.
Türkiye Ruhsatı:
Ramucirumab etken maddeli Cyramza, T.C. Sağlık Bakanlığı tarafından ruhsatlandırılmıştır.
Kullanılması gereken durumlarda, Bakanlığa Endikasyon Dışı Onay başvurusu yapılması gerekmektedir. Onay alınması durumunda, ilaç Türk Eczacıları Birliği (TEB) aracılığıyla temin yoluna gidilebilir.
Geri Ödemesi Var mı?
Ülkemizde Sosyal Güvenlik Kurumu (SGK) geri ödeme kapsamında değerlendirilmemektedir.
Fiyatı: Ağustos 2025 itibarı ile Cyramza 100 mg 2x10 ml flk 28.265.24 TL dir.
Direnç Mekanizması:
Ramucirumaba karşı direnç mekanizmaları şunlardır:
- Pro-anjiyogenik faktörlerin (örn. bFGF, HGF) artan aktivasyonu ve/veya regülasyonu.
- Kemik iliğinden türeyen hücrelerin tümör mikroçevresine göçü, bu durum VEGF sinyalini atlayarak yeni damar oluşumunu ve anjiyogenezi yeniden başlatır.
Emilim:
Ramucirumabın emilimi net olarak karakterize edilmemiştir.
Dağılım:
Ramucirumabın vücutta dağılımı tam olarak karakterize edilmemiştir. Durağan hale gelme süresi yaklaşık 28 gündür.
Metabolizma:
Ramucirumabın metabolizması kapsamlı bir şekilde karakterize edilmemiştir. Ortalama ilaç klerensi mide kanseri, KHDAK ve metastatik kolorektal kanser (mKRK) hastaları için benzerdir ve ortalama yarılanma ömrü yaklaşık 15 gündür.
Doz Aralığı:
- Metastatik kolorektal kanser: Tavsiye edilen doz 8 mg/kg IV her 2 haftada bir FOLFIRI ile birlikte.
- İleri evre mide veya gastroözofageal bileşke adenokarsinomu: Tavsiye edilen doz 8 mg/kg IV her 2 haftada bir.
- Küçük hücreli dışı akciğer kanseri (KHDAK): Tavsiye edilen doz 10 mg/kg IV her 3 haftada bir doksetaksel ile kombine.
- EGFR mutasyonu pozitif KHDAK: Tavsiye edilen doz 10 mg/kg IV her 2 haftada bir erlotinib ile kombine.
- Hepatoselüler karsinom (HCC, karaciğer kanseri): Tavsiye edilen doz 8 mg/kg IV her 2 haftada bir.
İlaç Etkileşimleri:
Henüz iyi karakterize edilmemiştir.
Dikkat Edilmesi Gereken Durumlar:
- Ciddi, bazen yaşam kaybına neden olabilecek arteriyel tromboembolik olaylar (miyokard enfarktüsü, inme, serebral iskemia) oluşabilir. Bu tür olaylar yaşanırsa tedavi kalıcı olarak kesilmelidir.
- Ramucirumab tedavisi sırasında hemorajik olayların (şiddetli kanamalar dahil) riski artar. Özellikle NSAİİ'ler ile tedavi edilen gastrik kanser hastalarında dikkatli olunmalıdır. Bu hastalarda NSAİİ kullanımı dışlanmıştır, bu nedenle risk tam olarak bilinmemektedir.
- Ramucirumab hipertansiyon riskini artırır. Özellikle tedavi sürecinde kan basıncı yakından izlenmeli ve kontrol altına alınmalıdır.
- İnfüzyonla ilişkili semptomlar sıkça görülebilir (ateş, titreme, baş ağrısı, yorgunluk gibi). Bu belirtiler oluştuğunda parasetamol veya diphenhidramin gibi ilaçlar kullanılabilir.
- Gastrointestinal perforasyon (mide-bağırsak sisteminde delinme) gelişebilir ve böyle bir durum oluşursa tedavi derhal kesilmelidir.
- VEGF sinyal yolunun inhibisyonu yara iyileşmesini olumsuz etkileyebilir. Yara iyileşmesi tam olarak sağlanmadan tedavi yeniden başlatılmamalıdır.
- Karaciğer yetmezliği bulunan hastalarda klinik kötüleşme gözlenebilir. Child-Pugh B ve C sınıfı siroz hastalarında dikkatli olunmalıdır.
- Böbrek hastalarında dikkatli kullanılmalıdır. Proteinüri ve nefrotik sendrom vakaları rapor edilmiştir. Eğer idrar protein düzeyleri belirli seviyeleri aşarsa tedavi kesilmelidir.
- Tiroid fonksiyonları düzenli olarak izlenmelidir.
- Hafif ve orta dereceli böbrek yetmezliğinde doz ayarlaması gerekmez.
- Hafif ve orta dereceli karaciğer yetmezliğinde doz ayarlaması gerekmez. Ancak şiddetli karaciğer yetmezliği olan hastalarda dikkatli olunmalı ve toksisite artışı göz önünde bulundurulmalıdır.
- Hamilelik kategorisi B'dir.
Yan Etkiler:
En sık olandan en seyrek olana göre yan etkiler şunlardır:
- Hipertansiyon (%20-30 arası), %8-15 arasında derecesi daha ağır hipertansiyon görülebilir.
- Kanama komplikasyonları (epistaksis, gastrointestinal kanama, şiddetli kanamalar dahil).
- Yorgunluk ve baş ağrısı.
- Bulantı, kusma, iştahsızlık, karın ağrısı, ishal.
- Gastrointestinal perforasyonlar ve yara iyileşmesi komplikasyonları.
- Nefrotik sendrom ile birlikte proteinüri.
- İnfüzyon ilişkili semptomlar (ateş, titreme, kızarıklık, baş ağrısı).
- Arteriyel ve venöz tromboembolik olaylar (miyokard enfarktüsü, inme).
- Hipotiroidizm.
- RPLS (geri dönüşlü posterior lökoensefalopati sendromu): Nadir görülür (%0,1'den az) ve baş ağrısı, nöbet, bilinç değişikliği gibi semptomlarla ortaya çıkar.
Chu, Edward; DeVita Jr., Vincent T.. Physicians' Cancer Chemotherapy Drug Manual 2024.






