
İnsan moleküler genetiği ve genomiği – Önemli gelişmeler ve heyecan verici olasılıklar
Geçtiğimiz 50 yılda meydana gelen moleküler genetikteki nefes keseci gelişimleri ve genomik tıbba geçişi, 1970’lerde hayal etmek zor olurdu. Genomik terimi henüz türetilmemişti, modern biyoteknolojinin temeli olan araçlar ve teknolojiler henüz başlangıçtaydı ve hatta birkaç nükleotidin sekanslanma (dizileme) metodu da nadiren uygulanabilmekteydi (genetik kodumuzun detaylı haritasının çıkarılması).
Tahmin edilemeyecek gelişmeler
Genomik tıbbın ilk adımları, Boyer ve Cohen’nin rekombinant metodu, Sanger’in DNA-sekanslama çalışması ve Mulli’nin polimeraz zincir reaksiyonu (PCR) teknolojisi gibi DNA ile ilişkili paradigma değiştiren keşiflerdi. Yine bu temele karşı bile, insan genomunu sekanslama çabası için “büyük bilim” kavramı radikal gözüküyordu.
1987’de New York Times dergisinde İnsan Genom Projesi, tarihteki en büyük, en maliyetli, en provokatif biyomedikal araştırma projesi olarak nitelendirildi. Fakat projenin başlatıldığı yıl 1990 ile tamamlandığı yıl 2003 yılları arasında, genomik teknoloji çarpıcı bir şekilde gelişti.
DNA sekanslama miktarı günlük 1000 baz çiftinden saniyede 1000 baz çiftinden daha fazla bir sayıya çıktı, ki bu rutin tıbbi tedaviye dahil edilecek genomik gelişmelere olanak sağlayan düşük maliyetli sekanslama tekniklerinin kapısını açtı. Genomik araştırma, insan genetik kodunun temelini anlama arayışından, insanlar arasında farklılık gösteren bu kodun yollarını açıklamak ve daha sonra bu bilgileri hastalıkların altında yatan sebepleri hassasiyet ile hedeflemek için uygun hale getirilen müdahalelere uygulamaya kadar geniş bir yelpazeye dağıldı.
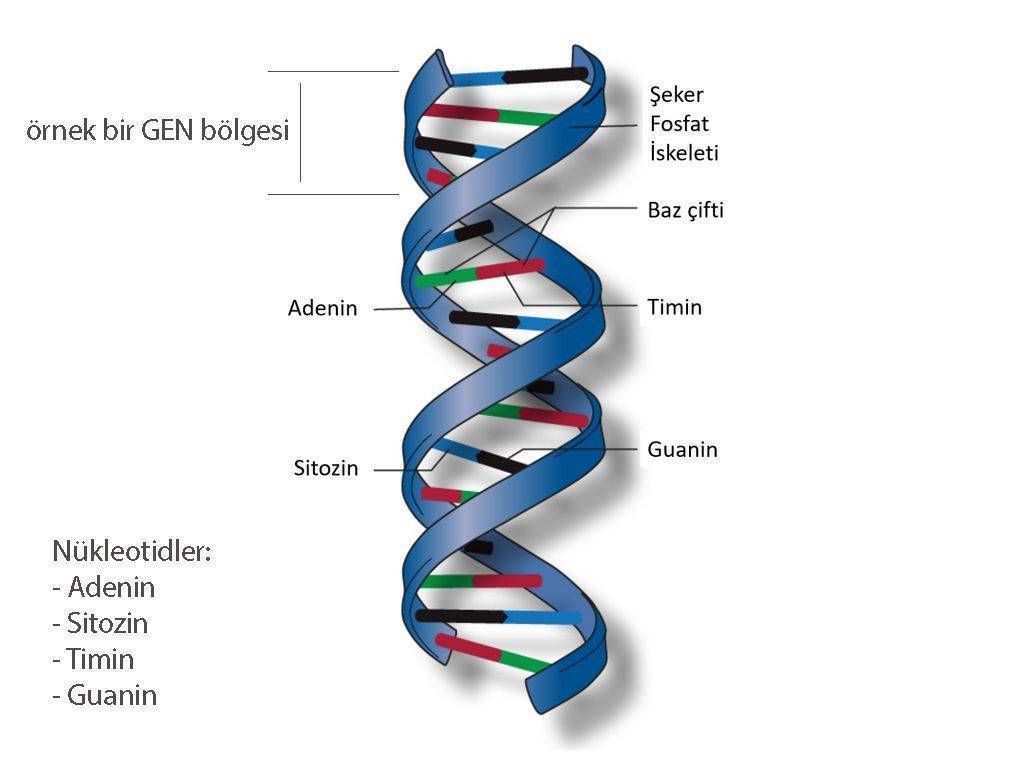
DNA merdiven şekline benzeyen yapısıyla birlikte, çift sarmallı, 4 çeşit nükleotitten (Adenin, Timin, Sitozin ve Guanin) oluşmaktadır. Bu haliyle genetik kodumuz olan DNA, 4 harfli bir dil gibi düşünülebilir. DNA, hücrelere ne yapmaları gerektiğinin talimatlarını verir. İnsan DNA’sı 3 milyar nükleotid çiftinden oluşur ve DNA sarmalının %2 kadarı hücrelerin temel yapıtaşı olan proteinlerin üretiminden sorumludur; DNA’nın bu anlamlı bölümlerine gen denir. DNA’mızda yaklaşık 20 bin gen bulunur ve tüm genlerim birleşimine genom denir.
Genomik gelişmeler tıbbın doğasını değiştirdi
Genomik araçların ve veri setlerinin gelişimi, bilim insanlarına, aday yollara odaklanılan hipotezleri test etmekle sınırlı kalmaktansa, kapsamlı ve güçlü keşiflere adım atmak için olanak sağlayarak tıbbi keşfin doğasını değiştirdi. İnsan genomunun sekanslanmasının ilk kaynağının tamamlanması ile dikkatler genlerin araştırılmasından genlerin fonksiyonlarını keşfetmeye döndü. Ailelerde ve toplumlarda sistematik genetik haritalama bilim insanlarına, insan hastalıklarına yol açan genetik değişikliklerin tam yerini saptamaları konusunda yardımcı oldu. İnsan Genom Projesi’nin sonucu olarak 2000 sonrası tıp adeta yeniden yazıldı.
Etkiler çok derindir. Ender mendeliyen (bir çeşit kalıtsal durum) hastalıklardan sorumlu 5000’den fazla genin keşfi çoğu hasta, hamilelik ile ilişkili danışmanlık, yeni ilaç tedavileri ve bazı durumlarda gen terapiler için genetik tanıyı kolaylaştırmaktadır.
Genomik bölgeler ve yaygın hastalıklar arasındaki 100,000’den fazla güçlü ilişkinin keşfi, Alzheimer hastalığındaki mikroglianın, iltihabi bağırsak hastalığında otofajinin, şizofrenide sinaptik budamanın rolü gibi yeni biyolojik mekanizmaları gösterdi. Ayrıca klinik sonuçların değerlendirilmesini içeren bu tür hastalıkların ek titiz testlerine ihtiyaç duyulmasına rağmen, kalp-damar hastalığı, meme kanseri ve diğer durumlar için yüksek risk altındaki hastaları belirlemek adına poligenetik risk skorlarının geliştirilmesine de olanak sağlamıştır.
Kanser genom çalışmaları tümör başlaması ve büyümesini teşvik eden somatik (kalıtsal olmayan) mutasyonlardaki yüzlerce geni açığa çıkardı, ki bu bilgi yeni ilaçların geliştirilmesini ateşledi (bunlara onkolojide genetik hedeflere yönelik akıllı ilaçlar diyoruz).
Kanserde genomik analizler (genetik testler) ayrıca, neden bazıları yapamazken bazı kişilerin belli tedavilere yanıt verdiğini ya da belli enfeksiyonlara karşı hayatta kaldığını açıklamaya yardımcı oluyor.
İnsan moleküler genetik ve genomiğinde önemli noktalar – Kısaca tarihi
Kısaltmalar: Cas9: CRISPR ilişkili protein 9 / CRISPR: Düzenli aralıklar ile bölünmüş palindromik tekrar kümeleri / İGP: İnsan Genom Projesi / NIH: ABD Ulusal Sağlık Enstitüsü
- 1973 – Herbert Boyer ve Stanley Cohen rekombinant DNA teknolojisini geliştirdi.
- 1977 – Walter Gilbert ve Fredick Sanger DNA sekanslama için teknikler keşfetti.
- 1983 – Kary Mullis polimeraz zincir reaksiyonu (PCR) uygulamasını icat etti.
Hastalıkla ilişkili ilk gen James Gusella ve Nancy Wexler tarafından moleküler olarak bir insan kromozomuna eşlenir. - 1986 – Leroy Hood otomatikleştirilmiş DNA sekanslayıcı icat etti.
- 1990 – NIH ve Enerji Bölümü, İnsan Genom Projesi’ni (İGP) başlatır.
- 1994 – İGP’nin insan genetiğinin haritalanması hedeflerine ulaşıldı.
- 1995 – İGP’nin insan genetiğinin haritalanması hedeflerine ulaşıldı.
- 1996 – İGP insan genomunun geniş ölçekte sekanslanması için stratejileri test etmeye başlar.
- 1997 – “Bermuda İlkeleri” olarak adlandırılacak olan şeyde, İGP araştırmacıları kullanım kısıtlaması olmadan genom dizisi verilerinin hızlı, halka açık yayınlanmasını onayladı.
- 2001 – İGP uluslararası konsorsiyumu insan genom sekansının ilk taslağını yayımlar; J. Craig Venter’ın Celera Genomik Derneğindeki grubu sekansın başka bir versiyonunu yayımlar.
- 2002 – Uluslararası HapMap Projesi yaygın hastalıklar ile ilişkili genlerin tanımlanmasını hızlandırmak için kullanılabilecek insan genetik varyasyonları üzerine veri toplamak için başlatılır.
- 2003 – İGP, insan genomunun bir referans sekansını üreterek planlanandan iki yıl önce tamamlanır.
- 2006 – NIH, 33 kanser tipini kapsayan 20,000 örnekten daha fazlasını moleküler olarak karakterize etmek için Kanser Genom Atlas’ını (TCGA) başlatır.
- 2008 – Sağlık sigortası ve istihdamda genetik bilginin ayrıcalık yapan kullanımına karşı koruma için ABD Genetik Bilgi Ayrımı Yapmama Hareketi yasallaştırılır.
- 2009 – Klinik bir ilk olarak, Wisconsin araştırmacıları 5 yaşındaki bir erkek çocuğun genlerinin hepsini sekanslar ve yeni bir hastalığın tam yerini saptamak için verileri kullanır, ki bu da hayat kurtarıcı tedaviye yol açar.
- 2012 – Afrika’da İnsan Kalıtımı ve Sağlığı (H3Afrika) konsorsiyumu açılış toplantısını Addis Ababa, Etiyopya’da gerçekleştirir.
- Emanuella Charpentier ve Jennifer Doudna CRISPR’ın DNA’yı in vitro düzenleyebildğini gösterir (bu onlara 2020 Kimya dalında Nobel Barış Ödülünü kazandırır); yaklaşık 6 ay sonra Feng Zhang ve George Church memeli hücrelerinde CRISPR düzenlemesini bağımsız olarak kanıtlar.
- 2018 – TCGA, tüm veri setine dayalı çapraz-kanser analizlerinin bir koleksiyonu olan Pan-Kanser Atlas’ını yayımlar.
NIH, genetik, sağlık ve çevresel verilere katkı sağlayacak 1 milyondan fazla katılımcıdan oluşan geniş ölçekli bir araştırma kaynağı olan araştırma programı “Hepimiz (All of Us)” için kayıta başlar. - 2020 – Orak hücre anemi hastalığına sahip ilk hasta CRISPR – Cas9 kullanılarak ex vivo yaklaşım ile tedavi edilir.
Araştırmacılar gen ifadesine odaklandı
Son dönemlerde genetik araştırmanın odağı, DNA varyasyonlarının (farklılıklarının) analiz edilmesinin ötesine, tek hücreli RNA sekanslama ve kromatin analiz için yeni metotlar tarafından yürütülen bir adım olan tek tek hücrelerde gen ifade modelini çalışmak oldu. İnsan vücudunun tam bir hücre atlası yolunda şimdiye kadar on milyonlarca hücre karakterize edildi. Bu çaba yüzlerce yeni hücre tiplerini ortaya çıkarıyor ve çeşitli hastalıklara sahip kişiler ile sağlıklı kişiler arasındaki hücre tiplerinin farklılaşma yollarının karakterize ediyor.
İnsan Genom Projesi sırasında 3 milyar dolar olan ve bugün 600 dolara düşmüş olan tam bir genom sekanslama maliyeti ile geniş ölçekli tam genom sekanslama biyobankaları ve yüz binlerce insandan elde edilen fenotip bilgiler yaratmak için artan çabalar vardır. Örnekler, Birleşik Krallık Biyobankası’nı ve ABD “Hepimiz (All of Us)” araştırma programını içerir. Son hedef, tıbbi kayıtlar ile genomik bilgileri birleştirmek için sağlık bakım sistemleridir.
- İlgili Konu: Tüm ekzom sekanslama genom dizi analizi nedir?
Daha çok yolumuz var
İnsan genetik farklılıklarını ve hastalıkların genetik temellerini anlamak için daha yapılacak epey çalışma var.
Çeşitli hastalık geçmişlerine sahip insanlar üzerinde çalışarak sunulan biyoloji ve sağlık farklılıkların iç yüzünü kavrama sözüne rağmen hem araştırmacılar hem de genomik araştırmaya dahil olan katılımcılar büyük ölçüde Avrupa soyundandır. Bu çeşitlilik eksikliği kendi biyolojimizi anlamamızı engeller, halihazırda kabul edilemez sağlık farklılıklarını kötüleştirir ve genomik araştırmalardan elde edilen poligenetik risk skorlarının, tanıların ve ilaçların tüm toplumlara eşit derecede yarar sağlayacak olup olmadığı sorusunu doğurur.
Farklı ailesel geçmişe sahip insanlar üzerine olan çalışmalar şunları ortaya çıkardı:
- genomik varyasyonlar hastalıklara yakalanma riski,
- ilaç yanıtları ve
- genomik araştırma tarafından yol gösterilen klinik yaklaşımların tanısal doğruluğundaki toplum seviye farklılıklarını
Örnekler
Afrika uyku hastalığına karşı koruyan ancak böbrek yetmezliği riskini artıran Afrika kökenine özgü APOL1 varyantı: bu varyantlar Birleşik Devletlerdeki Afrika kökenli insanlarda diyabetik olmayan böbrek yetmezliği vakalarının yaklaşık %70’ini oluşturur.
Yerli Amerikalıların yaklaşık yarısında var olan ve Avrupa veya Afrika kökenli insanlarda nadir görülen SLC16A11'deki tip 2 diyabet için bir risk haplotipi, Avrupalı Amerikalılar ile karşılaştırıldığında Meksikalı Amerikalılar arasında artan tip 2 diyabet sıklığının yaklaşık %20’sini açıklar.
Genomik araştırmalar ayrıca PCSK9 işlev kaybı mutasyonlarının Afrika kökenlilerde diğer toplumlardan daha yaygın olduğunu göstermektedir; bu tür mutasyonlar kolesterol seviyelerini ve kalp hastalıkları riskini azaltır.
Daha önce yeterince temsil edilmeyen toplumlardan araştırmacıların ve çalışma katılımcılarının katılımını artırmak için tasarlanan birkaç girişimler devam etmekte. Afrika’daki İnsan Kalıtım ve Sağlık girişimi, örneğin, 500’den fazla Afrikalı bilim insanı için genomik teknolojilere erişime olanak sağlayan pan-Afrika laboratuvarlar konsorsiyumunu geliştirdi; 60.000’den fazla araştırmacı katılımcı kaydedildi ve bir biyoinformatik ağı ve üç bölgesel biyorepositori kurdu.
Hedef: Gen-düzenleme teknolojileri
Genetik hastalıkların tanısı, genomik sekanslama teknolojisi sayesinde artık çok daha hızlı bir şekilde konulmakta. Fakat tedavileri geliştirmek ve geçerli kılmak daha zor olmaktadır. Bazı mendeliyen bozukluklar için moleküler hedeflenmiş ilaçlar patolojinin ayrıntılı anlaşılmasının kullanımı ile geliştirilmiştir. CFTR geninin 1989 keşfine dayanan çalışma sayesinde, örneğin, güvenli ve etkili moleküler hedeflenmiş ilaçlar, kistik fibrozlu kişilerin %90’ına önerilebilir. Fakat bu yaklaşım on yıllar alabilir ve kesin moleküler sebebi bilinmediği için genetik bozuklukların binlercesini daha iyi ölçeklendirmez.
Doğrudan geni hedefleyen etkili tedaviye olanak sağlayan bir strateji, önemli gelişmelere sahip olabilirdi. İnişli çıkışlı yıllardan sonra spinal musküler atrofi ve hemofili gibi gen terapisinin bazı önemli başarıları doğuyor. Bu araştırmanın temposu gelecekte önemli derecede artabilir; kesin olarak hedeflenmiş gen-düzenleme teknolojileri şu anda terapötiklere yeni yollar sağlıyor.
2020 Nobel Kimya Ödülü
Geçtiğimiz 8 yılı aşkın süredir CRISPR – Cas9 (düzenli aralıklar ile bölünmüş palindromik tekrar kümeleri – CRISPR-ilişkili protein 9) teknolojileri genomlar üzerine çalışmak ve değiştirmek için uyarlanabilir ve erişilebilir araçlar olarak doğdu. CRISPR – Cas9 bölgeye özgü DNA onarımını tetikleyen hedeflenmiş DNA parçaları yaratarak genomu düzenlemek için kullanılabilir. Gelecek nesil formatlarında, ayrıca genlerin transkripsiyonel çıktılarını kontrol edebilir ya da DNA parçalarının onarımını gerektirmeyen bir nükleotid baz düzenleme işlemini kullanarak genom sekanlarını değiştirebilir. Bu teknolojiler olgunlaşmaya devam ettikçe hücresel genomları etkili ve doğru bir şekilde değiştirmek git gide mümkün olacak.
CRISPR teknolojisi hem şimdiye kadar getirdikleri hem de geleceği değiştirme potansiyeli ile 2020 Nobel Kimya Ödülü'ne layık görüldü.
Tasarlanmış nükleazların hemen arkasından gelen CRISPR – Cas9 araçları, hücreler veya model organizmalardaki neredeyse her bir genin yüksek derecede etkili düzenlenmesi veya nakavt edilmesine izin vererek genomik araştırmanın temposunu hızlandırmaktadır. Çoklu CRISPR – Cas9 tabanlı klinik deneyler devam etmektedir ya da yakında başlaması beklenmektedir. Cas9-tasarımlı hücreler henüz ölçekteki etkinliğini kanıtlamamış olmasına rağmen erken deney sonuçları bu tür hücrelerin sabit olduğu ve insanda ani gelişen olumsuz reaksiyonlara sebep olmadığını göstermiştir. Uzun vadeli güvenlik henüz belirlenmedi. Mevcut uygulamalar orak hücre anemisi durumunda kemik iliği hematopoietik kök hücreler gibi gen düzenlemelerin uygun hücreler üzerinde ex vivo yürütülmesi için büyük ölçüde tek-gen bozukluklarına odaklanmaktadır. Keşifler, gen düzenleme aracını uygun dokuya in vivo hedefleyebilen teslimat sistemleri geliştirme yolundadır.
Sonuç
Genomik teknoloji gelişmeleri temel bilimi güçlü yollara doğru ilerletmeye devam edecektir, hepsi öngörülemeyebilir. Bundan 10 yıl önce genomlar, transkriptomlar ve kromatin işaretleri üzerindeki büyük miktarlardaki verilere anında ve ücretsiz erişimi hayal bile edemezken, önümüzdeki 5-10 yıl içinde bu mümkün olacak – ve git gide bu veriler tek hücreler için mevcut hale gelecek. Bu tür veri setlerine tüm biyologların, genetikçilerin ve biyoinformatikçilerin hazırlıklı olması gerekecek. Bu çapta genomik veri, çok karmaşık hesaplamalı analiz gerektiren biyolojik kavrayış için fırsatlar sağlayacaktır.
Ancak tüm büyük sorular yalnız bilim tarafından cevaplanamayabilir. Örneğin, klinik araştırma fırsatlarına ve genomik devrim ile yaratılan tedavilerin yararlarına adil ve kapsamlı erişimi nasıl sağlayabiliriz? Kalıtsal genetik değişikliklerin genom düzenleme teknolojileriyle tedavisinin doğurabileceği etik sorunlar ile bilimsel ilerlemeyi nasıl dengeleriz? Kültürel normlara saygı duyma ve katılımcıların mahremiyetini korurken aynı zamanda genom bilimini ateşleyen veri paylaşımı inancını nasıl sürdürürüz? Bu tür soruların tatmin edici cevapları için önümüzde bir 50 yıla ihtiyaç olabilir.
Francis S. Collins et al. (2021, Jan 7). Human Molecular Genetics and Genomics — Important Advances and Exciting Possibilities.






