
Yeni Bir Kanser Aşısı, İleri Evre Akciğer Kanseri için Umut Veriyor
Aşı ile kanseri tedavi etme çabalarının yaklaşık 130 yıllık bir tarihi vardır. Bu amaçla ilk kullanılan ajanlar bakterilerdi (bakınız Coley toksinleri). Fakat tedavi edici kanser aşıları için tutarlı, anlamlı ve öngörülebilir yanıtlar 2010'lu yıllara kadar elde edilemedi. Bununla birlikte çok az sayıda kanser için tedavi edici kanser aşıları FDA onayı alabildi (melanom için Lmlygic ve prostat kanseri için Provenge).
Şimdiye kadar denenen kanser aşılarının amaçları ortaktır: bağışıklık sistemini kansere karşı tetiklemek. Bu haliyle kanser aşıları, bir çeşit immünoterapidir. Bu amaçla yeni geliştirilen bir kanser aşısının erken aşama insan deneyi sonuçları, Journal of Clinical Oncology adlı önde gelen onkoloji dergisinde 7 Eylül 2022'de yayımlandı.
İlgili konu: İmmunoterapi ve Kanser Aşısı Çeşitleri
Adotevi ve arkadaşları tarafından bildirilen Fransız faz Ib/IIa çalışmasında, tedavi edici peptid-bazlı kanser aşısının (UCPVax), dirençli ileri evre küçük hücreli dışı akciğer kanserli birçok hastada spesifik CD4+ T helper-1 yanıtlarını tetiklediği ve aşıya yanıt veren hastaların tedaviden fayda sağladığı gösterildi.
Peptid-bazlı Kanser Aşısı Nedir?
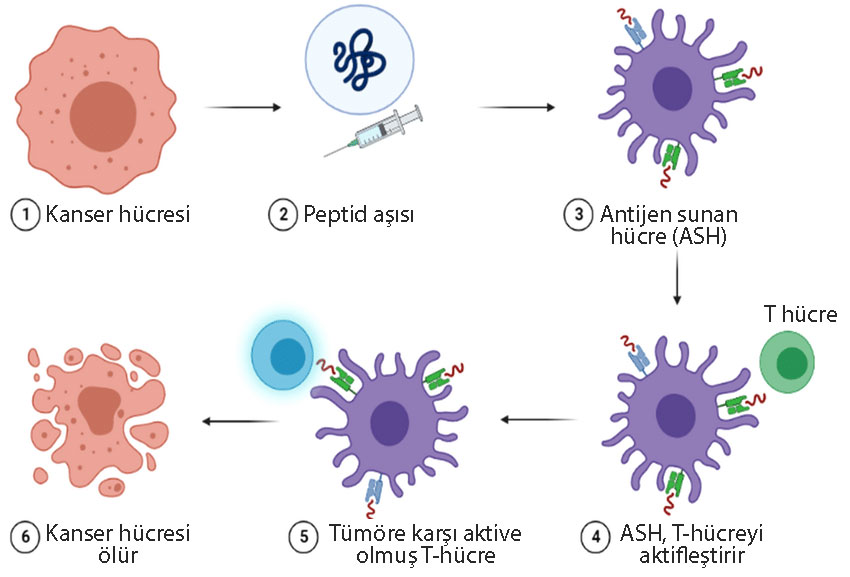
Bir kanser aşısı, hastaların bağışıklık sistemini harekete geçirmeyi, onu tümör hücrelerini tanıması, saldırması ve yok etmesi için hazırlamayı amaçlar. Peptid aşılama yaklaşımlarında, tümöre özgü antijenlerin sentetik peptid formları, aşı tasarlamak için kullanılmaktadır. Peptid-bazlı kanser aşıları genellikle istenen bağışıklık tepkisini ortaya çıkarmak için yüksek oranda immünojenik olduğu bilinen antijenlerden spesifik epitoplar içeren 20-30 amino asitten oluşur. Peptid aşının, özellikle güvenlik ve üretim kolaylığı açısından diğer aşı türlerine göre birçok avantajı vardır.
Bununla birlikte günümüzde tümöre özgü genetik çalışmalarla elde edilen kişiselleştirilmiş peptid-bazlı kanser aşı çalışmaları da vardır.
Akciğer Kanseri için UCPVax Aşısı
UCPVax, antitümör CD4+ T yardımcı-1 hücre yanıtını tetiklemek için tasarlanmış, yüksek düzeyde seçilmiş iki yardımcı peptitten oluşan yeni bir tedavi edici kanser aşısıdır.
Çalışma Detayları
Nisan 2016 ile Temmuz 2021 arasında daha önce tedaviler almış ve tedavilere direnç gelişmiş ileri evre küçük hücreli dışı akciğer kanseri olan yaklaşık 60 hasta çok merkezli bu çalışmaya dahil edildi.
Tedavi, 1, 8, 15, 29, 36 ve 43. günlerde 0.25 mg, 0.5 mg veya 1 mg aşı dozlarından oluşuyordu ve ardından en fazla 12 ay süreyle her 8 haftada bir rapel doz uygulandı.
Faz Ib klinik çalışmaya toplam 15 hasta kaydedildi ve faz IIa'da değerlendirilebilir 51 hasta tedavi edildi; 51 hastadan 15'i 0.25 mg, 16'sı 0.5 mg ve 20'si 1 mg doz aldı. Hastaların toplam %95'i önceden üç basamak sistemik tedavi almıştı.
Önemli Bulgular
- Çalışmanın Ib fazında doz sınırlayıcı yan etki gözlenmedi ve tolere edilen maksimum doz 1 mg olarak belirlendi.
- Faz IIa'daki hastalar arasında, UCPVax'ın üçüncü ve altıncı dozu, sırasıyla 51 hastanın %56'sında ve 39 hastanın %87,2'sinde spesifik CD4+ T helper-1 yanıtlarını tetikledi ve üç doz seviyesi arasında önemli bir fark gözlenmedi.
- Üçüncü dozdan sonra 0.25 mg alan 15 hastanın 7'sinde, 0.5 mg alan 16 hastanın 9'unda ve 1 mg alan 20 hastanın 13'ünde bir yanıt gözlendi. Takviye dozları aldıktan sonra değerlendirilen 18 hastanın neredeyse tamamında bir yanıt gözlendi.
- 20 hastada stabil hastalık ve 1 hastada tam yanıttan oluşan 21 hastada (%39) hastalık kontrolü gözlendi.
- 51 hastanın tamamında 1 yıllık genel sağkalım %34.1 idi (%95 güven aralığı [CI] = %23.1–50.4) ve ortanca genel sağkalım 9,7 aydı (%95 GA = 6,7–12,6 ay), doz seviyeleri arasında önemli bir fark gözlenmedi.
- Üç dozdan sonra immün yanıt verenler ve yanıt vermeyenler için, 1 yıllık progresyonsuz sağkalım %17,2 (%95 GA = %7,8-%38,3) ve %4,5 (%95 GA = %0,7–%30,8, P = 0,015) idi ve ortanca genel sağkalım 11.6 aydı (%95 GA = 9.7–16.7 ay) ve 5.6 aydı (%95 GA = 2.5–10 ay, P = .005). 1 yılda genel sağkalım %47.5 (%95 GA = %32.2-%70.0) ve %18.2 (%95 GA = %7.5-%44.1) idi.
Tedaviye bağlı en yaygın yan etkiler, 1. veya 2. derece enjeksiyon bölgesi reaksiyonları (%58.5), grip benzeri belirtiler (%16.1) ve gastrointestinal bozukluklar (%8.5) idi. Enjeksiyon yeri reaksiyonları, 0.5 mg ve 1 mg dozlarda daha yaygındı. 0.25 mg alan bir hastada derece 5 serebral vaskülit lezyonları vardı; olay muhtemelen tedaviyle ilgili olarak değerlendirildi ve beklenmedik olarak kabul edildi.
Sonuç
Sonuç olarak bu çalışmada UCPVax kanser aşısı, son derece immünojenik (bağışıklık tetikleyici) ve güvenliydi ve daha önce çok sayıda tedavi görmüş ileri evre küçük hücreli dışı akciğer kanserli hastalar için beklentilerin üstünde 1 yıllık genel sağkalım oranı sağladı. Araştırmacılar bu olumlu sonuçlar üzerine daha kapsamlı faz-III çalışmayı başlatacaklardır.
Peptid-bazlı kanser aşılarının, kişinin tümöründen elde edilen diğer kişiselleştirilmiş hücresel tedavilere kıyasla kolay hazırlama, daha ulaşılabilir olma ve uygun maliyet gibi avantajları vardır. Bu aşıların diğer immünoterapilere eklenemsinin daha etkili sonuçlara yol açıp açmayacağı merak konusudur.
*
NOT: UCPVax aşısının etki mekanizması, Küba aşısı ile benzer olmakla birlikte oldukça kritik farklara sahiptir. Küba aşısı CimaVax'ın sunduğu bağışıklık yanıtı, bağışıklık sisteminin ana hücreleri (T-hücre, NK’lar ve makrofajlar) üzerinden değil antikorlar üzerindendir, bu nedenler oldukça kısa süreli ve zayıf bir immün yanıt sunmaktadır. Fakat UCPVax kanser aşısı, etkinliğini CD4+ T-hücreler üzerinden göstermektedir ve bu sayede daha güçlü ve etkili bir antitümör bağışılık yanıt sağlıyor olabilir.
İlgili konu: Küba Kanser Aşısı Hakkında Gerçekler Nedir?
Olivier Adotévi, Dewi Vernerey, Pascale Jacoulet, Aurélia Meurisse, Caroline Laheurte, Hamadi Almotlak, et al. Safety, Immunogenicity, and 1-Year Efficacy of Universal Cancer Peptide–Based Vaccine in Patients With Refractory Advanced Non–Small-Cell Lung Cancer: A Phase Ib/Phase IIa De-Escalation Study. Journal of Clinical Oncology Published online September 07, 2022.






