
Kadcyla (ado-trastuzumab emtansine) Nedir? FDA Onayı, Türkiye Ruhsatı ve Geri Ödeme Durumu
Trastuzumab antikoruna kovalent bağla iliştirilmiş DM1 sitotoksik yük taşıyan bir antikor-ilaç konjugatıdır. Metastatik ve “neoadjuvan sonrası rezidüel invaziv hastalık” bulunan erken evre HER2-pozitif hastalarda tek ajan olarak kullanılır.
FDA Onay Geçmişi
- 22 Şubat 2013: Metastatik HER2-pozitif meme kanserinde, önceden trastuzumab ve taksan alan hastalar için tek ajan onay.
- 3 Mayıs 2019: KATHERINE verileri temelinde; neoadjuvan taksan+trastuzumab tedavisine rağmen rezidüel invaziv hastalık bulunan erken evre hastalarda adjuvan onay.
- Mayıs 2025: Etikette KATHERINE uzun dönem güncellemeleri (Klinik Çalışmalar bölümü) yayımlandı.
Kadcyla Nedir?
Kadcyla (ado-trastuzumab emtansine, T-DM1), HER2’yi hedefleyen trastuzumab antikoru ile hücre içine taşınan DM1 mikrotübül inhibitöründen oluşan bir antikor-ilaç konjugatıdır. 100 mg ve 160 mg flakonlar halinde IV infüzyon için hazırlanır.
Nasıl Etki Eder?
Kadcyla, meme kanseri hücrelerinin yüzeyindeki HER2 reseptörüne bağlanır. Kompleks internalize olduktan sonra lizozomal parçalanma ile DM1 serbestleşir ve mikrotübül polimerizasyonunu bozarak hücre bölünmesini durdurur, apoptoz başlatır. Trastuzumab bileşeni, HER2 sinyallemesini baskılar ve antitümör immün efektör mekanizmalarını tetikler.
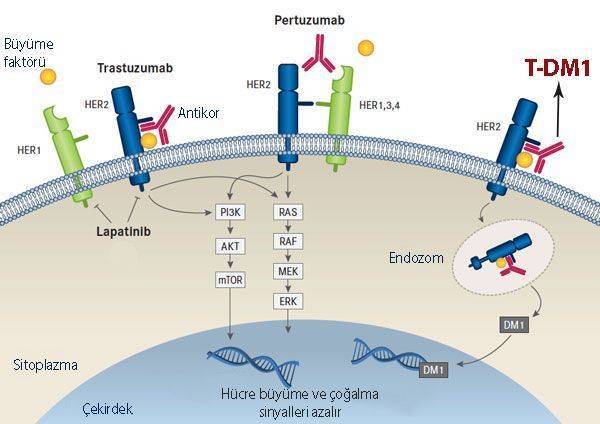
- T: Trastuzumab (hedefe yönelik antikor)
- DM1: Mikrotübül inhibitörü kemoterapötik yük
“Akıllı ilaç + kemoterapi” etkisini tek molekülde birleştirir.
Tedavinin Amaçları
- Metastatik evre: Tümör yükünü küçültmek, semptomları azaltmak, ilerlemeyi yavaşlatıp yaşam süresini uzatmak (palyatif hedef).
- Adjuvan (erken evre): Neoadjuvan tedaviye rağmen rezidüel invaziv hastalık varsa nüks riskini azaltmak ve küratif şansı artırmak.
Onaylı Endikasyon ve Klinik Konum
- Metastatik HER2-pozitif meme kanseri: Önceden trastuzumab ve bir taksan almış hastalarda tek ajan T-DM1.
- Erken evre HER2-pozitif: Neoadjuvan taksan+trastuzumab sonrası cerrahide rezidüel invaziv tümör saptananlarda adjuvan T-DM1 (genellikle 14 kür).
Hasta seçimi için onaylı HER2 testi (IHC 3+ veya ISH amplifikasyonu) gereklidir.
Türkiye Ruhsatı
Ürün, TİTCK kapsamında Roche ruhsatı ile kayıtlıdır. 100 mg ve 160 mg flakon formları mevcuttur;
Mart 2026 itibarı ile fiyatı:
Kadcyla 100 mg flakon fiyatı: 41.406,60TL dir.
Kadcyla 160 mg flakon fiyatı: 66.168,95 TL dir.
Ortalama 70 kg bir hasta için bir kürlük maliyeti: Yaklaşık 107.575,55 TL dir.
SGK Geri Ödeme Durumu
Metastatik meme kanserinde daha önce trastuzumab ve bir taksan tedavisi almış ve hastalığı sonrasında progresyon göstermiş, HER-2/neu testi immunhistokimyasal olarak 3+ (+++) veya FISH/SISH/CISH pozitif olan hastalarda kurtarma tedavisinde tek ajan olarak progresyona kadar kullanılır. Progresyon sonrası tek ajan veya kombinasyon tedavisinin bir parçası olarak kullanılamaz. Daha önce herhangi bir sebeple pertuzumab kullanmış hastalarda endike değildir. Tıbbi onkoloji uzman hekiminin yer aldığı ve bu hususların belirtildiği sağlık kurulu raporuna dayanılarak tıbbi onkoloji uzman hekimlerince reçete edilir.
Kanıtın Özeti
- EMILIA (faz 3, mBC): T-DM1, lapatinib+kapesitabin’e kıyasla PFS ve OS üstün; daha iyi tolere edilir.
- TH3RESA (faz 3, mBC): Ağır önceden tedavi görmüş popülasyonda OS/PFS faydası gösterildi.
- KATHERINE (faz 3, adjuvan): Neoadjuvan sonrası rezidü hastalıkta IDFS’de ~%50 rölatif risk azalması; uzun dönem verilerle kalıcı fayda.
Doz ve Uygulama Şeması
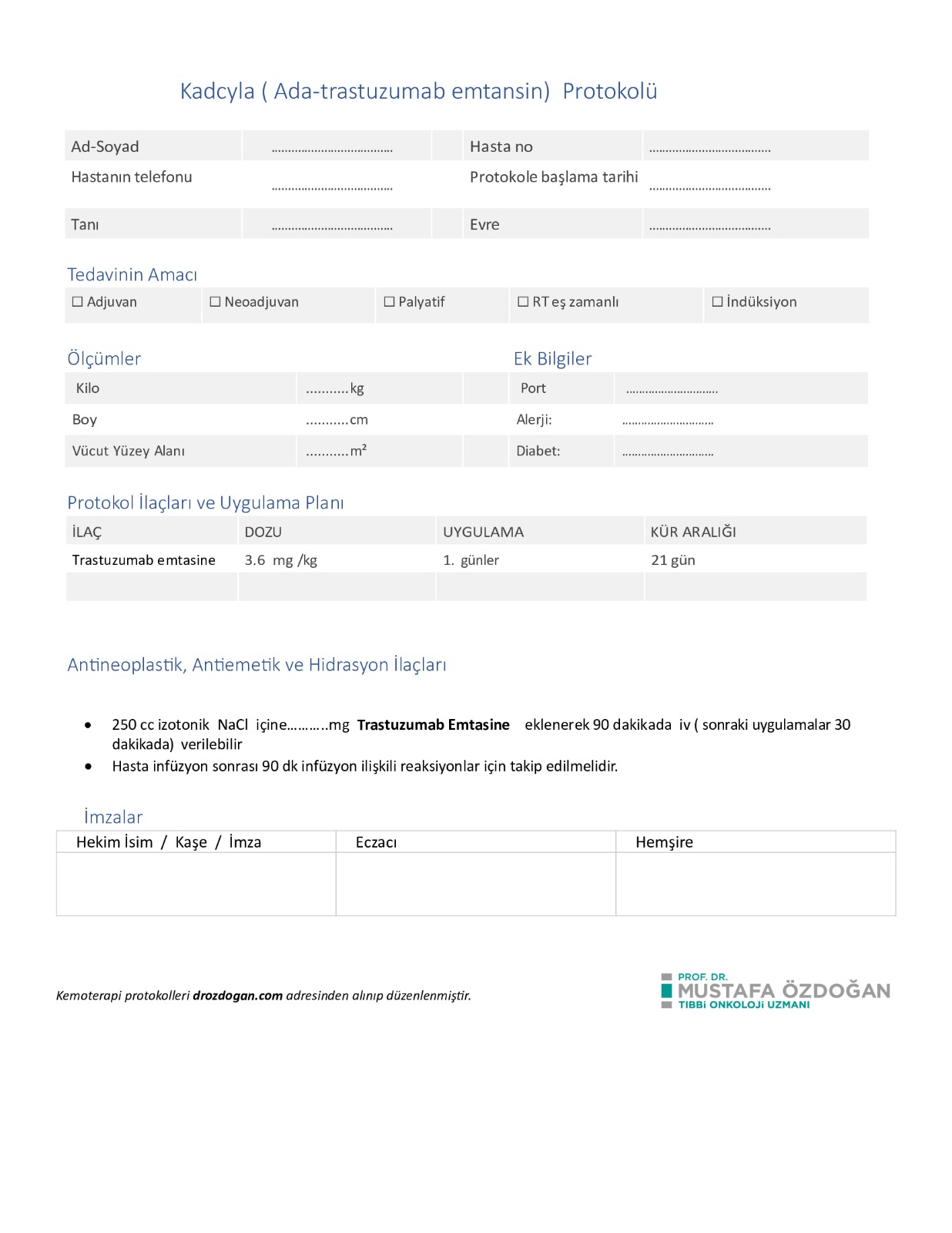
- Standart doz: 3.6 mg/kg IV, her 21 günde bir (3 haftada bir ). mBC’de progresyona/uygunsuz toksisiteye dek; adjuvan amaçla genellikle 14 kür.
- İlk infüzyon: Yaklaşık 90 dakika; tolere edilirse sonraki kürler ≥30 dakika.
- Uygulama ortamı: Günübirlik kemoterapi ünitesi; premedikasyon rutin şart değildir (klinik gerekliliğe göre).
Tedavi Süresi
- İlk kür toplam ziyaret süresi ~3 saate uzayabilir; sonraki kürlerde ~1.5 saat civarı.
- İnfüzyon sonrası 30–90 dk gözlem önerilir; reaksiyon durumunda infüzyon yavaşlatılabilir/durdurulabilir.
- Ön ilaçlar/sıvı destekleri toplam süreyi uzatabilir (kurum pratiği).
Uygulamada ve Kullanımında Dikkat
- Karaciğer toksisitesi: AST/ALT ve bilirubin artışı; nadiren nodüler rejeneratif hiperplazi — yakın izlem.
- Kardiyak toksisite: LVEF düşüşü; düzenli EKO/MUGA.
- Trombositopeni & kanama riski: Özellikle ilk döngülerde dikkat.
- İnfüzyon reaksiyonları/anafilaksi ve pnömonit (ILD) olasılığı.
- Gebelik: Embriyo-fetal risk; etkin kontrasepsiyon şart.
Tedavi Öncesi Kontroller ve Visit Arası İzlem
Başlangıçta
- HER2 doğrulaması (IHC 3+ veya ISH+; valide test).
- Doğurganlık çağında gebelik testi.
- Karaciğer fonksiyonları: AST/ALT, bilirubin.
- Tam kan sayımı: özellikle trombosit.
- Kardiyak değerlendirme: LVEF (EKO/MUGA).
Tedavi arası
- Her kür öncesi hemogram + biyokimya (AST/ALT/bilirubin, trombosit).
- LVEF ~3 ayda bir veya klinik gereklilikle daha sık.
- Yanıt değerlendirme için BT/PET-BT 2–4 kür aralıklarla (kurum pratiği).
Hasta Seçim Kriterleri
- HER2-pozitif (IHC 3+ veya ISH+), uygun performans durumu.
- Adjuvan: Neoadjuvan sonrası rezidüel invaziv tümör patolojik olarak gösterilmiş olmalı.
- Metastatik: Trastuzumab + taksan öyküsü.
- Not: Asya kökenli hastalarda trombositopeni riski daha yüksek olabilir (yakın izlem).
İlaç Etkileşimleri
- Güçlü CYP3A4 inhibitörleri (örn. klaritromisin, ketokonazol) → DM1 maruziyeti artar: mümkünse kaçın/çok yakın izlem.
- Güçlü CYP3A4 indükleyicileri (örn. rifampisin, karbamazepin) → etkinlik azalabilir.
- Antikoagülan/antiagreganlarla birlikte kanama riski açısından dikkat.
- Antifungal ve antiepileptiklerle potansiyel etkileşimler için ilaç listesi kontrolü.
Yan Etkiler ve Yönetimi
Sık Görülenler (≈%5+)
- Mide bulantısı (~%39)
- Halsizlik (~%35)
- Trombositopeni / kanama riski (~%28)
- İshal (~%23); Kusma (~%19)
- Anemi (~%10)
- Hipokalemi (~%9)
- Ağız yaraları (stomatit) (~%7)
- Nötropeni (~%6)
- El-ayak/deri reaksiyonları (~%1+)
Çalışmalara göre değişmekle birlikte tedaviyi bırakma oranı ~%6 civarında bildirilmiştir.
| Yan etki | Yönetim |
|---|---|
| Trombositopeni | Grade 3–4’te beklet; iyileşince doz azalt. |
| AST/ALT yükselmesi | Şiddete göre beklet; bilirubin eşlik ediyorsa kes. |
| LVEF düşüşü | Eşik altına inerse beklet; kalıcı düşüş/semptomatik KY’da kes. |
| Periferik nöropati | Grade ≥2’de beklet; düzelince azaltılmış dozla sürdür. |
| İnfüzyon reaksiyonu | Hafifte hız düşür/durdur; ağır/anafilaksi → kalıcı kes. |
| Pnömonit / ILD | Görüntüleme ile doğrula; orta-ağırda kes ve steroid düşün. |
İleri ön tedavisi olan olgularda lökopeni/nötropeni görülebilir; gerekirse G-CSF destekleri (filgrastim/pegfilgrastim) klinik endikasyonla kullanılabilir.
Doz Modifikasyonları
Kademeler
- Başlangıç: 3.6 mg/kg
- 1. Azaltım: 3.0 mg/kg
- 2. Azaltım: 2.4 mg/kg
- Daha fazla azaltım gerekirse: kes
Hematoloji
- Trombosit <75×10⁹/L: Beklet; ≥75 olduğunda azaltılmış dozla sürdür.
- Grade 4 (<25×10⁹/L): Düzelince bir kademe azalt.
Karaciğer/Kardiyak
- AST/ALT >5×ULN veya bilirubin >2×ULN: Beklet; klinik duruma göre kes.
- LVEF eşik altı: Beklet; kalıcı düşüş/semptomatik durumda kes.
Kaynakça
- US Prescribing Information — KADCYLA (ado-trastuzumab emtansine). Güncel etiket (Mayıs 2025), FDA.
- FDA Basın/Onay — 2013 mBC onayı; 2019 adjuvan onayı (KATHERINE).
- NEJM — KATHERINE: von Minckwitz ve ark., 2019.
- EMILIA & TH3RESA klinik özetleri — HCP materyalleri.
- Türkiye KÜB/KT — Roche/Medikaynak; ürün formları 100 mg ve 160 mg flakon.
- SGK — Bedeli Ödenecek İlaçlar Listesi (EK-4A); SUT kriterleri.
Verma S, Miles D, Gianni L, et al.
Trastuzumab Emtansine for HER2-Positive Advanced Breast Cancer.
N Engl J Med 2012






