
Kanser hücrelerinin bağışıklık sisteminden nasıl kaçtığına dair önemli bir keşif
Kanser tedavisinde yeni yaklaşımlara ilham olacak bir keşif
Kanser hücrelerinin bağışıklık sisteminden nasıl kaçtığı ile ilgili keşif yeni tedavi yaklaşımlarına ilham oluyor. Kanser hücreleri genetik karmaşayı yayması ile bilinir. Kanser hücreleri bölünürken DNA parçaları ve hatta tüm kromozomlar kopyalanabilir, mutasyona uğrayabilir ya da tümüyle kaybolabilir. Buna kromozomal kararsızlık denir ve Memorial Sloan Kettering'den (MSK) bilim insanları bunun kanserin agresifliği ile ilişkili olduğunu keşfetti. Kromozomlar ne kadar dengesiz ise, bu kromozomlardan gelen DNA parçaları da o kadar büyük olasılıkla ait olmadıkları yerde sonlanırlar: hücrenin merkez çekirdeğinin dışında, sitoplazmanın içinde yüzerler.
Hücreler, viral istilacıların kanıtı olarak DNA’nın bu parçalarını yorumlar, ki bu da hücre içi alarm çanlarını tetikler ve enflamasyona (iltihaplanmaya) yol açar. Bağışıklık hücreleri tümörün yanına gider ve savunma kimyasalları üretir. Buradaki gizem ise kanser hücreleri tarafından tetiklenen bağışıklık reaksiyonunun neden bu hücreleri çökertemediğidir?
Kanserin kaçış hilesini aydınlatan çalışma
"Odadaki fil, kanser hücrelerinin nasıl hayatta kalabildiklerini ve bu inflamatuvar ortamda gerçekten gelişebildiğini anlamadığımızdandır" diyor MSK ’da doktor-bilim insanı ve İnsan Onkoloji ve Patogenez Programı üyesi Samuel Bakhoum.
28 Aralık Cancer Discovery dergisinde Dr. Bakhoum’un laboratuvardan yayımlanan yeni bir çalışmaya göre bunun nedeni, kısmen kanser hücrelerinin yüzeyinde bulunan ENPP1 adlı bir molekülün, uyarıcı sinyalleri her seferinde komşu bağışıklık hücrelerine ulaşmadan önce yok etmesi ile ilgilidir. Bulgular bazı tümörlerin neden immünoterapiye yanıt vermediğini açıklamaya yardımcı olur ve eşdeğer öneme sahip olan hücresel yollar gösterir: onları immünoterapiye duyarlı hale getirecek yollar.
Tehlikeli DNA parçalarının tespiti
Dr. Bakhoum uyarı sistemi çalışmaları cGAS – STING olarak adlandırılır. Bir virüsten (ya da kararsız bir kanser kromozomundan) gelen DNA bir hücrenin sitoplazmasında konumlanır, cGAS ona bağlanır. Oluşturulan birleşik molekül cGAMP olarak adlandırılır, bu da bir uyarı sinyali olarak görev yapar. Hücre içinde bu uyarı sinyali, STING olarak adlandırılan ve potansiyel bir viral istilacının acil sorununa hitap eden bir bağışıklık yanıtını aktive eder.
Ek olarak cGAMP’ın çoğu, komşu bağışıklık hücrelerine uyarı sinyali olarak görev yapan hücrelerin dışına da giderler. Onların STING yolaklarını aktive eder ve viral olarak enfekte olmuş hücreye karşı bir bağışıklık saldırısını serbest bırakır.
Bakhoum laboratuvarındaki bir önceki çalışma kanser hücrelerinin içindeki cGAS-STING sinyalinin metastaz yapma yeteneklerine yardımcı olan – özellikle sinsice ilerleme ve yayılma kapasitesine – bağışıklık hücrelerinin özelliklerine adapte olan hücrelere sebep olduğunu göstermişti. Bu, kanser hücrelerinin inflamasyonlu ortamda nasıl hayatta kaldığı ve süreç içindeki metastaza nasıl yardımcı olduğu sorusuna verilecek cevabın bir kısmını karşıladı.
Uyarı sinyallerinin engellenmesi
Yeni çalışma kanser hücrelerinin cGAS-STING’in çevreye salınmasını aktive eden uyarı sinyalleri ile nasıl başa çıktığını gösterir. Makas benzeri bir protein hücrelerin bağışıklık yıkım tehditlerini önleyebildikleri ikinci bir yolu sağlayarak sinyalleri keser.
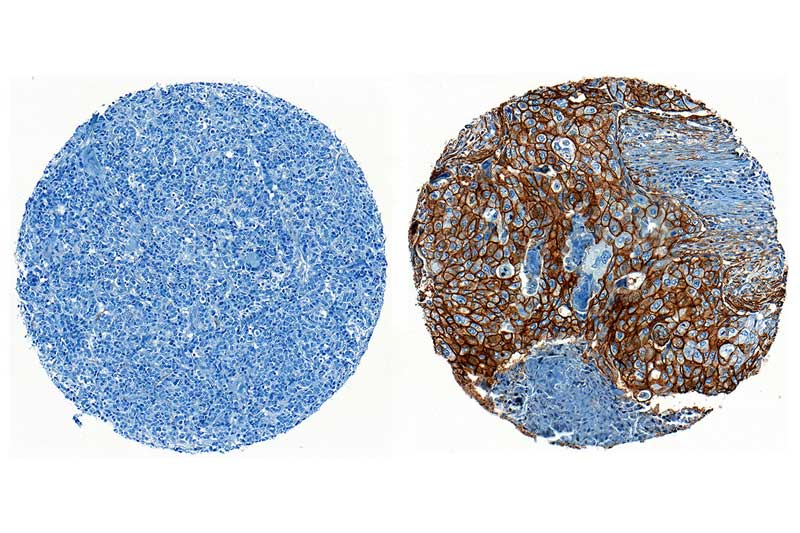
Yukarıda, ENPP1 ifadesi için negatif (sol) ve pozitif (sağ) boyayan, üçlü negatif meme kanseri doku örnekleri.
Kanser hücrelerini kaplayan makas benzeri protein ENPP1 olarak adlandırılır. cGAMP hücre dışında yolunu bulduğunda, ENPP1 onu keser ve bağışıklık hücrelerinden ulaşan sinyali engeller. Aynı zamanda, bu kesme adenozin olarak adlandırılan bağışıklık baskılayan bir molekülü serbest bırakır, ki bu ayrıca inflamasyonu da baskılar.
Meme, akciğer ve kolorektal kanserlerinin fare modelinde yürütülen deneyler aracılığı ile Dr. Bakhoum ve meslektaşları ENPP1’in bağışıklık baskılamak ve metastaz yapmak için "bir kontrol düğmesi" gibi hareket ettiğini gösterdi. Onu açmak bağışıklık yanıtlarını baskılar ve metastazı artırır, onu kapatmak ise bağışıklık yanıtlarına olanak sağlar ve metastazı azaltır.
Bilim insanları ayrıca insan kanserlerinin örneklerinde de ENPP1’e baktı. ENPP1 ifadesi hem artan metastaz hem de immünoterapiye direnç ile ilişkiliydi.
İmmünoterapiyi güçlendirmek
Tedavi perspektifinden bakıldığında, ENPP1 anahtarını kapatmanın, kontrol noktası inhibitörleri olarak adlandırılan immünoterapi ilaçlarının birkaç farklı kanser tiplerinin duyarlılığını artırabilmesi belki de çalışmanın en göze çarpan bulgusudur. Araştırmacılar bu yaklaşımın kanserin fare modellerinde etkili olduğunu gösterdi.
Şu anda Dr. Bakhoum ve meslektaşlarının kurduğu bir şirketinde içlerinde olduğu birkaç şirket, kanser hücreleri üzerindeki ENPP1’i inhibe edecek (engelleyecek) ilaçlar geliştiriyor. Dr. Bakhoum ENPP1’in kanser hücrelerinin yüzeyinde olmasının şanslı bir durum olduğu çünkü bu durumun ENPP1’i engellemek üzere dizayn edilmiş ilaç için onu daha kolay bir hedef yaptığını söylüyor. Ayrıca zamanda nispeten spesifiktir de. Sağlıklı bir bireyde diğer dokuların çoğu inflame (iltihaplı) olmadığı için ENPP1’i hedefleyen ilaçlar ilk olarak kanseri etkiler.
Sonuç olarak, ENPP1’in hedeflenmesi kanseri iki ayrı yolda keser: Dr. Bakhoum “Kanser hücrelerinin dışındaki cGAMP seviyesini eş zamanlı olarak artırıyorsunuz, ki bu ayrıca immün baskılayıcı adenozinin üretimini engellerken komşu bağışıklık hücrelerindeki STING’i aktive ediyorsunuz. Yani tek taşla iki kuş vuruyorsunuz” diyor.
Araştırmanın temposunun inanılmaz şekilde hızlı olduğunu söylüyor. “Gerçekten gurur duyduğum şeylerden biri, bu çalışmaya 2018 de başladığımız göz önünde tutulursa yakında hastalara yardımcı olarak sonuçlanması olacaktır” diye ekliyor Dr. Bakhoum. ENPP1 inhibitörlerinin faz-I klinik deneyinin bir yıl içinde olacağına inanıyor.
Jun Li, Mercedes A Duran,.. Samuel F Bakhoum, et al. Metastasis and immune evasion from extracellular cGAMP hydrolysis. Cancer Discovery, 2020; CD-20-0387






