Over, Fallop Tüpü veya Primer Periton Kanseri İçin Mirvetuximab Tam FDA Onayı Aldı
22 Mart 2024'te, ABD Gıda ve İlaç İdaresi (FDA), FRα pozitif, platine dirençli epitelyal over, fallop tüpü veya primer periton kanseri olan yetişkin hastalar için mirvetuximab soravtansine-gynx'i (Elahere, ImmunoGen, Inc. [şimdi AbbVie'nin bir parçası]) onayladı.
Hastalar bu tedavi için, daha önce bir ila üç basamak sistemik tedavi rejimi almış olmalıdır. Hastalar, FDA tarafından onaylı bir test ile folat reseptör alfa (FRα) pozitifliği yönünden belirlenmeli. Mirvetuximab soravtansine-gynx, daha önce 2022'de bu endikasyon için hızlandırılmış onay almıştı.
Tıbbi onkoloji alanında, kanser tedavisindeki yenilikler hayat kurtarıcı dönüşümler sunar. Bu yeniliklerin en çarpıcı örneklerinden biri, Folat Reseptör Alfa (FRα) pozitif, platine dirençli epitelyal over, fallop tüpü veya primer periton kanseri olan hastalar için tasarlanmış bir tedavi olan mirvetuximab soravtansine-gynx'in (Elahere) geliştirilmesidir. İlk olarak 2022'de hızlandırılmış onay alan bu ilaç, şimdi daha geniş bir klinik veri setine dayanarak 22 Mart 2024'te FDA tarafından tam onay almıştır. Bu, mirvetuximab soravtansine-gynx'in tedavi potansiyelinin ve güvenliğinin daha geniş çapta tanınması anlamına gelir.
Folat Reseptör Alfa'nın Önemi
Folat reseptör alfa (FRα), belirli kanser türlerinde, özellikle epitelyal over kanserinde %35-40 oranında ifade edilen bir protein olup, bu kanser hücrelerinin folat alımını artırır. Folat, hücre büyümesi ve DNA sentezi için kritik öneme sahiptir, dolayısıyla bu reseptörün aşırı ifadesi kanser hücrelerinin büyümesini ve yayılmasını destekler. FRα'nın yüksek ifadesi, hedeflenmiş terapilerin geliştirilmesi için benzersiz bir fırsat sunar ve mirvetuximab soravtansine-gynx bu potansiyeli gerçekleştirme yolunda önemli bir adımdır.
FRα Nasıl Tets Edilir?
Folat reseptör alfa (FRα) çalışmaları çeşitli yöntemlerle gerçekleştirilmektedir ve bu yöntemlerin başında immünohistokimya (IHK), akış sitometrisi, ve floresan görüntüleme teknikleri gelmektedir.
Çalışma Metodları
- İmmünohistokimya (İHK): FRα ekspresyonunu belirlemek için yaygın olarak kullanılır. Bu yöntem, doku kesitlerinde FRα'nın varlığını ve yoğunluğunu belirlemek için antikorların kullanıldığı bir tekniktir. Özellikle klinik çalışmalar ve tanı süreçlerinde önemli bir yer tutar.
- Akış Sitometrisi: Bu teknik, hücre yüzeyindeki FRα ekspresyonunu ölçmek için kullanılır. Tek tek hücrelerin yüzey antijenlerini tanımlamak için floresan işaretli antikorlar kullanılır.
- Floresan Görüntüleme: FRα hedefli floresan ajanlar kullanılarak tümörlerin intraoperatif olarak görüntülenmesi sağlanır. Bu yöntem, cerrahi sırasında tümör dokusunun daha etkin bir şekilde çıkarılmasına yardımcı olabilir
En Yaygın Kullanılan Metod
Şu anda en yaygın kullanılan yöntem immünohistokimyadır (İHK). Bu yöntem, FRα ekspresyonunun belirlenmesi ve sınıflandırılmasında yaygın olarak tercih edilmektedir. Örneğin, MIRASOL klinik araştırmasında, folat reseptör alfa (FRα) pozitifliği belirlemek için kullanılan immünohistokimya (IHK) testi, VENTANA FOLR1 (FOLR1-2.1) klonu ile gerçekleştirilmiştir. Bu klon, FDA onaylı bir teşhis aracı olarak kullanılmıştır ve özellikle yüksek FRα ekspresyonu olan over kanseri hastalarını tanımlamak için tasarlanmıştır. Bu çalışmada, tümör hücrelerinin en az %75'inde FRα membran boyaması ve en az 2+ yoğunlukta ekspresyon olması gerekliliği belirlenmiştir.
MIRASOL ile Gelen İkinci FDA Onayının Anlamı
Etkinlik, 453 platin dirençli epitelyal over, fallop tüpü veya primer periton kanseri hastası ile gerçekleştirilen çok merkezli, açık etiketli, aktif kontrollü, randomize, iki kollu MIRASOL Çalışması ile değerlendirildi.
Hastaların daha önce en fazla üç basamak sistemik tedavi almalarına izin verildi. Çalışma, tümörleri VENTANA FOLR1 (FOLR1-2.1) RxDx Assay ile belirlenen FRα ekspresyonu pozitif olan hastaları kaydetti.
Hastalar, mirvetuximab soravtansine-gynx 6 mg/kg (ayarlanmış ideal vücut ağırlığına göre) her 3 haftada bir intravenöz infüzyon olarak veya araştırmacının seçimi olan kemoterapi (paklitaksel, pegile liposomal doksorubisin veya topotekan) hastalık ilerleyene kadar veya kabul edilemez toksisiteye kadar alacak şekilde 1:1 oranında randomize edildi.
Sonuçlar
Başlıca etkinlik sonuç ölçütleri, genel sağkalım (OS), araştırmacı tarafından değerlendirilen ilerlemesiz sağkalım (PFS) ve araştırmacı değerlendirmesiyle onaylanmış toplam yanıt oranı (ORR) idi.
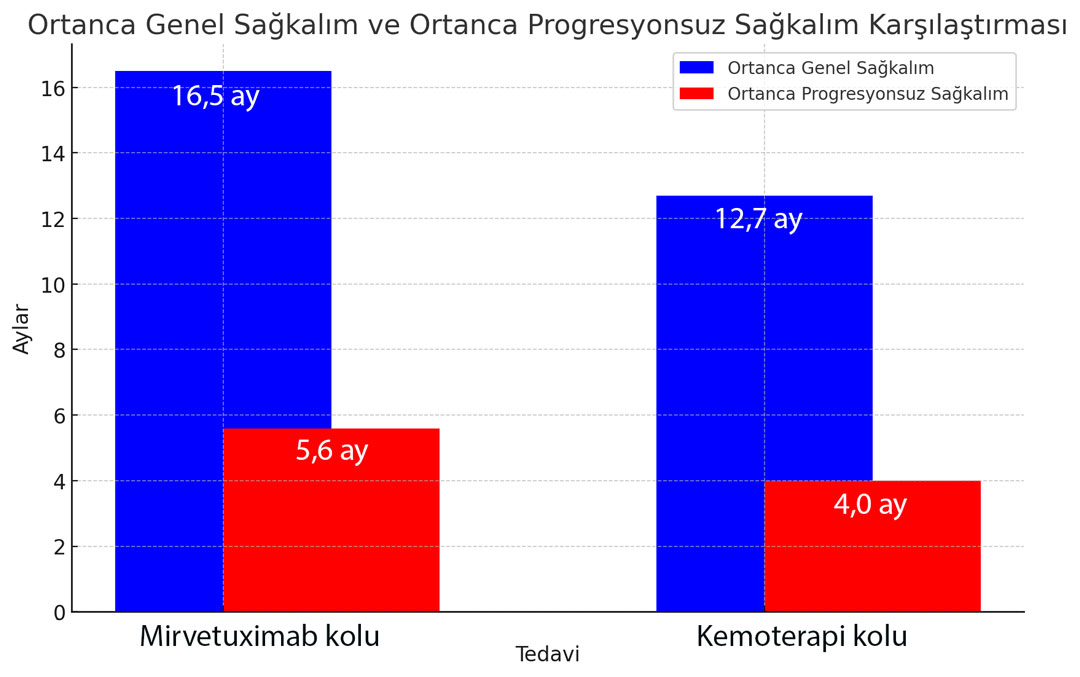
- Ortanca genel sağkalım, mirvetuximab soravtansine-gynx kolu için 16.5 ay (95% CI: 14.5, 24.6) ve kemoterapi kolu için 12.7 ay (95% CI: 10.9, 14.4) idi (Hazard Ratio [HR] 0.67 [95% CI: 0.50, 0.88] p-değeri 0.0046).
- Ortanca progresyonsuz sağkalım sırasıyla 5.6 ay (95% CI: 4.3, 5.9) ve 4 ay (95% CI: 2.9, 4.5) (HR 0.65 [95% CI: 0.52, 0.81] p-değeri <0.0001) idi.
- Objektif yanıt oranı sırasıyla %42 (95% CI: 36, 49) ve %16 (95% CI: 12, 22) (p-değeri <0.0001) idi.
Bir önceki hızlandırılmış FDA onayının konusu olan SORAYA Çalışması'nda mirvetuximab, beş tam yanıt dahil olmak üzere %31,7 objektif yanıt oranı göstermişti (%95 güven aralığı [GA]: 22,9, 41,6).
Elahere (mirvetuximab soravtansine-gynx) Etki Mekanizması Nasıldır?
ELAHERE (mirvetuximab soravtansine-gynx), bir folat reseptörü alfa bağlayıcı antikor, bölünebilir bağlayıcı ve hedeflenen kanser hücrelerini öldürmek için tasarlanmış güçlü bir tübülin inhibitörü olan maytansinoid DM4 kemoterapisi içeren, kendi sınıfının ilki olan bir antikor-ilaç konjugatıdır.
Elahere'nin bu hızlandırılmış onayı, yeni nesil antikor-ilaç konjugatlarını geliştirmeye adanmış onlarca yıllık çalışmaların bir kanıtıdır. Önümüzdeki süreçte çok daha fazla antikor-ilaç konjugatlarının kanser tedavisi için onay alacağını duyacağız.
Antikor–İlaç Konjugatı Nedir?
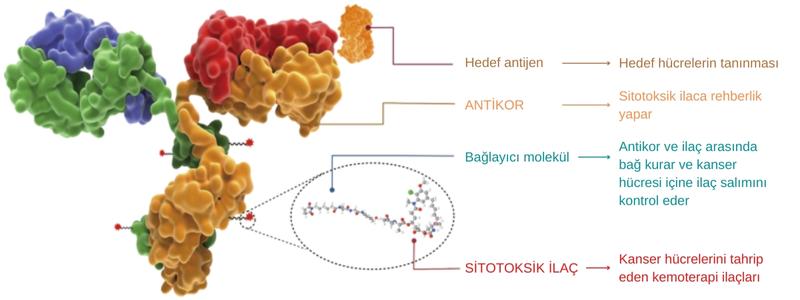
Antikor–ilaç konjugatları, tümördeki moleküler hedefi bağlayacak şekilde geliştirilen bir antikorun, kemoterapi ajanına eklendiği ve bunun belli bir tümör hücresine iletilmesine izin verdiği "Truva atı" yaklaşımını kullanır.
Aşağıda, antikor-ilaç konjugatlarının genel yapısı resmedilmiştir. Hedef antijenler, çoğunlukla kanserli hücrelerin yüzeyinde bulunur. Böylelikle antikor kanserli hücreye bağlanır ve daha sonra sitotoksik (hücre öldürücü) ilacı salar.
FDA approves mirvetuximab soravtansine-gynx for FRα positive, platinum-resistant epithelial ovarian, fallopian tube, or primary peritoneal cancer. 27.02.2024 https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-mirvetuximab-soravtansine-gynx-fra-positive-platinum-resistant-epithelial-ovarian