Over (kadın yumurtalık) kanseri tedavilerinde gelinen son nokta
Kadın yumurtalık epitelinden kaynaklanan kanserler tıbbi terim olarak over kanseri adlandırılmaktadır. 2018’de ülkemizde 3729 yeni over kanseri tanısı konmuş ve bu sayı yıllık tüm yeni kanser vakalarının %1.8’ini oluşturmaktadır. Ortalama görülme yaşı 63 olup, çoğu zaman erken belirti vermediği ve duyarlı bir kanser tarama testi olmadığı için hastaların %75’ine ileri evrede – yani kanser over dışına yayılmış, karında su birikimi (assit) başlamış durumda – tanı konmaktadır.
Over kanserinin standart tedavisi nerdeyse son 15 yıldır aynıdır; sitoredüktif cerrahiyi (ameliyat sırasında karında gözle görülen tüm tümörlerin çıkarılması) takiben verilen platin+taksan içeren kemoterapi. Ancak bu hastaların %70-80’inde ilk 2 yıl içinde kanserde rekürrens (tekrarlama) görülmektedir. Hastalık her tekrar ettiğinde bir sonraki basamakta verilecek tedavilere yanıt oranı giderek düşmektedir. Bu nedenle ilk tedavi sonrası hastalığın tekrar etmesine kadar geçen süre yaklaşık 18 ay iken, sonraki her tekrar ettiğinde bu süre 4 aya kadar düşmektedir.
Over kanserlerinin sık tekrarı nedeni ile hastalığın tekrarlamasına kadar geçen süreyi uzatacak idame tedavilere ihtiyaç vardır. Şu ana kadar bu konuda etkili bir tedavi bulunamamıştı. Ancak son 2 yıldır idame tedavide PARP inhibitörleri sayesinde beklenenden çok daha iyi sonuçlar elde edilmiştir. Sadece idame tedavisinde değil, çoklu tedavi almış over kanserli hastaların tedavisinde de PARP inhibitörleri ile başarılı sonuçlar elde edilmiştir.
PARP inhibitörlerinden ilk FDA onayı idame tedavide değil 4. basamak (olaparib – 2014) ve 3. basamak (rucaparib – 2016) tedavide olmuştur. Artık tedavi seçeneklerinin azaldığı bu basamaklarda bu ilaçlarla %30-50 yanıt oranları görülmesi ve hastalık ilerlemesine kadar geçen süreleri 9 aylara çıkarması çok sevindiricidir. Olaparib ve rucaparibden sonra niraparib de Ekim 2019’da 3 basamak ve sonrasında hastalığı ilerleyen homolog rekombinasyon eksikliği olan (BRCA mutasyonu olan veya olmayan) hastaların tedavisinde onay aldı. Bu basamaklardaki FDA onayı BRCA mutasyonu olan hastalar için geçerlidir. Günümüzde özellikle çoklu tedavi alan hastalarda immunoterapi ile veya diğer hedefe yönelik tedavilerle PARP inhibitörlerinin kombine edildiği çalışmalar devam etmektedir.
Poli (ADP-riboz) polimeraz, DNA mutasyonlarını tamir eden hücresel sistemlerden birisidir ve kısaca PARP olarak adlandırılır. PARP sisteminin çalışmasını engellemek için küçük molekül sınıfından ilaçlar geliştirilmiştir; bunlardan olaparib (Lynparza), PARP inhibitörlerinin ilki ve en yaygın kullanılanıdır. Olaparib, daha önce over ve meme kanserinde kullanılması için FDA onayı almıştır... BRCA gen ailesi de bir başka DNA tamir sistemidir.
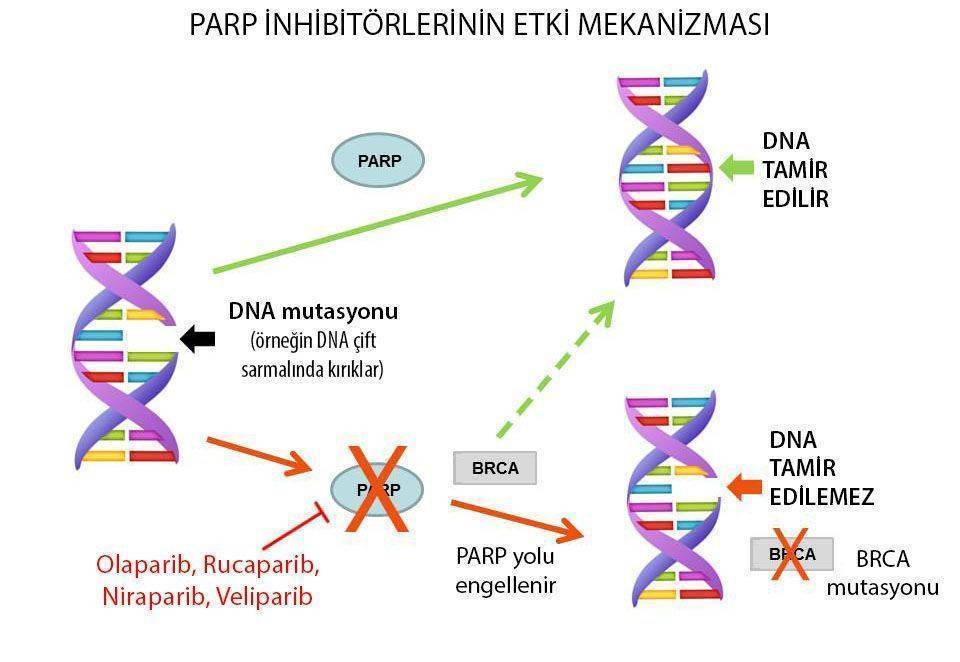
Şeklin açıklaması: Olaparibin etki ettiği BRCA ve PARP genleri DNA hasarlarının tamirinde görev alırlar. Bu genlerden sadece birisi bozuksa, kanser hücresi yaşamına devam eder. Ancak ikisi de bozulursa kanser hücresi DNA tamirini etkili bir şekilde gerçekleştiremez. Bu nedenle germline (kalıtsal olarak) BRCA geni mutasyonlu hastalarda, PARP genini hedef alan PARP inhibitörleri, daha güçlü bir anti-kanser etkinlik gösterir.
İleri evre over kanserli hastalar için idame tedavide ilk FDA onayları iki sıra ve daha fazla tedavi alan hastalarda olmuştur. İdame tedavide onay alan ilk ilaç niraparib olmuştur (Mart 2017), daha sonra olaparib ve rucaparib sırayla onay almışlardır. Bu ilaçların başarılı bir kemoterapi sonrası idame tedavide verildiğinde hastalığın ilerlemesine kadar geçen süreyi 4 kat arttırdığı ve hastalığın tekrarlama veya ölüm riskini %70’den fazla azalttığı gösterilmiştir. Bu başarı BRCA mutasyonu olan hastalarda daha belirgin olmaktadır, ancak BRCA mutasyonu olmayan hastalarda da risk azalması %60’larda bulunmuştur. Bu itibarla 2 basamak ve üzeri idame tedavilerdeki FDA onayları BRCA mutasyonundan bağımsız olmuştur.
Birinci basamak tedaviden sonra idame tedavide ise ilk onay alan PARP inhibitörü olaparib olmuştur (Aralık 2018). İlk basamak sonrası idame tedavisinde olaparib alan hastalarda tekrarlama riskini %70 azaldığı görülmüştür. Bu basamaktaki FDA onayı BRCA mutant olan hastalarda geçerlidir. Nirapribin birinci basamak tedavi sonrası idame tedavi çalışması (PRIMA) Eylül 2019’da yayınlandı; humolog rekombinasyon eksikliği olan hastalarda progresyon riskini %57 azaltmış ve progresyon süresini 2 kat uzatmıştır, FDA onayı ise 29 Nisan 2020'de gelmiştir.
Her ne kadar idame tedavilerde BRCA mutasyonundan bağımsız olarak bu ilaçlar faydalı olsa da BRCA mutasyonu olanlarda bu fayda 2-3 kat daha fazladır. Son 5 yılda FDA tarafından onaylanan bu PARP inhbirötlerinin çığır açan başarılarına bakıldığında çıkarılacak olan sonuç şudur; Artık her over karsinomlu hastalarda BRCA mutasyonu bakmak gerekmektedir. Ancak bu ilaçlar henüz ülkemizde onaylanmadığı için geri ödeme kapsamında kullanılamamaktadır.