Sinovyal Sarkomda Dönüm Noktası – İlk T-Hücre Tedavisi FDA Onay Yolunda
Sinovyal sarkom, genellikle genç yetişkinleri etkileyen ve tedavisi zor bir yumuşak doku kanseri türüdür. Bu kanser türü, vücudun farklı bölgelerindeki sinovyal dokularda, yani eklem çevresindeki dokularda başlar ve metastaz yapabilir. Uzun yıllardır, sinovyal sarkomun tedavisinde önemli bir ilerleme kaydedilememiştir, bu da hastalar için sınırlı tedavi seçenekleri anlamına gelmektedir. Ancak, Adaptimmune Therapeutics'in geliştirdiği ve yakın zamanda Amerika Birleşik Devletleri Gıda ve İlaç Dairesi (FDA) tarafından öncelikli inceleme için kabul edilen afami-cel tedavisi, bu alandaki bilim ve umudu yeniden şekillendiriyor.
Afami-cel ve Adaptif Hücresel Tedavi
Afami-cel, sinovyal sarkom dahil olmak üzere solid (doku veya organ kaynaklı) tümörlere karşı mücadelede yeni bir umut ışığı sunan genetik mühendisliği destekli bir T-hücre reseptörü (TCR) T-hücre terapisidir.
Adaptif hücresel tedavi, hastanın kendi bağışıklık hücrelerinin, genellikle T-hücrelerinin, laboratuvar ortamında modifiye edilip güçlendirildikten sonra kanseri hedef alacak şekilde hastaya geri verildiği bir immünoterapi türüdür. Bu yöntem, bağışıklık sistemini doğrudan kanserle mücadele etmeye programlayarak hastanın kendi savunma mekanizmasını güçlendirir.
Afami-cel, MAGE A4 adlı bir proteini hedef alacak şekilde tasarlanmıştır. MAGE A4, hücrenin içinde, özellikle kanser hücrelerinin çekirdeğinde bulunan bir tümör antijenidir. Bu antijen, bazı kanser türlerinde normalden daha fazla ifade edilir ve mühendislik destekli T-hücre terapileri tarafından hedef alınarak, bu kanser hücrelerini seçici bir şekilde yok etmek için kullanılır.
MAGE A4 kanser hedefine yönelik tasarlanmış ve ileri evre sinovyal sarkom için tek doz olarak düşünülen bu yenilikçi tedavi, son on yıl içinde bu alanda ilk etkili tedavi seçeneği olma ve onay alma potansiyeline sahiptir. Pazopanib etken maddeli Votrient'in 2012 yılında onaylanmasından bu yana, sinovyal sarkom tedavisinde bir ilk olarak karşımıza çıkıyor.
Aşağıdaki görselde, hücresel düzeyde Afami-cel gibi mühendislik destekli bir T-hücre reseptörü (TCR) terapisinin nasıl çalıştığına dair bir süreç gösterilmektedir.
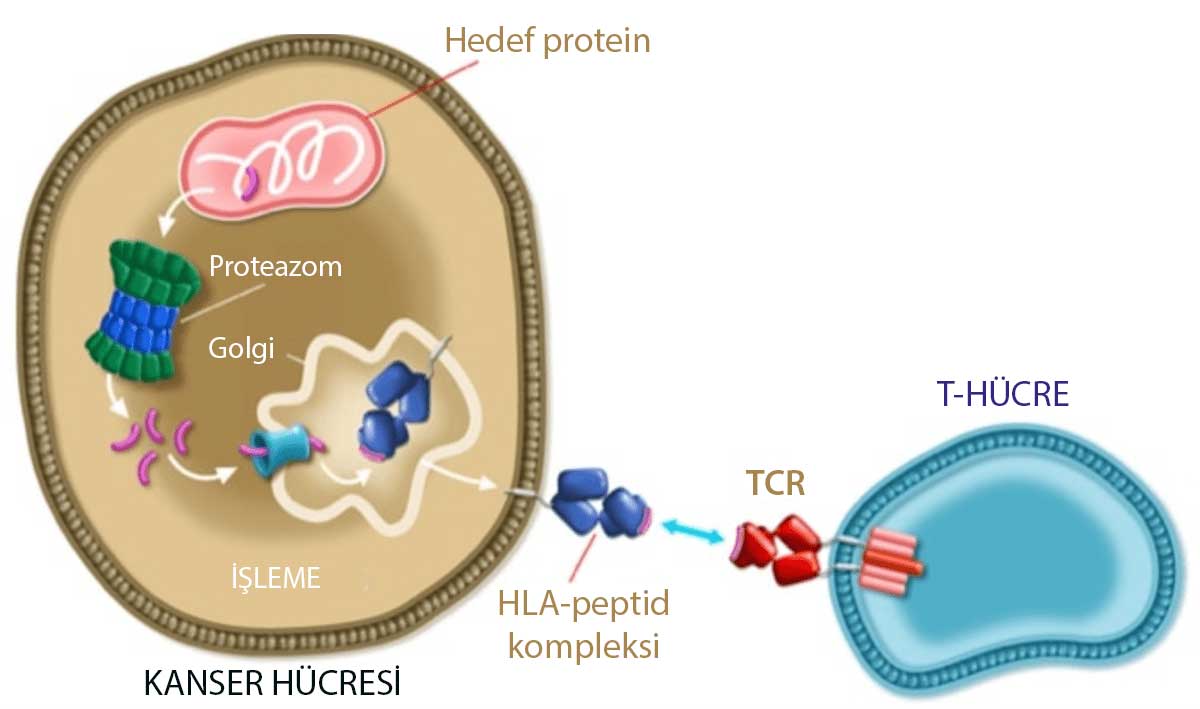
- Hedef proteini belirleme: Afami-cel, özellikle kanser hücrelerinde bulunan ve normal hücrelerde nadiren bulunan MAGE A4 gibi bir hedef proteini tanır.
- Proteini işleme: Hedef protein, hücre içindeki proteasom tarafından parçalanır ve peptid parçalarına ayrılır.
- HLA-peptid kompleksi oluşturma: İşlenmiş peptid parçaları, hücrenin yüzeyindeki HLA (Human Leukocyte Antigen) molekülleri ile birleşir. Bu kompleks, T-hücrelerinin tanıması için hücre yüzeyine taşınır.
- TCR ile tanıma ve etkileşim: Mühendislik destekli T-hücrelerin yüzeyinde bulunan T-hücre reseptörleri (TCR), bu HLA-peptid kompleksini tanır ve kanser hücrelerine spesifik olarak bağlanır.
- Kanser hücrelerine karşı etki: TCR'ların HLA-peptid kompleksine bağlanması, T-hücrelerinin kanser hücrelerini yok etmek için aktive olmasını tetikler. Bu aktivasyon, kanser hücrelerinin öldürülmesi ve böylece tümörün küçülmesi veya yok edilmesi sonucunu doğurur.
Bu mekanizma, Afami-cel gibi tedavilerin, yalnızca kanser hücrelerini hedef almasını ve sağlıklı hücrelere zarar vermemesini sağlayarak etkin bir kanser tedavisi sunmasını mümkün kılar.
Klinik Araştırma ve Sonuçları
SPEARHEAD-1 adlı kilit klinik çalışmanın 1. kohortundan elde edilen olumlu verilere dayanarak, Afami-cel'in etkinlik açısından birincil son noktayı karşıladığı gösterilmiştir.
Bu çalışmada, ileri evre sinovyal sarkomlu ve daha önce yoğun tedavi görmüş hastalarda,
- Genel yanıt oranı %39'du ve
- Ortanca yanıt süresi yaklaşık 12 aydı.
- Ortanca genel sağkalım yaklaşık 17 aydı ve
- Afami-cel'e yanıt veren hastaların %70'i tedaviden 2 yıl sonra hayattaydı.
Bu sonuçlar, Afami-cel'in sinovyal sarkomlu hastalar için yeni ve yenilikçi bir tedavi seçeneği sunabileceğinin altını çizmektedir.
FDA BLA Başvurusu ve Anlamı
Biologics License Application (BLA), biyolojik ürünler için FDA tarafından onay sürecinin bir parçasıdır. Afami-cel için yapılan BLA başvurusunun öncelikli inceleme için kabul edilmesi, tedavinin potansiyel onay sürecinin hızlandırılacağı anlamına gelir. Bu, Adaptimmune'nin sinovyal sarkom tedavisini yeniden tanımlama yolunda önemli bir adımı temsil eder. Prescription Drug User Fee Act (PDUFA) hedef karar tarihi 4 Ağustos 2024 olarak belirlenmiş olup, bu tarih, FDA'nın Afami-cel'in onayı hakkında karar vermesi beklenen son tarihtir.
Sonuç
Adaptimmune'nin Afami-cel için FDA BLA başvurusunun kabulü, sinovyal sarkoma sahip bireyler için tedavi yaklaşımlarını yeniden tanımlama potansiyeline sahiptir. Yıllardır beklenen bu ilerleme, ileri evre sinovyal sarkom tedavisinde umut verici yeni bir dönemi müjdeliyor. Afami-cel, mühendislik destekli T-hücre terapilerinin solid tümörler üzerindeki etkinliğini kanıtlama yolunda önemli bir adımdır ve onaylanması durumunda, hastalar için önemli bir tedavi seçeneği haline gelecektir.
Adaptimmune announces US FDA acceptance of Biologics License Application for afami-cel for the treatment of advanced synovial sarcoma with Priority Review. News release. Adaptimmune Therapeutics. January 31, 2024. Accessed February 2, 2024. https://www.adaptimmune.com/investors-and-media/news-center/press-releases/detail/260/adaptimmune-announces-u-s-fda-acceptance-of-biologics.