
Akciğer kanseri tedavisinde Atezolizumab FDA onayı aldı
Atezolizumab (Tecentriq) isimli immünoterapi ilacı, 18 Ekim 2016’da 4. evre (metastatik) Küçük Hücreli Dışı Akciğer Kanseri tedavisi için FDA onayı aldı.
OAK ve POPLAR adlı klinik çalışmaların sonuçları bu yeni nesil immün tedaviye FDA onayını getirmiştir.
OAK çalışmasına, daha önce akciğer kanserinin standart tedavilerinden olan platin tabanlı kemoterapi alan ve hastalığı ilerleyen 3. veya 4. evre küçük hücreli dışı akciğer kanserli (KHDAK) hastalar alınmış. Bu hastaların bir kısmına immünoterapi ilacı Atezolizumab uygulanırken, diğer kısmına dosetaksel adlı kemoterapi uygulanmış. Atezolizumab, dosetaksele göre yaşam sürelerini ortalama 4 ay artırmış (13,8 aya karşı 9,6 ay).
PD-L1, bağışıklık sistemi susturucusu olan hücre yüzey proteinlerinden biridir. Atezilozumab ise PD-L1 proteinini hedef alan bir ilaçtır; PD-L1’e bağlanır ve bu proteinin bağışıklık sistemi hücrelerini susturmasını engeller. Böylelikle savunma sistemimizin kansere karşı aktifleşmesini tetikler.
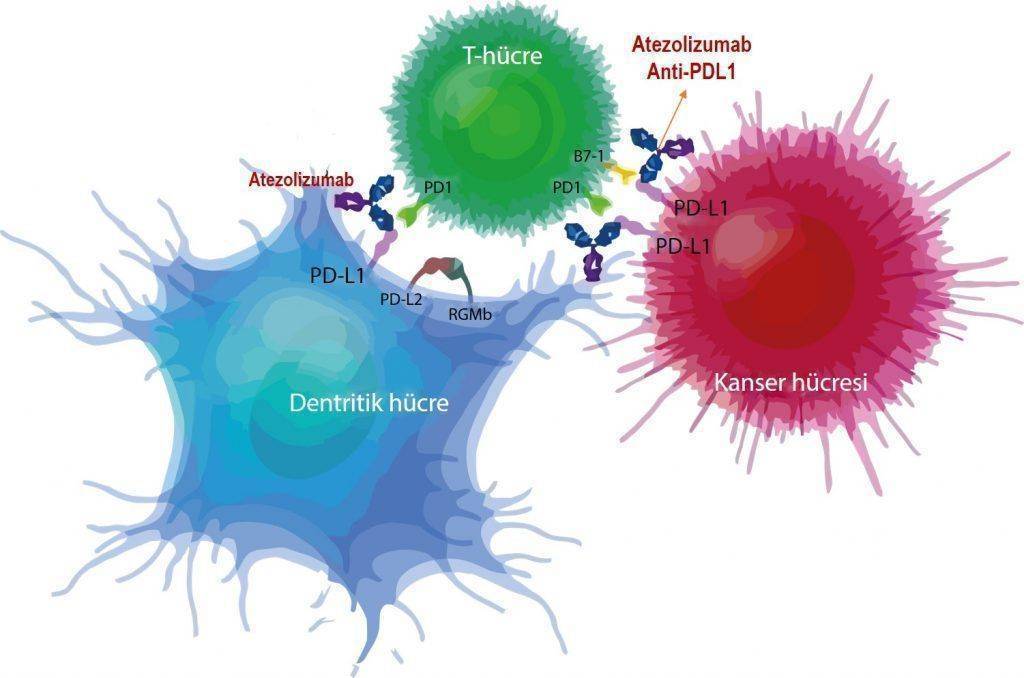
PD-L1 hücre yüzey proteini (ligand), hem tümör hem de bazı bağışıklık sistemi hücrelerinde (dentritik hücre gibi) bulunur. PD-1 ve B7 gibi kendine özgü algaçlara (reseptör) bağlanarak bağışıklık sistemi hücrelerinin pasif konuma geçirir. Atezolizumab gibi yeni nesil immünoterapi ilaçları bu susturucu molekülleri engelleyerek bağışıklık sisteminin kansere karşı aktifleşmesini tetikler.
Fakat bu immünoterapi ilacı akciğer kanserinin ikinci sıra tedavisi için denendiğinde, tümör hücrelerinin yüzeyinde farklı yoğunluklarda bulunan ve özel patolojik immünhistokimyasal yöntemlerle ölçülen PD-L1 düzeylerinden bağımsız bir şekilde etkili olabilmiştir. Yani Atezolizumab’ın uygulanması için immün tedaviler için bir biyolojik belirteç olarak değerlendirilen PD-L1 pozitifliği şartı yoktur.
- İlgili konu: Atezolizumab daha önce mesane kanseri tedavisi için de FDA onayı almıştı.
KHDAK ikinci sıra tedavisi için FDA onayı alan bu ilaç henüz ülkemizde kullanım onayı almamıştır. Klinik çalışmalarla etkinliğine dair kanıtlar arttıkça önümüzdeki dönemde ülkemizde de kullanım onayı alması muhtemeldir. Ülkemizde kullanım onayı alan yeni kanser ilaçlarının duyurusu da web sitemizden takip edebilirsiniz.
FDA Hematology/Oncology (Cancer) Approvals & Safety Notifications: Atezolizumab (TECENTRIQ)
https://www.fda.gov/ October 18, 2016






