Ameliyat Edilebilir Mide Kanserinde Durvalumab, Patolojik Tam Yanıtı 2.7 Kat Artırıyor
İmmünoterapi, Erken Evre Mide Kanserinde Sahneye Çıktı
Mide ve gastroözofageal bileşke adenokarsinomları, dünya genelinde kansere bağlı yaşam kayıplarının önde gelen nedenlerinden biridir. Bu hastalıklarda küratif (tam şifa) niyetle yapılan cerrahi tedavi halen ilk basamak yaklaşımdır. Ancak özellikle evre II–IVA arası lokal ileri hastalarda, ameliyat sonrasında yüksek oranda lokal veya uzak nüks gelişmektedir.
Bu nedenle, sadece cerrahi yeterli olmayıp multimodal (ameliyat öncesi ve sonrası) sistemik tedavi stratejileri gerekmektedir. Bu amaçla uygulanan perioperatif tedavi, kemoterapi ve/veya immünoterapinin hem cerrahiden önce (neoadjuvan), hem de cerrahiden sonra (adjuvan) verilmesini kapsar. Neoadjuvan tedavi, tümör hacmini küçültüp cerrahi başarıyı artırırken; adjuvan tedavi, mikroskobik kalıntı hastalığı ortadan kaldırarak nüks riskini azaltmayı hedefler.
Mide kanserlerinin tanı anındaki rezeksiyon (ameliyat) şansı, hastalığın coğrafi bölgeye, tarama uygulamalarına ve sağlık sistemine bağlı olarak değişmekle birlikte genel eğilim şu şekildedir:
🔍 Genel Durum: Erken Tanı Az, İleri Evre Yaygın
- Batı ülkelerinde (Avrupa, ABD, Türkiye dahil):
- Tanı anında ameliyat edilebilir (lokalize veya lokal ileri evre) hastalık oranı %30–40 civarındadır.
- Geriye kalan %60–70 oranındaki hastada ya uzak metastaz (M1) vardır ya da lokal invazyon çok ileri düzeydedir.
- Doğu Asya (özellikle Japonya, Güney Kore):
- Ulusal tarama programları sayesinde, hastaların %50–60’ı erken evrede tanı alır.
- Bu bölgelerde, tanı anında ameliyat edilebilirlik oranı %60–70'e kadar çıkar.
Önceki Standart: FLOT Rejimi ile Perioperatif Kemoterapi
2016 yılında yayımlanan FLOT4-AIO Faz 2/3 çalışması, bu hasta grubu için çığır açıcı bir gelişme sundu. Bu çalışmada, epirubisin + sisplatin + 5-FU/kapesitabin (ECF/ECX) ile karşılaştırıldığında, FLOT rejimi (5-FU, lökoverin, oksaliplatin ve dosetaksel) anlamlı derecede daha uzun sağkalım ve daha iyi lokal kontrol sağladı.
Bunun üzerine, periyoperatif FLOT + cerrahi yaklaşımı, Avrupa başta olmak üzere birçok ülkede evre II ve üzeri mide veya GEJ adenokarsinomları için standart tedavi haline geldi.
Ancak FLOT rejimiyle dahi, nüks oranları yüksek kalmaya devam etti. Bu, hastaların bir kısmında mikroskobik rezidü hastalığın (MRD) ve bağışıklık sisteminden kaçan tümör hücrelerinin kalmaya devam ettiğini düşündürdü. Bu nedenle, bağışıklık sistemini aktive eden tedavilerin bu döneme entegre edilmesi gündeme geldi.
Yeni Soru: Bağışıklık Sistemiyle Harekete Geçen Bir FLOT Daha mı Etkili?
Bağışıklık kontrol noktası inhibitörleri (örneğin anti–PD-1/PD-L1 antikorları), ileri evre mide ve GEJ kanserlerinde kemoterapiyle kombine edildiğinde sağkalımı uzatabilmektedir. Ancak şimdiye kadar bu ajanlar, küratif niyetli rezeke edilebilir hastalıkta perioperatif dönemde sistematik olarak test edilmemişti.
İşte tam bu noktada, MATTERHORN Faz 3 çalışması, standart FLOT tedavisine bağışıklık sistemini hedef alan anti–PD-L1 ajanı durvalumabı ekleyerek perioperatif dönemde sağkalımı iyileştirip iyileştiremeyeceğini araştırdı.
Bu çarpıcı çalışma, 2025 ASCO Kongresi’nin Plenary oturumunda sunuldu ve aynı gün NEJM dergisinde eşzamanlı olarak yayımlandı.
MATTERHORN Çalışması: Tasarım ve Katılımcılar
- Tasarım: Faz 3, çok merkezli, çift kör, randomize kontrollü
- Katılımcılar: 948 hasta (474 durvalumab + FLOT, 474 plasebo + FLOT)
- Hasta özellikleri: Evre II–IVA, rezeke edilebilir mide veya GEJ adenokarsinomu, ECOG 0–1
- Tedavi şeması:
- 2 kür neoadjuvan durvalumab + FLOT ya da plasebo + FLOT
- Cerrahi
- 2 kür adjuvan durvalumab + FLOT ya da plasebo + FLOT
- Ardından 10 kür durvalumab ya da plasebo idamesi
Temel Bulgular: Olaydan Bağımsız Sağkalım (EFS)
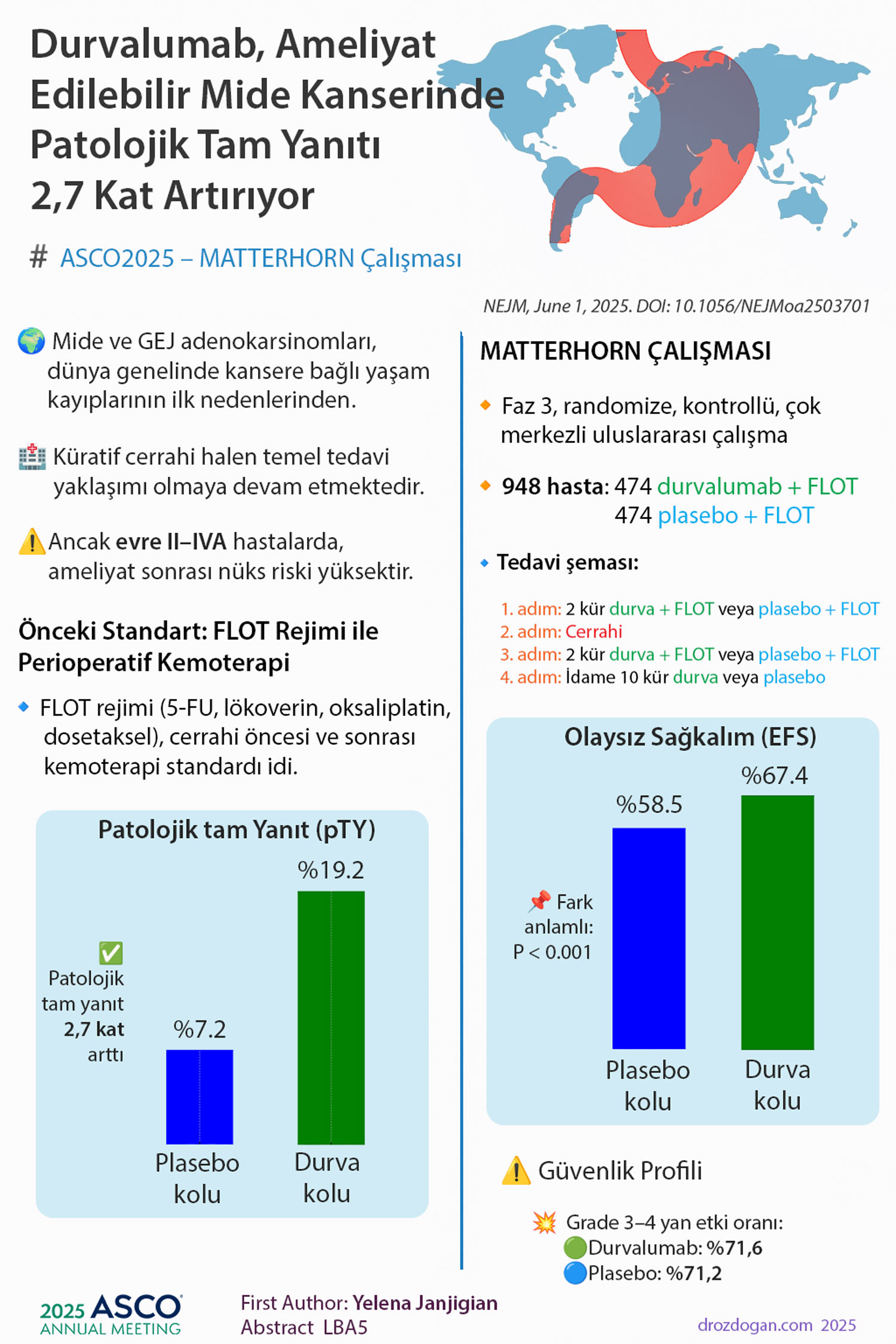
- 24 aylık olaysız sağkalım (EFS):
- Durvalumab + FLOT: %67,4
- Plasebo + FLOT: %58,5
- Risk azaltma: Olay veya yaşam kaybı riski %29 azaldı (HR: 0.71; %95 GA: 0.58–0.86; P<0.001)
🧠 Klinik Anlamı: Bu veri, FLOT rejimine durvalumab eklenmesinin, nüksü geciktirdiğini ve hastaların küratif tedaviden daha fazla yararlanmasını sağladığını gösteriyor.
Patolojik Tam Yanıt (pTY) Oranları Belirgin Arttı
- pTY oranı:
- Durvalumab + FLOT: %19,2
- Plasebo + FLOT: %7,2
- Göreli artış: pTY olasılığı 2,7 kat arttı (RR: 2.69; %95 GA: 1.86–3.90)
📌 Not: Patolojik tam yanıt, sağkalım ile doğrudan ilişkili güçlü bir biyolojik yanıttır. Bu oranlardaki artış, tedaviye bağışıklık sisteminin katkısını açıkça göstermektedir.
Genel Sağkalım (OS): Eğilim Olumlu ama Sonuçlar Nihai Değil
- 24 aylık ortanca OS:
- Durvalumab + FLOT: %75,7
- Plasebo + FLOT: %70,4
- İlk 12 ayda fark yok; ancak 12. aydan sonra belirgin ayrışma (HR: 0.67; %95 GA: 0.50–0.90)
📈 Kısıtlama: OS farkı istatistiksel anlamlılık eşiğini henüz geçmedi (P=0.03), ancak eğilim güçlü ve takip devam ediyor.
Güvenlik Profili: Ekstra Toksisite Yok
- Grade 3-4 yan etki oranı:
- Durvalumab: %71,6
- Plasebo: %71,2
- İmmün ilişkili yan etkiler:
- Durvalumab: %23,2
- Plasebo: %7,2
🔒 Güvence: Durvalumab, FLOT’a eklendiğinde ek ciddi toksisiteye neden olmadı. Cerrahiyi geciktirme veya adjuvan tedaviye başlama oranlarında fark görülmedi.
Bölgesel Alt Gruplar: Türkiye Dahil Tüm Bölgelerde Fayda Tutarlı
Durvalumab + FLOT tedavisi, Asya, Avrupa, Kuzey ve Güney Amerika dahil tüm bölgelerde anlamlı pCR artışı sağladı.
| Bölge | pTY (Durvalumab + FLOT) | pTY (Plasebo + FLOT) | OR (95% GA) |
|---|---|---|---|
| Küresel | %19,2 | %7,2 | 3,08 (2,03–4,67) |
| Asya | %19 | %6 | 3,96 (1,39–11,26) |
| Almanya | %30 | %13 | 2,88 (1,13–7,35) |
| Brezilya | %29 | %3 | 11,94 (1,35–105,54) |
Sonuç: Yeni Bir Perioperatif Standart Doğuyor mu?
MATTERHORN çalışması, rezeke edilebilir mide ve GEJ kanserlerinde durvalumab + FLOT kombinasyonunun:
- ✅ Olaydan bağımsız sağkalımı anlamlı şekilde artırdığını,
- ✅ Patolojik tam yanıt oranını 2.7 kat yükselttiğini,
- ✅ Kabul edilebilir bir güvenlik profiline sahip olduğunu göstermiştir.
🧬 Sonuç olarak, durvalumab + FLOT kombinasyonu, bu hasta grubu için dünya genelinde yeni bir perioperatif standart tedavi olmaya adaydır.
Janjigian YY, Al-Batran SE, Wainberg ZA, et al. Perioperative Durvalumab in Gastric and Gastroesophageal Junction Cancer. N Engl J Med. 2025; DOI: 10.1056/NEJMoa2503701.