Antikor-İlaç Konjugatı Yapısında Yeni İlaçlar, İleri Evre Kanserler için Geliyor
2022 ESMO Kongresinde, yeni antikor–ilaç konjugatlarının ileri evre solid tümörleri (organ/doku kaynaklı kanserleri) olan hastalar ile yapılan ilk insan denemelerinden umut verici verilerin elde edildiği bildirildi.
Antikor–İlaç Konjugatı Nedir?
Antikor–ilaç konjugatları, tümördeki moleküler hedefi bağlayacak şekilde geliştirilen bir antikorun, kemoterapi ajanına eklendiği ve bunun belli bir tümör hücresine iletilmesine izin verdiği "Truva atı" yaklaşımını kullanır. (konunun detayları için bakınız İlaç keşfinde son noktalardan biri – Hedefe yönelik antikor ve kemoterapi konjugatları)
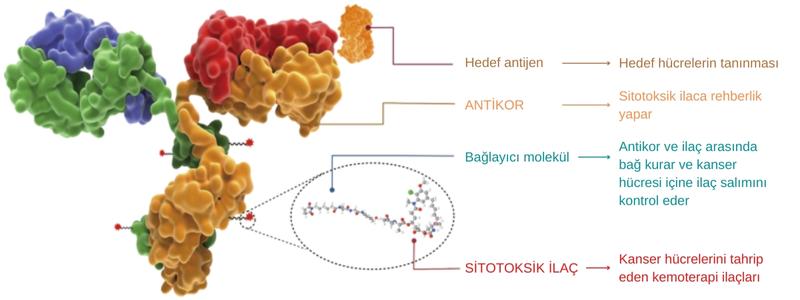
Aşağıda, antikor–ilaç konjugatlarının genel yapısı resmedilmiştir. Hedef antijenler, çoğunlukla kanserli hücrelerin yüzeyinde bulunur. Böylelikle antikor kanserli hücreye bağlanır ve daha sonra sitotoksik (hücre öldürücü) ilacı salar.
ESMO 2022'de İki Sunum
Çalışmaların verileri, önceden ağır şekilde tedavi edilmiş kanserleri olan hastalarda umut verici yanıtlar ve güvenlik profilleri bildirmektedir.
Çalışmanın ilk sunumunda, ileri evre solid tümörü olan 147 hastada, topoizomeraz I inhibitör yükü ile B7-H3’e yönelik bir antikor–ilaç konjugatı olan DS-7300’ün doz bulma faz I/II çalışmasından elde edilen verilen sunuldu.
Daha önce ortanca 5 basamak farklı tedavi alan hastalarda, %32'lik bir yanıt oranı ve %71.4'lük bir hastalık kontrol oranı gözlemlendi.
Küçük hücreli akciğer kanserli (KHAK) olan 19 hastadan 11’i (%58), ortanca 5,5 aylık yanıt süresi ile kısmi veya tam yanıt elde etti. Daha önceki kısa vadeli verilerle karşılaştırıldığında hiçbir yeni güvenlik sinyali rapor edilmedi; ancak en yüksek doz grubundaki daha fazla hasta, düşük dozlara kıyasla daha erken ortaya çıkan 3. derece olarak değerlendirilen yan etkilere sahipti.
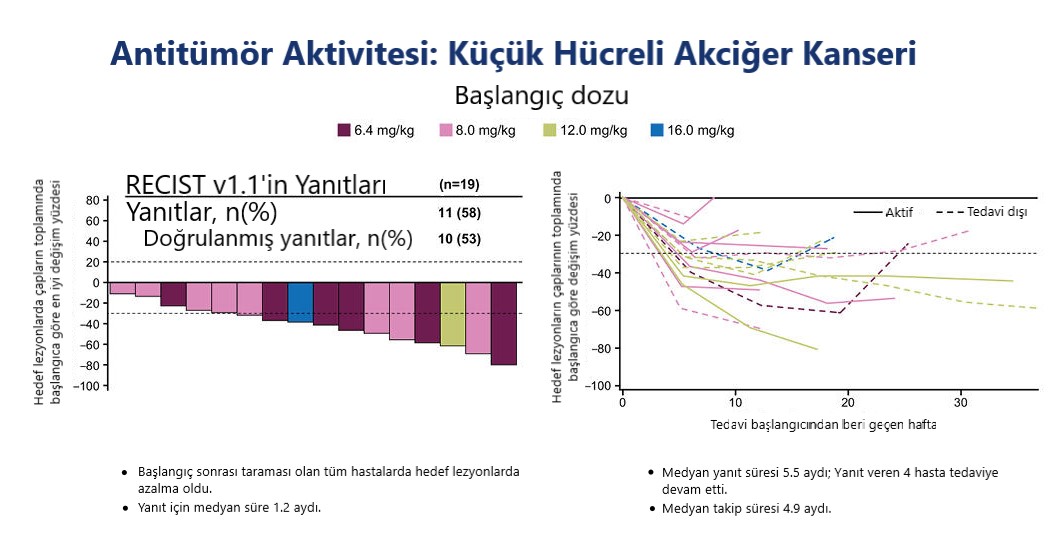
Bu çalışmada değerlendirilen bireysel tümör tiplerindeki hasta sayıları küçük olsa da en büyük yanıt agresif bir kanser olan KHAK'ya sahip hastalarda görülüyor. Bu hastalarda yanıt süresi, solid tümörlerde kullanılan diğer tedavi yöntemlerine göre uzun süreli olarak kabul edilmeyebilir ancak bunlar, özellikle tedaviye direnç kazanmış zor bir hastalık türü için kesinlikle umut verici verilerdir.
Çalışmanın ikinci sunumunda, HER2'ye yönelik bispesifik bir antikor ve bir auristatin toksini içeren antikor–ilaç konjugatı zanidatamab zovodotinin (ZW49) doz yükseltme ve doz genişletme faz I çalışmasından elde edilen ön sonuçlar da bildirildi. Önceden ağır şekilde tedavi edilmiş HER2 pozitif kanserli 77 hasta değerlendirildi ve bunların sırasıyla %27'si gastroözofageal ve %22'si meme kanserine sahipti. Bir hastada haftada bir uygulanan 1.75 mg/kg'da ve başka bir hastada da 3 haftada bir uygulanan 2.5 mg/kg'da doz sınırlayıcı toksisite gözlendi. Toplamda, hastaların %91'inde tedaviyle ilgili yan etkiler vardı ve bunlar çoğunlukla 1. veya 2. derece yan etkilerdi. Hastaların %12'sinde de 3. derece yan etkiler bildirildi.
Değerlendirilebilir 29 hasta arasında, her 3 haftada bir ZW49 2.5 mg/kg ile doğrulanmış objektif yanıt oranı %31 ve hastalık kontrol oranı %72 idi.
Bu çalışmadaki güvenlik sinyalleri makul görünüyor ve ayrıca, farklı tümör tipleri arasında bu antikor–ilaç konjugatının daha fazla değerlendirilmesini destekleyecek erken antitümör aktivitesi belirtileri var.
Sonuç
Antikor–ilaç konjugatları için büyük umut var, ancak standart sistemik kemoterapi ile gözlenen kalıcı hastalık kontrolünün olmaması burada da geçerli olabilir. Kombinasyon yaklaşımlarını değerlendiren, özellikle de bağışıklık sisteminin gücünden yararlanmaya çalışan çalışmaları sabırsızlıkla bekliyorum. Ayrıca, standart kemoterapi yaklaşımlarıyla ilişkili iyi bilinen toksisite göz önüne alındığında, antikor–ilaç konjugatlarının (neo)adjuvan sistemik tedavi uygulanan kanserlerde daha erken bir rol oynayıp oynamayacağı ve daha uygun bir yan etki profili gösterip gösteremeyeceği merak ediliyor.
Son olarak, kansere karşı bağışıklığı arttırmaya veya tümör mikroçevresine pozitif olarak modüle etmeye hizmet edenler de dahil olmak üzere ya doğrudan kanser karşıtı aktiviteye yol açarak ya da tümör mikroçevresini çeşitli ilaçlarla daha iyi yanıt verecek şekilde düzenlemeye hizmet ederek, kemoterapi dışındaki tedavilere kombine olacak şekilde yeni nesil antikor–ilaç konjugatlarının geliştirilip geliştirilemeyeceğini önümüzdeki dönemde görmeyi bekliyoruz.
1. Antibody–drug conjugates show potential in advanced solid tumours. (2022). ESMO daily reporter: https://dailyreporter.esmo.org/esmo-congress-2022/top/antibody-drug-conjugates-show-potential-in-advanced-solid-tumours
2. Doi T, et al. DS-7300 (B7-H3 DXd antibody drug conjugate [ADC]) shows durable antitumor activity in advanced solid tumors: extended follow-up of a phase I/II study. ESMO Congress 2022, Abstract 453O
3. Jhaveri K, et al. Preliminary results from a phase I study using the bispecific, human epidermal growth factor 2 (HER2)-targeting antibody-drug conjugate (ADC) zanidatamab zovodotin (ZW49) in solid cancers. ESMO Congress 2022, Abstract 460MO






