Gastrointestinal stromal tümör (GIST) tedavisi için avapritinib FDA onayı aldı
9 Ocak 2020'de ABD Gıda ve İlaç İdaresi (FDA), plateletten türetilmiş bir büyüme faktörü reseptörü alfa (PDGFRA) ekson 18 mutasyonu bulunan, metastatik evre veya cerrahi olarak tümörü çıkarılamayan gastrointestinal stromal tümörlü (GIST) yetişkin hastalar için avapritinib (Ayvakit) adlı ilacı onayladı.
Avapritinib, PDGFRA ekzon 18 mutasyonu bulunan GIST hastaları için onaylanan ilk tedavidir.
PDGFRA D842V mutasyonlu 38 hasta dahil olmak üzere PDGFRA ekzon 18 mutasyonu barındıran GIST'li 43 hastayı içeren çok merkezli, tek kollu, açık etiketli bir çalışma olan NAVIGATOR'da bu ilacın etkinliği araştırıldı. Klinik çalışmada başlangıçta hastalara günde bir kez 400 mg avapritinibverildi ve daha sonra toksisite (yan etkiler) nedeniyle günde bir kez oral olarak önerilen 300 mg dozuna düşürüldü. Hastalar hastalık ilerleyene veya kabul edilemez toksisiteye kadar avapritinib aldı. Başlıca etkinlik sonuç ölçüsü, genel yanıt oranı idi. Ek bir etkinlik sonuç ölçütü yanıt süresiydi.
- PDGFRA ekzon 18 mutasyonu bulunan hastalar için objektif yanı oranı % 84; % 7 tam yanıt ve % 77 kısmi yanıt idi.
- PDGFRA D842V mutasyonları olan hasta alt grubu için objektif yanı oranı % 89; % 8 tam yanıt ve % 82 kısmi yanıt vardı.
- 10.6 aylık takipte, hastaların yarısından çoğu tedaviye yanıt vermeye devam ettiği için ortanca yanıt süresine ulaşılamadı.
- Ekzon 18 mutasyonları olan ve yanıt veren hastaların % 61'inde 6 ay veya daha uzun süren bir yanıt vardı.
Avapritinib alan hastalarda en yaygın (≥% 20) yan etkiler ödem, bulantı, yorgunluk / asteni, bilişsel bozukluk, kusma, iştah azalması, ishal, saç rengi değişiklikleri, artan lakrimasyon (göz yaşı), karın ağrısı, kabızlık, döküntü ve baş dönmesidir.
Önerilen avapritinib dozu, aç karnına günde bir kez, yemekten en az bir saat önce ve iki saat sonra ağızdan 300 mg'dır.
*
İLERİ OKUMA
Gastroitestinal stromal tümör (GIST) nedir, tedavisi nasıldır?
Gastrointestinal stromal tümörler (GIST), her ne kadar nadir tümörlerden biri olsa da global yıllık sıklığı milyonda 10-15 vaka ile en yaygın mezenkimal kanserlerdendir. GIST, Cajal'ın interstisyel hücrelerinden, esas olarak gastrointestinal (GI) yoldan kaynaklanır, çoğunluğu midede bulunur (% 60).
Aşağıda, gastrointestinal stromal tümörlerin vücutta hangi organlarda ne oranda görüldüğü resmedilmiştir.

Patolojik tanı, immünohistokimya ve moleküler biyoloji gibi morfolojik özelliklere ve yardımcı tekniklere dayanır. GIST'lerin % 95'inden fazlası CD117 (c-KIT) için güçlü ve yaygın bir şekilde pozitiftir (KIT pozitif). Özellikle KIT-negatif GIST'lerde tanısal doğruluğu artırmak için birkaç yeni immünohistokimya (IHC) markırı incelenmiştir. Bunlar arasında, DOG1 (Discovered Gist-1), KIT pozitif GIST'lerin çoğunu ve KIT negatif tümörlerinin üçte birine kadar başarıyla tanımlayabilen oldukça hassas bir markırdır.
GIST'lerin malign potansiyelini belirleyen en önemli prognostik (hastalık gidişatı) faktörler tümör boyutu (5> cm ise kötü prognoz), 5 milimetrekarelik bir alan başına düzen mitoz sayısı ve tümör bölgesi. Son zamanlarda, tümör rüptürü (dağılması) ek bir olumsuz prognostik faktör olarak tanımlanmıştır.
Moleküler biyoloji önemli bir araçtır çünkü tanıyı doğrulamaya ve hedefe yönelik tedavilere hastalık duyarlılığına ilişkin prognostik ve prediktif değeri için yardımcı olabilir. Çoğu GIST'de, KIT veya trombosit türevli büyüme faktörü reseptör alfa ( PDGFRA ) genlerini içeren aktive edici mutasyonlar bulunabilir. GIST'lerin yaklaşık % 60-85'i KIT mutasyonları yönünden pozitiftir.
GIST'lerin 5-10'u PDGFRA mutasyonları yönünden pozitiftir ve genellikle lokalize gastrik tümörlerle ilişkilidir. PDGFRA mutasyonlarının % 65-75'i ekzon 18'de D842V mutasyonudur.
Gastrointestinal stromal tümörlerde (GIST) immünohistokimyasal boyama ve genetik analize genel bakış:
Mavi kesikli sınır CD117 / DOG1 + GIST'leri gösterir. Turuncu keskin sınır KIT / PDGFRA mutasyonları olan GIST'leri gösterir. Siyah kesik çizgiler GIST'leri somatik ve germ hattı mutasyonlarına ayırır.

GIST'ler, solid kanserlerin moleküler biyolojisini anlamak için önemli ve istisnai vakaları temsil eder. KIT inhibitörü imatinib, bir solid (organ) kanserin doğal sürecini kökten değiştirmiştir ve kanser tarihinin önemli dönüm noktalarından biridir. İmatinib gibi tirozin kinaz inhibitörü (TKI) sınıfından ilaçların aktivitesi büyük ölçüde KIT ve PDFRA genlerinde bulunan belli mutasyonlara bağlıdır. Gerçekten de tirozin kinaz inhibitörleri, KIT pozitif GIST'ler için standart terapidir ve avapritinib ile PDGFRA mutasyonu pozitif olanlar için de standart olmuştur. Yeni ve daha aktif TKI'lerin yaklaşan onayı ile moleküler profil, en iyi tedavinin seçimi için giderek daha önemli hale gelecektir.
Erişkinlerin yaklaşık % 10'u ve pediatrik GIST'lerin % 85'i her iki gende de bir mutasyon göstermez ve bu nedenle "wild (vahşi) tip GIST'ler" olarak tanımlanır. Bu tümörlerde, BRAF mutasyonunu aktive etme, NF1 mutasyonlarını inaktive etme veya süksinat dehidrojenaz (SDH) enzimatik kompleksinin bileşenlerini kodlayan genler ve kinaz NTRK3'ü içeren gen füzyonları dahil olmak üzere bir dizi genetik değişiklik tarif edilmiştir. Wildtype GIST'lerin klinik davranış spektrumu değişkendir, ancak metastatik hastalıkta bile yavaş ilerleme yaygındır.
GIST tedavisi nasıldır?
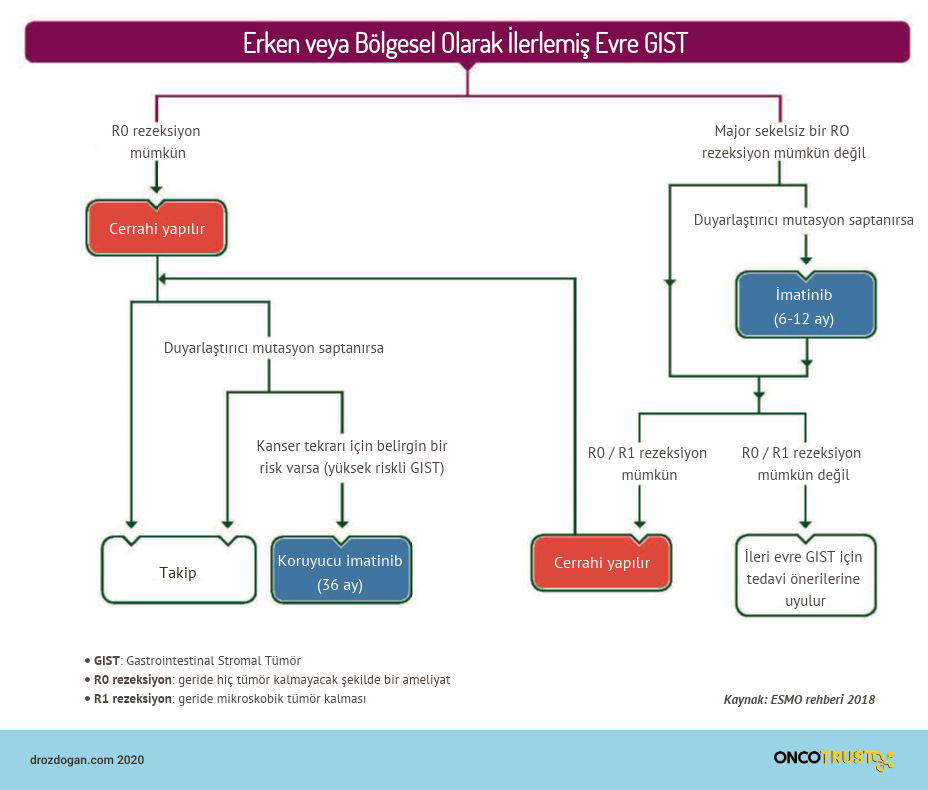
Gastrointestinal stromal tümörlerin tedavisi planlanırken, temel olarak hastalığın evresi ve risk faktörleri hesaba katılır. Aşağıdaki ilk görselde, "erken / bölgesel olarak ilerlemiş evre" GIST'lerin tedavi algoritmalarını özetledik. Avapritinib, erken evre GIST'te onay almadığı için, bu evre için tedavi yaklaşımı değişmemiştir.
*
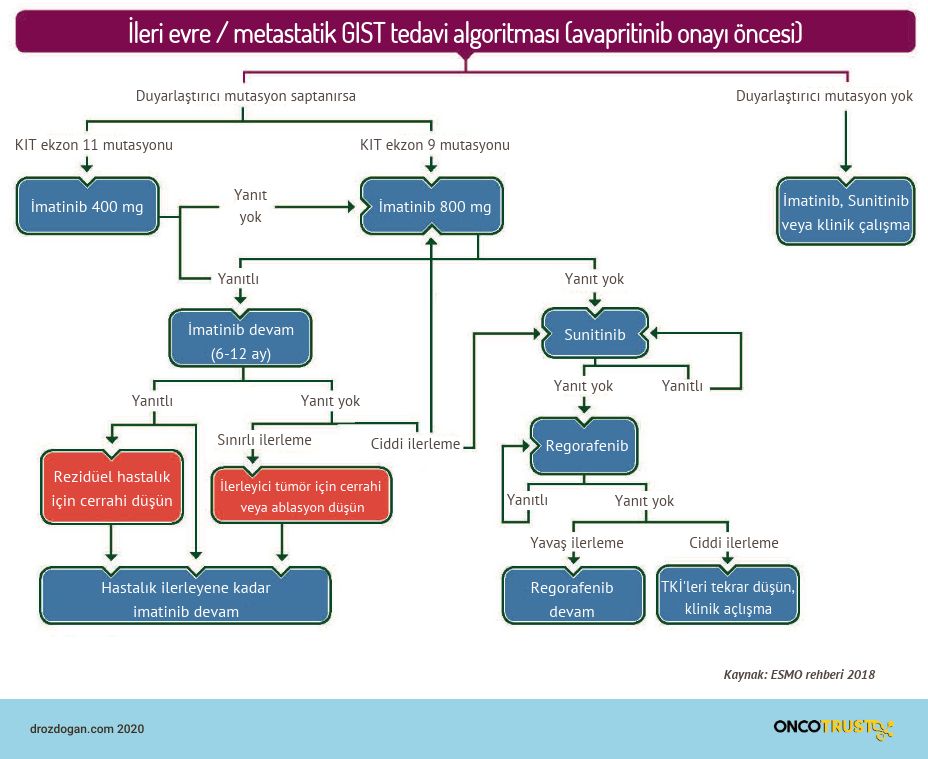
İkinci görselde "ileri / metastatik evre" GIST'lerin, "avapritinib öncesi" tedavi algoritmalarını özetledik.
*
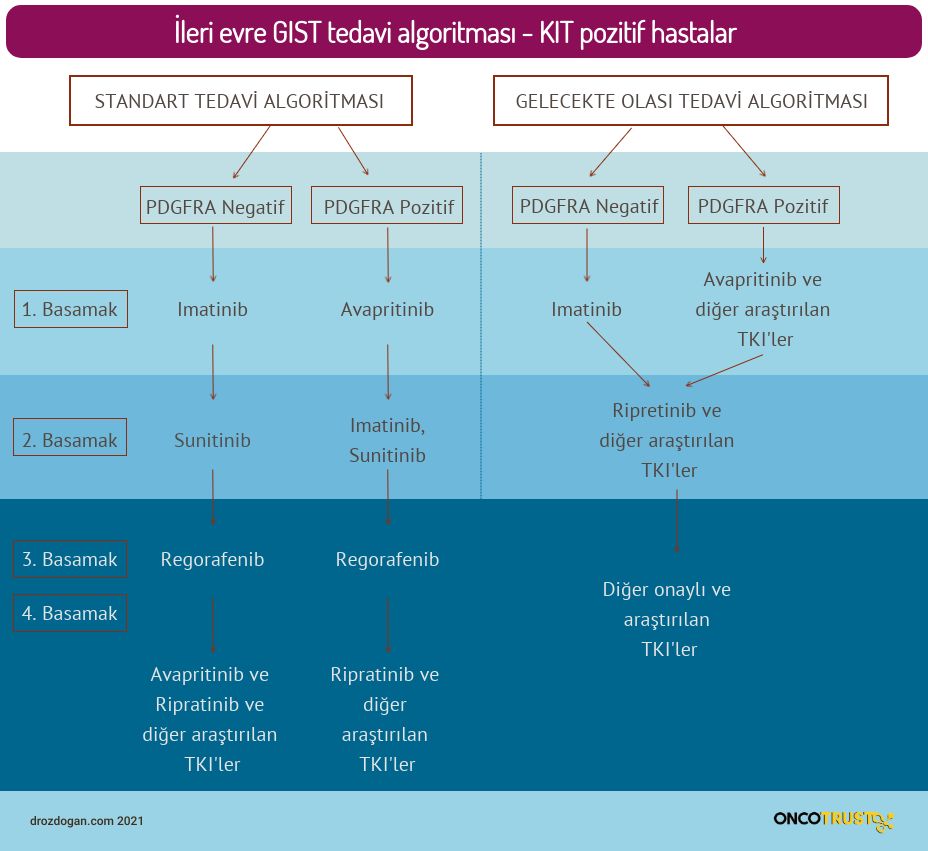
Üçüncü görselde "ileri / metastatik evre" GIST'lerin, "avapritinib sonrası ve gelecekte olası" tedavi algoritmalarını özetledik.
1. FDA approves avapritinib for gastrointestinal stromal tumor with a rare mutation.
fda.gov, 9 Jan 2020.
2. Mazzocca A ve ark.
New frontiers in the medical management of gastrointestinal stromal tumours.
Ther Adv Med Oncol. 17 may 2019.