
Merkel Hücreli Deri Kanseri Tedavisi İçin İlk Defa Bir İlaç FDA Onayı Aldı
FDA, deri kanserinin nadir görülen ve agresif bir şekli olan merkel hücreli karsinom tedavisi için ilk kez bir ilaca onay verdi. 23 Mart 2017 tarihinde FDA, metastatik merkel hücreli karsinomlu daha önce kemoterapi almayan hastalar da dahil olmak üzere yetişkin ve 12 yaş ve üstü pediyatrik hastaların tedavisi için avelumab adlı immünoterapi ilacına (piyasa adı Bavencio®) hızlandırılmış onay verdi.
Merkel Hücreli Cilt Kanseri Nedir?
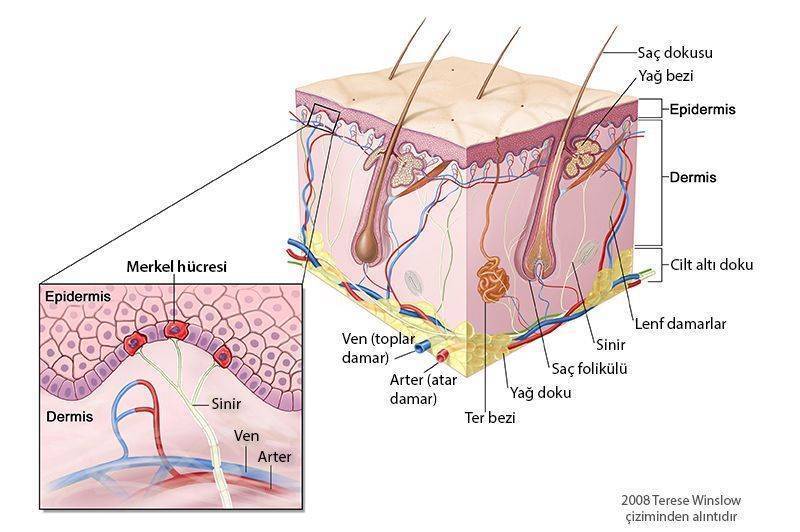
Merkel Hücreli Kanser, cildin “merkel” adı verilen hücrelerinden gelişen bir kanser türüdür. Ranvier veya dokunsal epitel hücreleri olarak da bilinen Merkel hücreleri, derimizde bulunan yüzeyel dokunma hissi için gerekli olan oval şekilli mekano-reseptörlerdir. Merkel hücreli kanser, çoğunlukla açık renkli cilde sahip ileri yaşlı erişkinleri etkileyen, bölgesel tekrarlama ve bölgesel lenf nodlarına metastaz yapmaya eğilimli, nadir görülen ve agresif biyolojide bir deri kanseridir. Bu tümörü tanımlamak için, cildin nöroendokrin veya primer küçük hücreli karsinoması, trabeküler hücre karsinoması ve cildin anaplastik kanseri de dahil olmak üzere çeşitli başka terimler de kullanılmaktadır. Nadir tümörlerden biridir, öyle ki ABD istatistiklerine göre yaklaşık her 166.000 kişide 1 gözükmektedir. Erkeklerde daha sıktır ve ortanca görülme yaşı erkekler için 74, kadınlar için 76’dır. Bu hastalık için tanımlanmış risk faktörleri güneşin UV ışınlarına yoğun maruziyet, açık renkli bir tene sahip olmak, bağışıklık sistemini baskılayan infeksiyonlara sahip olmak veya bağışıklık sisteminin baskılayan (immünsupresif) ilaçlar kullanmak ve ikincil kanserlere sahip olmaktır. Merkel hücreli karsinom lezyonlarının %81’i, güneş gören bölgelerde saptanmaktadır.
Merkel hücreli karsinom tanısı konulan bölgesel tümörü olan hastaların büyük bir kısmı ameliyat ile tedavi edilmeye çalışılırken, hastaların yaklaşık yarısında nüks (hastalık tekrarı) görülmekte ve %30'dan fazlasında da kanser vücudun diğer bölgelerine yayılarak metastatik hastalık gelişmesine neden olmaktadır.
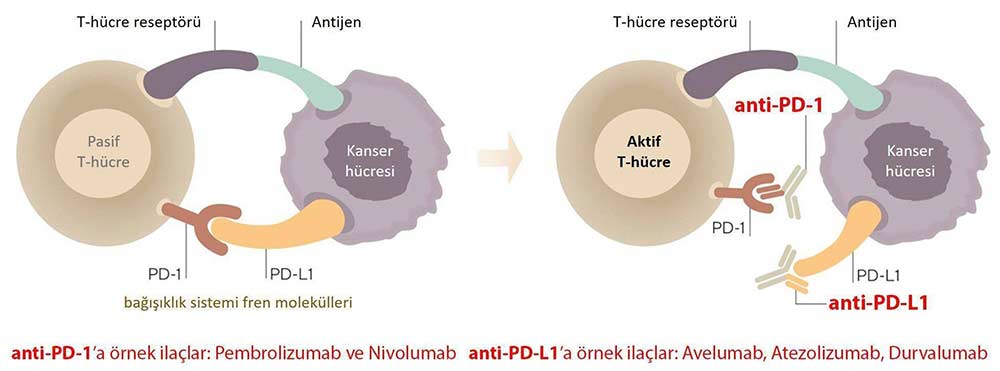
Avelumab, kanser hücrelerinin bağışıklık sisteminden saklanmasını sağlayan hücresel mekanizmalardan biri olan PD-1 ve PD-L1 protein etkileşmesini engelleyerek, bağışıklık sisteminin aktifleşmesine ve kanser hücrelerine saldırmasına yardımcı olan bir immünoterapi ilacıdır.
Çalışma
Avelumab onayı, daha önce en az bir kez kemoterapi rejimi uygulanmış 88 metastatik merkel hücreli karsinom tanılı hastanın dahil edildiği tek kollu bir çalışmadan elde edilen verilere dayandırılmaktadır. Çalışmada tam veya kısmı yanıt oranları (genel yanıt oranı) tümör boyutunun küçülmesine göre değerlendirilmiştir. Ayrıca tedaviye yanıt veren hastalarda tümörün kontrol altında tutulduğu süreler (yanıt süresi) incelenmiştir. Avelumab ile tedavi edilen 88 hastanın %33’ünde tam veya kısmi yanıt gözlenmiştir. Tedaviye yanıt, hastaların %86’sında 6 aydan, %45’inde ise 12 aydan uzun sürmüştür.
Avelumabın sık rastlanan yan etkileri yorgunluk, kas iskelet sistemi ağrısı, ishal, mide bulantısı, damardan uygulama ile ilgili reaksiyonlar, döküntü, iştah azalması ve ekstremitelerin şişmesi (periferik ödem) sayılabilir.
Önerilen doz ve uygulama şekli: Her 14 günde bir, 10 mg/kg dozunda, toplardamardan 60 dakika boyunca infüzyon.
Avelumab FDA onayını, hastaların klinik yarar göreceği öngörülen klinik çalışma verilerini kullanarak, ciddi bir hastalık için tıbbi ihtiyacı karşılamak amacıyla FDA’ın ilaç onay mekanizmalarından biri olan hızlandırılmış prosedürle (accelerated approval) almıştır. Avelumab’ın klinik yararını doğrulamak için daha ileri klinik araştırmalara ihtiyaç duyulmaktadır ve ilaç sponsoru da bu çalışmalarını sürdürmektedir.
Hematology/Oncology (Cancer) Approvals & Safety Notifications.
fda - gov






