PARP inhibitörleri akciğer kanserinde immunoterapinin gücünü artırabilir
İmmünoterapi, pek çok kanser türünde hastaların yaşam süresinde anlamlı artışlar sağlamıştır. Ancak hastaların sadece % 20’si immünoterapilere yanıt vermektedir. Son zamanlarda immünoterapilerin etkinliğini artırmaya yönelik çalışmalar artmıştır. Bu bağlamda, Mart 2019’da The Journal of Clinical Investigation’da yayımlanan çalışmada, PARP inhibitörleri adlı ilaçların, DNA tamiri bozuk kanser hücrelerinde kullanıldığında bağışıklık tepkisini artırabileceği ve immünoterapinin etkinliğini genişletebileceği keşfedildi.
Araştırma, Londra’da bulunan Kanser Araştırma Enstitüsü’nde gerçekleştirildi.
Araştırmacılar, akciğer kanserli hastalarından aldıkları tümör örneklerinde DNA tamir bozukluklarını analiz ettiler. Araştırma sonuçlarına göre,
- DNA tamir genlerinde bozukluklara sahip tümörlerde daha fazla bağışıklık sistemi hücresi infiltrasyonu (istilası) olduğu görüldü. Bu durum, DNA tamir genlerindeki mutasyonlarının tümörlere karşı bağışıklık tepkisinin oluşmasını sağladığını göstermektedir.
- Aynı zamanda, ERCC1 ya da BRCA1 gibi DNA tamir genlerinde bozukluk olan küçük hücreli olmayan akciğer kanseri ve üçlü negatif meme kanseri hücrelerinde PARP inhibitörlerinin bağışıklık sistemi tepkisi üzerindeki etkisi incelenmiştir.
- DNA tamir sistemi bozuk olan kanser hücreleri PARP inhibitörleri ile tedavi edildiğinde, herhangi bir DNA tamiri gerçekleştiremedikleri ve DNA hasarlarının kanser hücresi ölünceye kadar biriktiği gözlemlenmiştir.
- PARP inhibitörlerinin kullanımıyla birlikte kanser hücrelerinde DNA hasarının birikmesi bir takım sinyal moleküllerinin salgılanmasını sağlamaktadır. Bu sinyal molekülleri, bağışıklık sistemi hücrelerini tümöre saldırmasını uyarmaktadır.
Küçük hücreli olmayan akciğer kanserine sahip hastaların % 30 – 50’sinde ERCC1 DNA tamir sisteminde bozukluk bulunmaktadır. Bu keşif, bu tip hastalarda etkili tedavilerin önünü açabilir.
PARP inhibitörleri (örneğin olaparib) kanser hücrelerinin DNA tamiri için kullandığı sistemlerden birini bloke eder. Bu tip inhibitörler özellikle DNA tamir sistemlerinde bozukluk olan tümörleri hedef almak için tasarlanmıştır. Özellikle kalıtsal BRCA1 mutasyonuna sahip meme ve over (kadın yumurtalık) kanserine sahip hastalarda bu ilaç etkili olmaktadır.
Peki bu çalışma bize ne ifade ediyor?
- PARP inhibitörlerinin kanser immünoterapisinin etkinliğini artırabileceği keşfedildi. DNA tamir mekanizmaları hatalı olan kanser hücrelerinde PARP inhibitörleri ve immünoterapi kombinasyonu, kanser hücrelerine karşı bağışıklık tepkisinin artmasını sağlayabilir.
- Bu sene içerisinde bu yaklaşımın akciğer, prostat ve mesane kanseri hastalarının dahil olduğu klinik çalışmada değerlendirilmesi planlanmaktadır.
*
MERAK EDENLER İÇİN İLERİ DÜZEY BİLGİ: Aşağıda, çalışmanın grafik özeti görülebilir:
PARP inhibitörü tedavisi sonrası, ERCC1 hasarına bağlı cGAS/STING aktivasyonunun modellenmesi
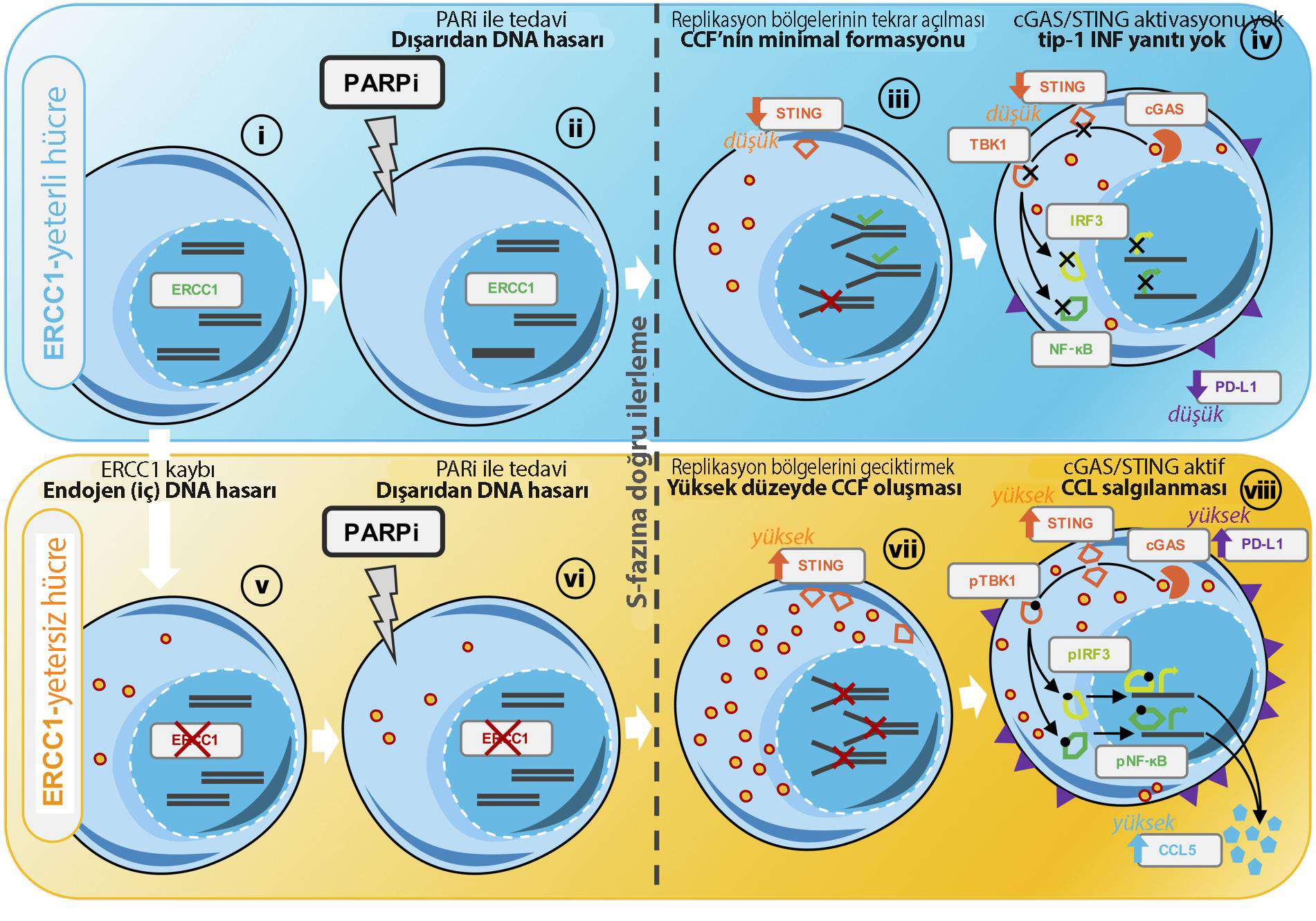
(i) ERCC1WT/WT hücreleri normal DNA tamir sistemlerine sahiptir ve genom yapılarını korumaktadır.
(ii) PARP inhibitörlerine (PARPi) maruz kalması üzerine, dışsal DNA hasarı tetiklenir, çoğunlukla kendiliğinden tek iplikçik kopma yerlerinde (SSB'ler) DNA'nın üzerinde bulunan PARP1'in kendisi tarafından başlatılır.
(iii) Hücre döngüsünün S evresi sırasında, kısaltılmış PARP1, çoğaltma çatallarının ilerlemesini önleyen, çatal durmasına ve ardından DSB'lerin oluşumuna yol açan lezyonlar üretir. ERCC1WT / WT hücrelerinde, en fazla tutulan PARP1 lezyonları çıkarılır ve bu, DSB'lerin HR yoluyla işlenmesini sağlar ve sonunda çoğalmanın yeniden başlatılmasını sağlar. Artık yetersiz onarımlı lezyonlar orta derecede CCF oluşumuna neden olur.
(iv) Üretilen düşük CCF seviyeleri, pTBK1 / IRF3 / NF-KB sinyal yolakklarını veya daha sonra tip-I IFN genlerinin transkripsiyonunu tetikleyemez; PD-L1 orta derecede uyarılır.
(v) ERCC1 - / - hücreleri, ERCC1'in kaybı sonrasi artmış endojen DNA hasarına maruz bırakılır. Bu durum CCF'nin seviyesini minimumda tutar.
(vi) PARP inhibitörü tedavisi sonrası, ERCC1 - / - hücreleri ek bir dış DNA hasarı kaynağına tabi tutulur.
(vii) Hücre döngüsünün S evresi sırasında, kısaltılmış PARP1, replikasyon çatallarının ilerlemesini önleyen, çatalların durmasına ve ardından DSB'lerin oluşumuna yol açan lezyonlar oluşturur. ERCC1'in yokluğunda, sıkışmış PARP1 lezyonları yeterince çözülemez, bu durum DSB'leri arttırır ve sonunda yüksek seviyelerde CCF üretir. CCF'ler cGAS tarafından tespit edilir ve ERCC1 - / - hücrelerinde STING'in artmış ifadesi nedeniyle, bunlar cGAS / STING sinyalini etkin şekilde aktive eder. Aktive edilmiş STING homodimer, IRF3 ve NF-κB'yi fosforile eden TBK1'i fosforile eder; bu, çekirdekte translokasyonlarını tetikler ve tip-1 IFN genlerinin transkripsiyonuyla sonuçlanır: CCL5 ve diğer tip-I IFN sitokinler salgılanır. Daha yüksek PD-L1 ekspresyonu, hücre yüzeyinde indüklenir. CCF'ler cGAS tarafından tespit edilir ve ERCC1 - / - hücrelerinde STING'in artmış ifadesi nedeniyle, bunlar cGAS / STING sinyalini etkin şekilde aktive eder. Aktive edilmiş STING homodimer, IRF3 ve NF-κB'yi fosforile eden TBK1'i fosforile eder; bu, çekirdekte translokasyonlarını tetikler ve tip-1 IFN genlerinin transkripsiyonuyla sonuçlanır: CCL5 ve diğer tip-1 IFN sitokinler salgılanır. Daha yüksek PD-L1 ekspresyonu, hücre yüzeyinde görülmeye başlar.
Chabanon RM, Muirhead G, Krastev DB ve ark.
PARP inhibition enhances tumor cell-intrinsic immunity in ERCC1-deficient non-small cell lung cancer.
J Clin Invest. 1 March 2019






