Safra Yolları Kanseri Tedavisinde Üçlü Kemoterapi Fark Yarattı
Nab-paklitaksel (Abraxane) adlı albumin bağlı nanotanecik ürünü kemoterapinin, gemsitabin-sisplatinin kombinasyonuna ilave edilmesi, sadece gemsitabin-sisplatin kullanımına kıyasla, ileri evre safra yolu kanserli hastalarda hayatta kalma süresini dikkat çekici bir şekilde uzatabileceği, sonuçları 18 Nisan'da JAMA Oncology'de yayımlanan bir faz 2 klinik araştırma ile gösterildi.
İleri evre safra yolları kanserinin (kolanjiokanser) standart tedavisi gemsitabin ve sisplatin ikilisidir ve bu yaklaşımla genel sağkalım 1 yıldan daha azdır. Safra yolları kanserleri, diğer kanserlere göre daha nadir görülmekle birlikte, her yıl dünya genelinde yaklaşık 130 bin yeni vaka olduğu tahmin edilmektedir. Bununla birlikte hastalık sonuçları genellikle kötüdür, genelde ileri evrelerde tanı konulur.
60 hastanın dahil olduğu bu araştırmada, gemsitabin + sisplatine nab-paklitaksel eklenmesi ile 11.8 aylık progresyonsuz (ilerlemesiz) sağkalım ve 19.2 aylık genel sağkalım süresi elde edildi.
Tarihsel olarak, standart tedavi görmüş ileri evre safra yolu kanserli hastalar için, ortanca progresyonsuz sağkalımın 8 ay ve ortanca genel sağkalımın 11,7 ay olduğunu biliyoruz.
Yeni tanı almış ileri evre safra yolları kanseri tedavisinin omurgasını yaklaşık 9 yıldır gemsitabin ve sisplatin oluşturmaktadır ve şu ana kadar gemsitabin ve sisplatine üstünlük gösteren hiçbir faz 3 randomize çalışma olmadı.
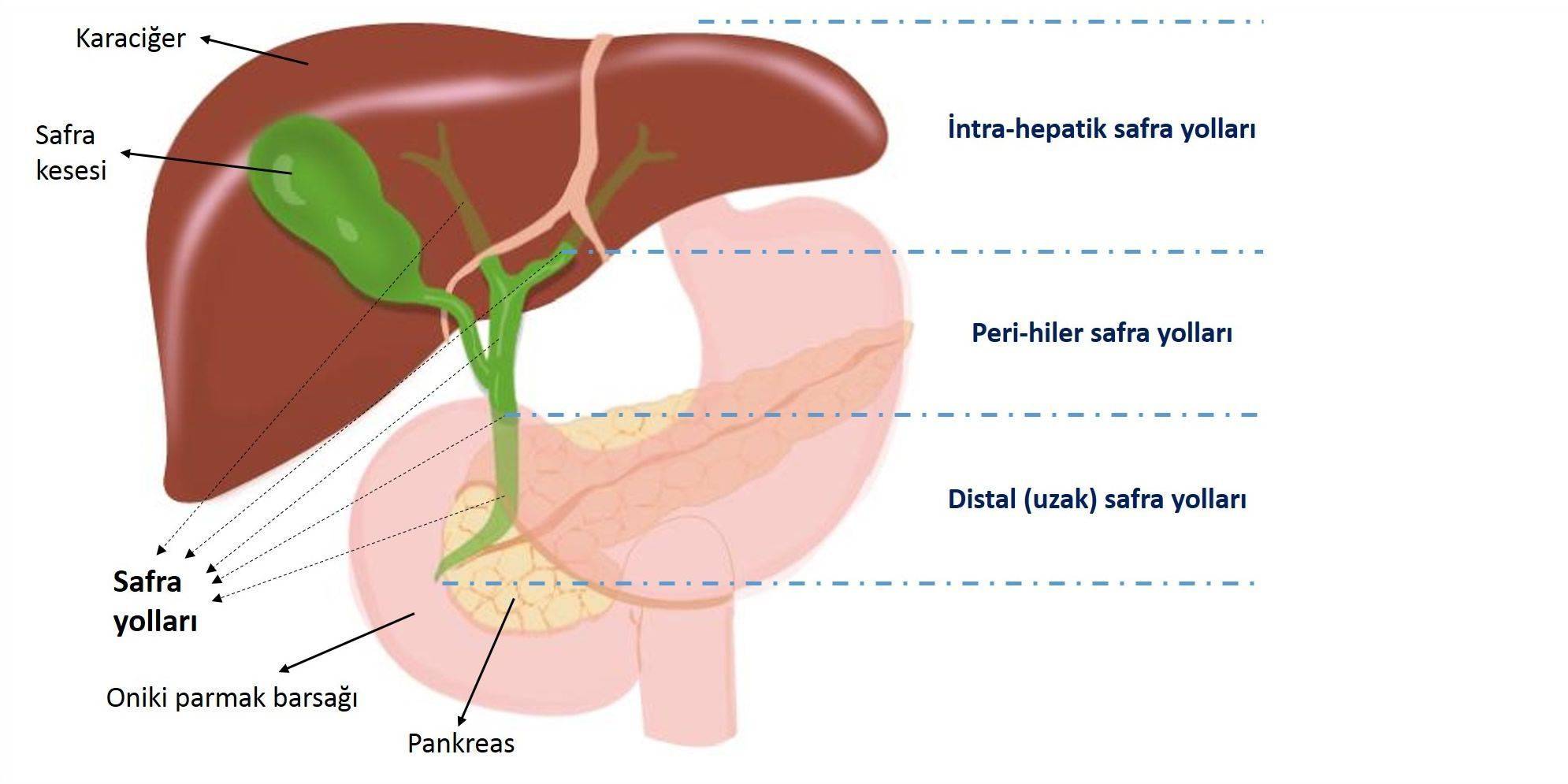
60 hastanın 38'inde (% 63) intrahepatik kolanjiokarsinom; dokuzunda (% 15) ekstrahepatik kolanjiokarsinom ve 13'ünde (% 22) safra kesesi kanseri vardı. Hastaların %78'inde metastatik, %22'sinde bölgesel olarak ilerlemiş kanser vardı. Yaş ortalaması 58,4 idi.
Açık etiketli, bu tek kollu klinik araştırma, Texas Üniversitesi MD Anderson Kanser Merkezi'nde ve Arizona'daki Mayo Clinic'te yapıldı.
Çalışmanın Detayları ve Dikkat Çekici Bulgular
- Başlangıçta, hastalara 21 günlük periyotların 1 ve 8. günlerinde gemsitabin (1000 mg / m2), sisplatin (25 mg / m2) ve nab-paklitaksel (125 mg / m2) verildi. Ancak, ilk 32 hasta hematolojik yan etkiler yaşadığı için 28 hastada dozlar sırasıyla 800, 25 ve 100 mg / m2'ye düşürüldü.
- Kısmi yanıt oranı % 45 ve hastalık kontrol oranı % 84 idi.
- Ciddi (3. derece veya daha yüksek) yan etkiler, hastaların % 58'inde meydana geldi ve dokuz hasta (% 16) çalışmadan çekildi. Nötropeni, 19 hastada (% 33) görüldü ve en yaygın ciddi yan etki idi.
- Çalışmanın yazarlarından Shroff, en ciddi yan etkilerin orijinal yüksek dozları alanlar arasında görüldüğünü ve Şubat 2019'da başlayan faz III çalışmada daha düşük dozların kullanıldığını söyledi.
- Tanı anında tümörü ameliyatla çıkarılamaz safra yolları kanserli bu 60 hastanın 12'sinde kanserin rezektabl (ameliyatla çıkarılabilir) hale geldiği de bildirildi. Bu hastalar çalışmayı yan etki veya kanser ilerlemesine bağlı olarak değil, ameliyat olabildikleri için bıraktılar.
Hastaların % 20'sinin bu üçlü kemoterapi sonucu ameliyat edilebilir hale gelmesi, araştırmacılar tarafından fantastik bir bulgu olarak nitelendirildi.
Shroff, erken sonuçların önerdiği aylarca süren sağkalım katkısının hastalar için paha biçilmez olduğunu ifade etti ve ekledi: "Bu çalışmada, kilometre taşlarını arayan, kızlarının düğününe veya torunlarının doğumuna yetişmeye çalışan hastalarımız vardı. 8 aylık ek sürenin bu etkisi çok derin." dedi.
Araştırmacılar, nab-paklitakseli safra yolları kanserinde test etmeye karar vermelerinin sebebini, yoğun bir tümör mikroçevresine sahip olma özelliği taşıyan pankreas kanserinde nab-paklitakselin etkili olması olarak ifade ettiler. Nab-paklitaksel, tümör mikroçevresini zayıflatıyor gibi görünüyor.
Sonuç olarak, bu faz 2 çalışma her ne kadar kontrol grubu ve rastgele hasta seçim olmayan küçük çaplı bir araştırma olsa da, tarihsel veriler ile karşılaştırıldığında, sağkalım farkı oldukça belirgindir. Bu da yeni başlayan faz 3 çalışma için umutları artırmaktadır.
Rachna T. Shroff, Milind M. Javle, Lianchun Xiao ve ark.
Gemcitabine, Cisplatin, and nab-Paclitaxel for the Treatment of Advanced Biliary Tract Cancers A Phase 2 Clinical Trial.
JAMA Oncology, 18 April 2019.