
Tedaviye Dirençli Hormon Pozitif Meme Kanseri için Yeni Bir İlaç: Elacestrant
CDK4/6 inhibitörleri ve standart hormonal tedavilere direnç gelişmiş ileri evre meme kanserinde yeni bir tedavi seçeneği karşımızda.
Deneysel bir oral selektif östrojen reseptör indirgeyici (SERD) ajan olan elacestrant, östrojen reseptörü pozitif (HR +) olan postmenopozal ileri evre meme kanserli hastalarda ikinci veya üçüncü basamak tedavi olarak uygulandığında, standart tedavi olan tekli endokrin ilaca kıyasla yaşam kaybı ve hastalık ilerlemesi riskini önemli ölçüde azalttı, ve ilerlemesiz sağkalımı artırdı. Bu faz III EMERALD çalışmasın sonuçları, 2021 San Antonio Meme Kanseri Sempozyumu'nda Dr. Aditya Bardia ve meslektaşları tarafından sunuldu.
Metastatik ER pozitif meme kanseri olan hastalar tipik olarak aromataz inhibitörleri veya fulvestrant gibi endokrin tedavisi ile tedavi edilir; bununla birlikte, bazı durumlarda ESR1 geninin mutasyonu nedeniyle bu tedavilere direnç yaygın olarak gelişir. Kas içi enjeksiyonlarla verilen fulvestrant, şu anda meme kanserli hastalar için onaylanmış tek SERD'dir.
ESR1 mutasyonu nedir?
ESR1, östrojen reseptörünü kodlayan bir gendir. Metastatik hormon reseptörü pozitif meme kanserinde hormonal tedavilere bağlı olarak sıklıkla ESR1 geninde mutasyonlar meydana gelir. ESR1 mutasyonları en sık olarak aromataz inhibitörleri altında ilerlemiş meme kanserlerinde görülür.
Massachusetts Genel Kanser Merkezi Meme Kanseri Araştırma Programı Direktörü ve Harvard Tıp Fakültesi'nde görevli Dr. Bardia, "ESR1 mutasyonları olanlar da dahil olmak üzere hormon-pozitif metastatik meme kanserine karşı etkili olan alternatif SERD'lere acilen karşılanmamış bir ihtiyaç var" dedi.
Elacestrant Nedir? Etki Mekanizması Nasıldır?
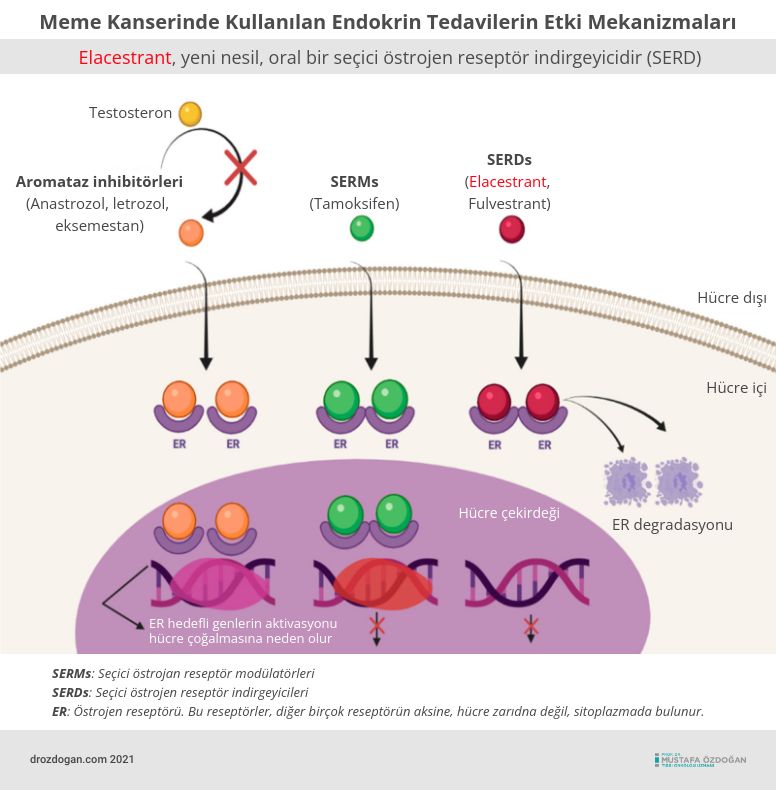
Elacestrant, fulvestranttan farklı olarak oral yoldan uygulanan deneysel bir SERD'dir. Dr. Bardia, fulvestrant ile karşılaştırıldığında elacestrantın daha fazla emilime, gelişmiş farmakokinetiklere ve gelişmiş ER (östrojen reseptörü) inhibisyonuna sahip olduğunu açıkladı. Ek olarak, elacestrant, ER-pozitif meme kanserinin fare modellerinde daha fazla antitümör aktivite göstermiştir göstermiştir. Bir faz I klinik çalışması, elacestrant tedavisinin kabul edilebilir bir güvenlik profiline sahip olduğunu ve ER-pozitif/HER2-negatif metastatik meme kanseri olan, önceden yoğun bir şekilde tedavi görmüş postmenopozal hastalarda anlamlı yanıtlara yol açtığını buldu.
Elacestrant, SERD sınıfından bir diğer hormonal tedavi olan fulvestranta göre kan-beyin bariyerini çok daha kolay geçebilmekte, bu da beyin metastazlı meme kanserli hastalar için uygun bir tedavi seçeneği olabileceğini akla getirmektedir.
Elacestrant'ın mevcut bakım standardı ile nasıl karşılaştırıldığını anlamak için Dr. Bardia ve meslektaşları, faz III EMERALD çalışmasını başlattı. Elacestrant, randomize bir faz III klinik çalışmada incelenen ilk oral SERD'dir.
EMERALD Çalışmasının Detayları
Çalışmaya, metastatik hastalığa sahip olup daha önce kemoterapi almamış, bununla birlikte bir veya iki basamak hormon ve bir CDK4/6 inhibitörü tedavisi almış ve kanseri ilerleyen, ER-pozitif/HER2-negatif metastatik meme kanserli postmenopozal 477 hasta dahil edildi.
Hastalar ya elacestrant ya da standart tedavi (araştırmacının fulvestrant ya da aromataz inhibitörü seçimi) alacak şekilde rastgele deneysel ya da kontrol grubuna atandılar. Hastaların 228'inde mutasyona uğramış ESR1'li tümörler vardı: deneysel kolda 115 ve standart tedavi kolunda 113.
Sonuçlar
- Deneysel koldaki hastaların standart tedavi kolundakilere kıyasla %30 daha düşük yaşam kaybı veya hastalık ilerlemesi riskine sahip olduğu bulundu.
- Tümörleri ESR1 mutasyonları olan hastalar arasında, deneysel koldakilerin yaşam kaybı veya hastalık ilerlemesi riskinde %45'lik bir azalma vardı.
Alt grup analizleri, viseral (iç organ) metastazların varlığı, önceden kaç basamak tedavi alındığı, fulvestrant ile ön tedavi veya coğrafi bölge ne olursa olsun, elacestrantın sonuçları iyileştirdiğini gösterdi.
- 12. ayda, deneysel koldaki hastalar, standart tedavi alan hastalara göre önemli ölçüde daha yüksek progresyonsuz sağkalım oranına sahipti (%22.32'ye karşı %9.42).
- ESR1 mutasyonlu tümörleri olan hastalar arasında, 12 aylık progresyonsuz sağkalım oranları, standart bakım ile tedavi edilen hastalarda %8.19'a kıyasla elacestrant ile tedavi edilenlerde %26.76 idi.
Genel sağkalımın bir ara analizi, ESR1- mutasyona uğramış tümörleri olan hastalar da dahil olmak üzere, elacestran lehine bir eğilim gösterdi.
Yan Etkiler
Tedaviye bağlı hafif (1. veya 2. derece) yan etkiler, bulantı (%25.3'e karşı %8.7), kusma (%11'e karşı %2.6) ve yorgunluk (%11'e karşı %7.9) dahil olmak üzere standart tedaviye kıyasla elacestrant ile tedavi edilen hastalarda daha yaygındı.
Elacestrant koldaki hastaların %7.2'sinde ve standart tedavi kolundaki hastaların %3.1'inde tedaviyle ilgili 3. derece veya daha yüksek yan etkiler gözlenmiştir. Her iki kolda da tedaviye bağlı yaşam kaybı olmadı.
Sonuç
Elacestrant, tümörleri ESR1 mutasyonu yönünden pozitif olan hastalar da dahil olmak üzere ikinci ve üçüncü basamak ayarlarında ER-pozitif/HER2-negatif metastatik meme kanserli hastalarda ilerlemesiz sağkalımda istatistiksel ve klinik olarak anlamlı bir iyileşme gösteren ilk oral SERD'dir. Elacestrant, yönetilebilir ve geri döndürülebilir yan etkilerle iyi tolere edildi. Bu ilaç, bu durumdaki meme kanserli hastalar için yeni tedavi standardı olma potansiyeline sahiptir.
Dr. Bardia, gelecekteki çalışmaların, daha önceki tedavi hatları sırasında ve diğer terapilerle kombinasyon halinde elacestrantın etkinliğini anlamayı hedefleyeceğini kaydetti. Planlı bir faz II denemesi, özellikle beyin metastazı olan hastalar için abemaciclib ile kombinasyon halinde elacestrantın etkisini inceleyecektir.
Bu çalışmanın bir sınırlaması, kayıtlı tüm hastaların önceden bir CDK4/6 inhibitörü ile tedavi görmüş olmasıydı; bu nedenle, önceden CDK4/6 inhibitörü tedavisi görmemiş hastalarda elacestrantın etkinliği bilinmemektedir.
Elacestrant May Improve Outcomes for Postmenopausal Patients With Progressive ER-Positive HER2-Negative Metastatic Breast Cancer. By The ASCO Post Staff. Posted: 12/8/2021






