ALK pozitif 4. evre akciğer kanseri birinci basamak tedavisinde brigatinib-Alunbrig FDA onayı aldı
Alunbrig, Birinci Basamakta FDA Onayı Aldı
22 Mayıs 2020'de, FDA (ABD Gıda ve İlaç İdaresi), anaplastik lenfoma kinaz (ALK) genetik değişimi taşıyan metastatik küçük hücreli dışı akciğer kanseri (KHDAK) tanılı hastaların birinci basamak tedavisi için brigatinib (piyasa adı Alunbrig, firma Takeda) adlı ilacı onayladı.
Eşzamanlı olarak FDA, brigatinib için eşlik eden bir teşhis aracı olarak Vysis ALK Break Apart FISH Prob Kitini de onayladı.
Alunbrig, daha önce 2017'de, krizotinib sonrası kullanım için FDA onayı almıştı.
ALTA 1 çalışması
Daha önce ALK hedefli tedavi almayan ileri evre ALK-pozitif KHDAK olan erişkin hastalarda 1:1 oranında randomize, açık etiketli, çok merkezli bir çalışma olan ALTA 1L adlı klinik araştırmada etkinlik araştırıldı. Deney 275 hastayı rastgele iki kola ayırdı;
- Alunbrig kolunda bulunan 137 hasta ilk ilk hafta günde 1 kez 90 mg ve takiben günde 1 kez 180 Alunbrig aldı;
- Krizotinib kolunda bulunan 138 hasta günde 2 kez 250 mg krizotinib aldı.
Klinik örneklerin bir alt kümesi, Vysis ALK Break Apart FISH Prob Kiti ile geriye dönük olarak hastaların tümörlerini test edildi. Kayıtlı hastaların 239'unun Vysis tanı testi kullanılarak ALK pozitif sonuçları vardı (sonuçlar 20 hasta için negatif ve 16 hasta için mevcut değildi). Çalışmanın ölçmek istediği ana etkililik sonuç ölçütü, kör bir bağımsız inceleme komitesi tarafından değerlendirilen progresyonsuz (ilerlemesiz) sağkalım (PFS) idi. Ek etkililik sonuç ölçümleri genel yanıt oranı olarak belirlendi.
- Alunbrig ile tedavi edilen hastalarda tahmini ortanca progresyonsuz sağkalım süresi 24 ay iken, krizotinib için 11 aydı.
- ALK pozitif ileri evre KHDAK'lı bu hasta grubunda krizotinib yerine Alunbrig kullanımı, hastalığın progrese (ilerleme) olma riskini %51 azalttı (HR 0.49; %95 CI: 0.35, 0.68; p <.0001).
- Onaylanmış genel yanıt oranları sırasıyla %74 ve %62 idi.
Alunbrig ile en sık (≥% 25) görülen yan etkiler ishal, yorgunluk, bulantı, döküntü, öksürük, kas ağrısı, baş ağrısı, hipertansiyon, kusma ve nefes darlığıydı. Önerilen Alunbrig dozu ilk 7 gün boyunca günde bir kez oral yoldan 90 mg'dır; daha sonra günde bir kez ağızdan 180 mg'a çıkar. Alunbrig yemekle birlikte veya yemeksiz alınabilir.
*
Alunbrig Etki Mekanizması Nasıldır?
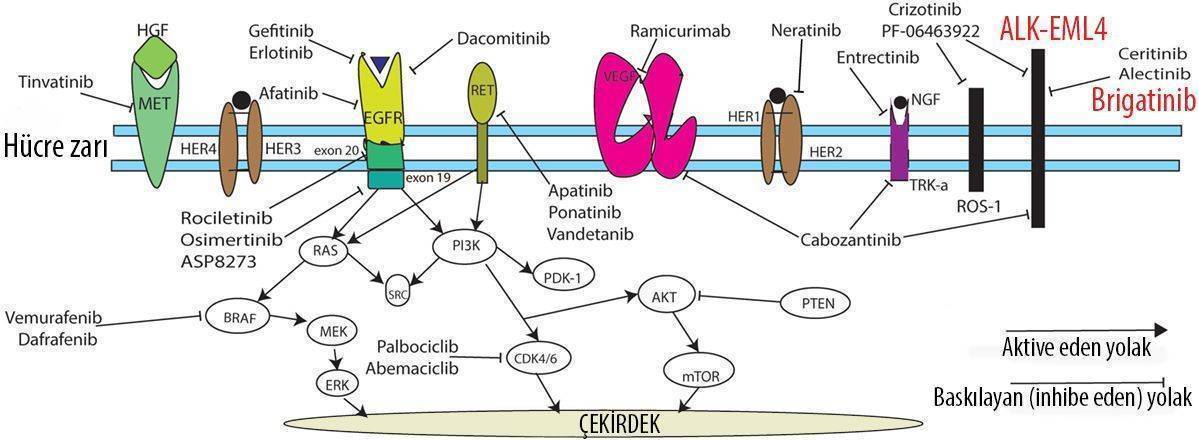
Alunbrig, ALK (anaplastik lenfoma kinaz) baskılayıcı bir ilaçtır. ALK reseptörü, insanlarda ALK geni tarafından kodlanan büyüme ve çoğalmadan sorumlu bir reseptördür. ALK, EML4 ile füzyona uğradığında (birleşme), akciğer kanserini tetikleyebilir. Sigara içmeyenlerde görülen akciğer kanserinin nedenlerinden biri de bu durumdur. Brigatinib bu füzyona uğramış genin aktivitesi baskılar. EML4-ALK füzyon geni küçük hücre dışı akciğer kanserlerinin yaklaşık %5'inden sorumludur. Bu oran az gelebilir, fakat akciğer kanserinin dünya genelinde en sık görülen kanser olduğu düşünülürse, bu oran yılda 70 bin yeni akciğer kanserli hastaya karşılık gelmektedir.
*
Ülkemizde Alunbrig Kullanım Durumu Nedir?
Alunbrig, ülkemizde hem birinci basamak hem de ikinci basamak tedavi olarak SGK (Sosyal Güvenlik Kurumu) tarafından geri ödeme kapsamındadır ve Sağlık Bakanlığı tarafından şu durumlar için ruhsatlandırılmıştır:
- Önceden ALK-Hedefli Tedavi Almamış İleri Evre ALK-Pozitif Küçük Hücreli Dışı Akciğer Kanseri (KHDAK) ALUNBRIG (brigatinib), anaplastik lenfoma kinaz (ALK)-pozitifliği FISH testi ile doğrulanmış ilerlemiş küçük hücreli dışı akciğer kanseri (KHDAK) olan hastaların tedavisinde progresyona kadar kullanımı endikedir.
- Önceden Krizotinib Tedavisi Almış ALK-Pozitif İleri Evre veya Metastatik Küçük Hücreli Dışı Akciğer Kanseri (KHDAK) ALUNBRIG (brigatinib), krizotinib ile önceden tedavi edilmiş anaplastik lenfoma kinaz (ALK)- pozitifliği FISH testi ile doğrulanmış ileri evre veya metastatik küçük hücreli dışı akciğer kanseri (KHDAK) olan hastaların tedavisinde progresyona kadar kullanımı endikedir.
*
FDA approves brigatinib for ALK-positive metastatic NSCLC.
fda.gov - 22 May 2020