
EGFR Pozitif Akciğer Kanseri Tedavisinde Yenilikler – 2023
Akciğer kanseri, artık bir tek hastalık olarak değil, çeşitliliğiyle dikkat çeken bir "hastalık grupları" topluluğu olarak anlaşılmaktadır. Her yıl yaklaşık 2 milyon yeni vaka ile dünya genelinde meme kanseri ile birlikte en sık görülen iki kanserden biri olmasına rağmen, akciğer kanseri birçok farklı alt türü barındıran karmaşık bir yapıya sahiptir. Bu bağlamda, akciğer kanseri hem yaygın hem de nadir görülen hastalık türlerini kapsayan, geniş bir yelpazede ele alınması gereken bir sağlık sorunu olarak tanımlanabilir.
Akciğer kanserlerinin yaklaşık %85'i, küçük hücreli dışı akciğer kanseri (KHDAK) olarak bilinir. KHDAK, kendi içinde onlarca farklı alt türe ayrılmakta ve bu alt türler, günümüzde tümörün genomik özelliklerine göre sınıflandırılmaktadır. Bu hassas onkoloji mümkün kılar, yani tedavi yaklaşımlarının daha hedef odaklı ve kişiselleştirilmiş olmasını sağlar.
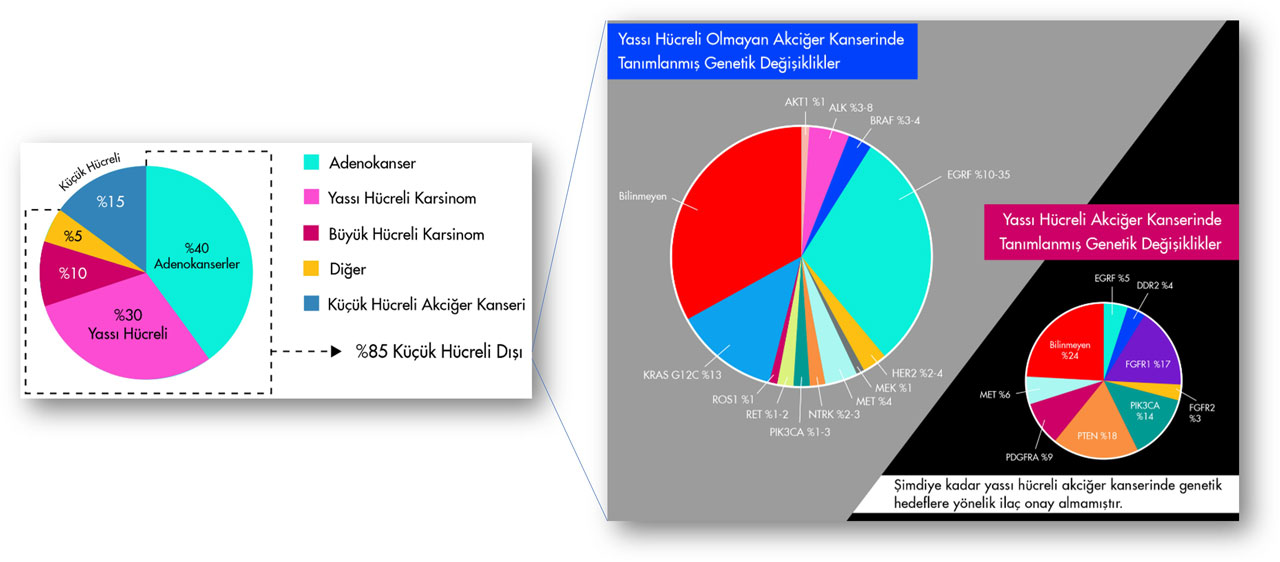
EGFR genetik değişimine sahip akciğer kanserleri, KHDAK'lerin önemli bir alt grubunu oluşturur ve bu kanserler, Epidermal Büyüme Faktörü Reseptörü (EGFR) genindeki mutasyonlarla karakterize edilir. EGFR mutasyonları, kanser hücrelerinin büyümesi ve yayılması üzerinde kritik bir rol oynar. Bu mutasyonlar, özellikle Asya kökenli kişilerde ve sigara içmeyen hastalarda daha yaygındır. EGFR'deki mutasyonlar arasında en sık rastlananlar ekzon 19 deleksiyonları ve ekzon 21 L858R nokta mutasyonlarıdır. Bu mutasyonların varlığı, EGFR tirozin kinaz inhibitörlerine (TKI) karşı duyarlılığı gösterir ve hastaların bu tedavilere iyi yanıt vermesini sağlar.
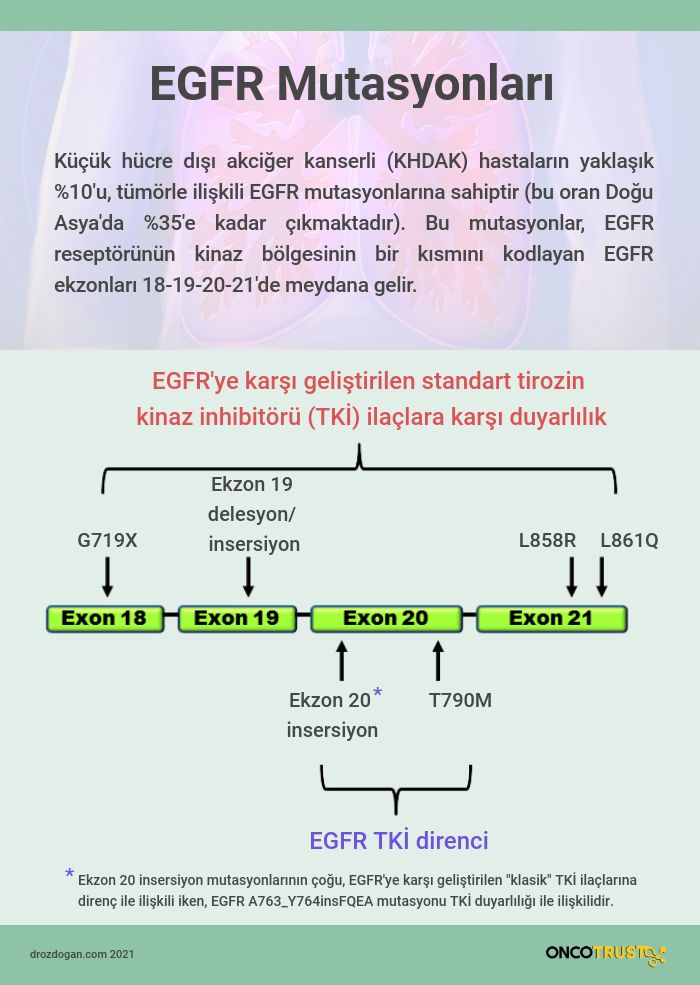
Zamanla EGFR mutasyonlu hastaların çoğu ilaca direnç geliştirir, bu da tedavi stratejilerinin sürekli olarak geliştirilmesini gerektirir. T790M gibi sekonder mutasyonlar, bu direncin en yaygın nedenlerinden biridir ve farklı tedavi yaklaşımlarını gerektirir. EGFR mutasyonlarının çeşitliliği ve bunların tedaviye olan etkileri, bu kanser alt türünün yönetiminde bireyselleştirilmiş tedavi yaklaşımlarının önemini vurgular. Bu nedenle, EGFR mutasyonlu KHDAK hastalarının tedavisi, mutasyonun tipi ve hastanın genel sağlık durumu göz önünde bulundurularak, kişiselleştirilmiş bir yaklaşım gerektirir.
Dikkat Çekici Güncel Çalışmalar
Son dönemde gerçekleştirilen birkaç faz 3 çalışma, EGFR genetik değişimine sahip KHDAK tedavisindeki yaklaşımlarımızı önemli ölçüde güncellemiştir. Bu çalışmalar, tedavi stratejilerinin sürekli evrim geçirdiğini ve kanser tedavisinde kişiselleştirilmiş tıbbın giderek artan önemini göstermektedir.
MARIPOSA çalışması, ileri evre EGFR mutasyonlu KHDAK hastaları için amivantamab ve lazertinib kombinasyonunu yeni birinci basamak tedavi standardı olarak öne çıkarıyor.
MARIPOSA-2 çalışması, osimertinib tedavisi sonrası ilerleyen hastalığı olan aynı hasta grubu için amivantamab ve kemoterapinin yeni bir tedavi standardı olarak değerlendirilmesini tavsiye ediyor.
PAPILLON çalışması, EGFR ekzon 20 insersiyo (ekleme) mutasyonlarına sahip KHDAK hastalarının birinci basamak tedavisi için amivantamab ve kemoterapi kombinasyonunu yeni bir tedavi standardı olarak gösteriyor.
Bu çalışmalar ESMO Kongresi 2023'te sunuldu.
MARIPOSA: Amivantamab Artı Lazertinib vs Osimertinib
MARIPOSA çalışmasında, amivantamab ve lazertinib, daha önce tedavi edilmemiş ileri evre EGFR mutasyonlu KHDAK hastalarında osimertinib monoterapisi ile karşılaştırıldığında ilerlemesiz sağkalımı (PFS) önemli ölçüde iyileştirdi.
Amivantamab, bir EGFR ve MET reseptör tirozin kinaz inhibitorüdür; hücre yüzeyindeki bu reseptörleri hedef alarak tümör hücrelerinin büyümesini ve çoğalmasını engeller. Lazertinib ise, özellikle EGFR mutasyonlarını hedef alan bir tirozin kinaz inhibitörüdür ve bu yolla tümör hücrelerinin büyümesini baskılar.
Amivantamab, Mayıs 2021'de ABD Gıda ve İlaç Dairesi (FDA) tarafından, daha önce tedavi edilmiş EGFR ekzon 20 mutasyon pozitif KHDAK hastalarında hızlandırılmış onay almıştır. Lazertinib için ise daha önce FDA onayı almamıştır.
Lazertinib, hem normal hem de yeni nesil bir anti-EGFR (Epidermal Büyüme Faktörü Reseptörü) ilacı olarak işlev görürken, amivantamab ise özellikle EGFR direnci ve EGFR ekzon 20 inserisyon mutasyonlarına karşı geliştirilmiş bir ilaçtır. Bu iki ilacın kombinasyonu, KHDAK tedavisinde hem anti-EGFR etkinliğini artırmayı hem de anti-EGFR tedavilere karşı gelişebilecek direnci baştan kırmayı amaçlar.
Çalışma, daha önce tedavi almamış, EGFR mutasyonlu, lokal olarak ileri veya metastatik KHDAK olan 1074 hastayı kaydetti. Hastalar rastgele amivantamab artı lazertinib (429 hasta), sadece osimertinib (429 hasta) veya sadece lazertinib (216 hasta) almak üzere gruplara ayrıldı.
Ortanca takip süresi 22 aydı. Çalışmanın birincil sonlanım noktası, kör bağımsız merkezi inceleme tarafından değerlendirilen progresyonsuz (ilerlemesiz) sağkalım süresi (PFS) idi.
Sonuçlar
- Amivantamab artı lazertinib ile ortalama PFS 23.7 ay ve osimertinib ile 16.6 aydı (hazard oranı [HR], 0.70; %95 CI, 0.58-0.85; P <.001).
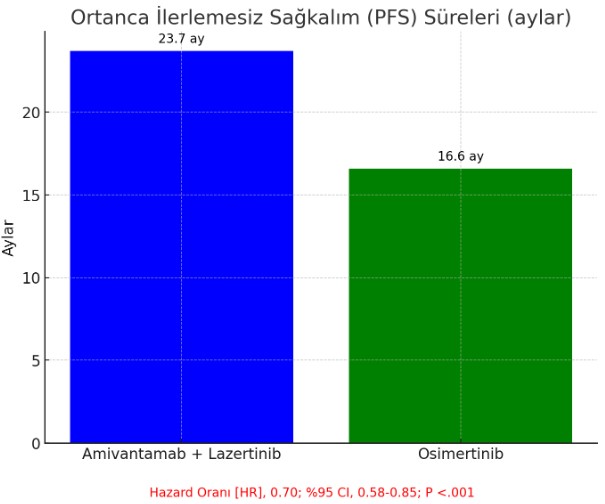
- 12 aylık PFS oranı sırasıyla %73 ve %65 idi.
- 24 aylık PFS oranı sırasıyla %48 ve %34 idi.
- Beyin dışı PFS ortalaması, amivantamab artı lazertinib ile 27.5 ay ve osimertinib ile 18.5 aydı (HR, 0.68; %95 CI, 0.56-0.83; P <.001). 24 aylık beyin dışı PFS oranı sırasıyla %53 ve %38 idi.
- Genel yanıt oranı, amivantamab artı lazertinib ile %86 ve osimertinib ile %85 idi.
- Yanıt süresinin ortanca süresi sırasıyla 25.8 ay ve 16.8 aydı.
- Birinci basamak tedavi sonrası PFS'nin (PFS2) 24 aylık oranı, amivantamab artı lazertinib ile %72 ve osimertinib ile %64 idi (HR, 0.75; %95 CI, 0.58-0.98; P =.03).
- Genel sağkalım verileri olgunlaşmamış olmasına rağmen, amivantamab artı lazertinib ile iyileşme eğilimi vardı. 24 aylık genel sağkalım oranı, amivantamab artı lazertinib ile %74 ve osimertinib ile %69 idi (HR, 0.80; %95 CI, 0.61-1.05; P =.11).
Bu sonuçlar, ileri evre EGFR mutasyonlu KHDAK hastaları için amivantamab artı lazertinibin yeni birinci basamak standart tedaviyi temsil ettiğini öne sürüyor.
Ancak, amivantamab-lazertinib kolunda osimertinib koluna göre 3. derece veya daha yüksek tedaviye bağlı advers olayların (AE'ler) daha yaygındır: sırasıyla %75 ve %43.
Tedaviyle ilişkili advers olayların tedaviyi bırakmaya yol açtığı hastaların oranı, kombinasyon kolunda %10 ve osimertinib kolunda %3 idi. İshal, osimertinib alan hastalarda daha sık görüldü, ancak paronişi, döküntü ve hipoalbüminemi amivantamab artı lazertinib ile daha yaygındı.
Özel ilgi gösterilen bir advers olay venöz tromboembolizm (VTE) idi, bu da amivantamab-lazertinib kolundaki hastaların %37'sinde ve osimertinib kolundaki hastaların %9'unda görüldü. VTE nedeniyle tedaviyi bırakma oranı, kombinasyon kolunda %3 ve osimertinib kolunda %0.5 idi.
Amivantamab-lazertinib kombinasyonu uygulanan hastaların çalışma süresince sadece %1'i antikoagülan kullanırken, osimertinib grubundaki hastaların hiçbiri antikoagülan kullanmamıştı. İlginç bir şekilde, amivantamab-lazertinib grubunda görülen venöz tromboembolizm (VTE) vakalarının çoğu tedavinin ilk dört ayı içinde meydana geldi. Bu bulgu, devam eden denemelerde amivantamab ve lazertinib kombinasyonu için ilk dört ay boyunca profilaktik doz antikoagülasyon kullanımının önerilmesine yol açtı.
Bu tedavinin hasta yaşam kalitesi üzerindeki etkilerini daha iyi anlamak önemlidir, özellikle de uzun süreli bir tedavi süreci göz önünde bulundurulduğunda. Yine de,amivantamab artı lazertinib tedavisinin daha yüksek oranda tedavi kesilmesine yol açtığı gözlemlendi. Bu durum, amivantamabın erken kesilmesinin tedavi sonuçları üzerindeki etkisini araştırmayı gerekli kılmaktadır. Özellikle birinci basamak tedavi süresince amivantamabın devam ettirilip ettirilmediğinin, tedavinin genel başarısı üzerinde önemli bir etkisi olabilir. Bu nedenle, tedavi süreçlerinde bu faktörlerin dikkatle değerlendirilmesi ve izlenmesi önem taşımaktadır.
MARIPOSA-2: Osimertinib Sonrası Amivantamab Artı Kemoterapi
MARIPOSA-2 çalışmasında, daha önce osimertinib tedavisi almış ileri evre EGFR mutasyonlu KHDAK hastalarında, amivantamab artı kemoterapi, yalnızca kemoterapiye kıyasla sonuçları iyileştirdi.
Çalışma, osimertinib monoterapisi sonrası hastalığı ilerleyen lokal ileri veya metastatik EGFR mutasyonlu KHDAK hastalarını kaydetti.
Hastalar rastgele olarak,
- karboplatin artı pemetreksed kemoterapisi (263 hasta),
- amivantamab artı kemoterapi (131 hasta) veya
- amivantamab artı lazertinib ve kemoterapi (263 hasta) almak üzere atandı.
Başlangıçta, amivantamab artı lazertinib ve kemoterapi alan hastalar, tedavilerini eş zamanlı olarak aldılar. Ancak, bu hastalarda artan hematolojik toksisiteler, araştırmacıları rejimi değiştirmeye yöneltti, böylece lazertinib kemoterapinin tamamlanmasından sonra başlatıldı. Amivantamab-lazertinib-kemoterapi kolundaki 263 hastanın 166'sı eş zamanlı lazertinib aldı ve 97'si kemoterapiden sonra lazertinib aldı.
Sonuçlar
- Ortanca takip süresi 8.7 aydı. İkili birincil son nokta, amivantamab-kemoterapi ile kemoterapiye kıyasla PFS ve amivantamab-lazertinib-kemoterapi ile kemoterapiye kıyasla PFS idi.
- Ortanca PFS, kemoterapi ile 4.2 ay, amivantamab-kemoterapi ile 6.3 ay (HR, 0.48; %95 CI, 0.36-0.64; P <.001) ve amivantamab-lazertinib-kemoterapi ile 8.3 aydı (HR, 0.44; %95 CI, 0.35-0.56; P <.001).
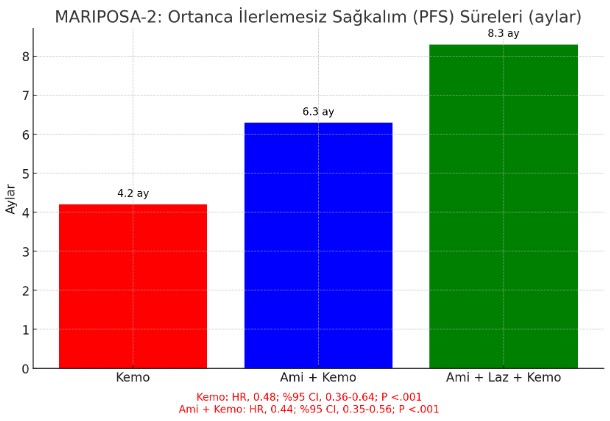
- Ortanca intrakraniyal PFS, kemoterapi ile 8.3 ay, amivantamab-kemoterapi ile 12.5 ay (HR, 0.55; %95 CI, 0.38-0.79; P =.001) ve amivantamab-lazertinib-kemoterapi ile 12.8 aydı (HR, 0.58; %95 CI, 0.44-0.78; P <.001).
- Genel Yanıt Oranı, kemoterapi ile %36, amivantamab-kemoterapi ile %64 (P <.001) ve amivantamab-lazertinib-kemoterapi ile %63 idi (P <.001). Yanıt süresinin ortanca süresi sırasıyla 5.6 ay, 6.9 ay ve 9.4 aydı.
- Amivantamab-kemoterapi ile genel sağkalım üzerinde iyileşme eğilimi vardı (HR, 0.77; %95 CI, 0.49-1.21), ancak amivantamab-lazertinib-kemoterapi ile böyle bir eğilim yoktu (HR, 0.96; %95 CI, 0.67-1.35).
1. derece veya daha yüksek tedaviye bağlı advers olayların oranı, amivantamab-lazertinib-kemoterapi kolunda %92, amivantamab-kemoterapi kolunda %72 ve kemoterapi kolunda %48 idi.
Amivantamab-lazertinib-kemoterapi alan hastalar, amivantamab artı kemoterapi alan hastalara (sırasıyla %45, %15 ve %10) veya yalnızca kemoterapi alan hastalara (sırasıyla %21, %9 ve %0) göre daha yüksek oranlarda 3. derece veya daha yüksek nötropeni (%55), trombositopeni (%37) ve döküntü (%15) yaşadılar.
Bu sonuçlar, EGFR mutasyonlu küçük hücreli olmayan akciğer kanseri (KHDAK) hastaları için, özellikle osimertinib tedavisi sonrası hastalık ilerlemesi gösterenlerde, amivantamab artı kemoterapinin yeni bir standart tedavi olarak değerlendirilmesi gerektiğini gösteriyor. Ancak, gözlemlenen toksisite, özellikle amivantamab ve lazertinib kombinasyonu ile kemoterapinin aynı anda verilmesinin önerilmemesine neden oluyor. Amivantamab artı kemoterapi ve amivantamab-lazertinib-kemoterapi rejimleri, EGFR mutasyonlu KHDAK tedavisinde yeni tedavi seçenekleri olarak karşımıza çıkıyor.
Bu yeni tedavi yöntemlerinin, özellikle dermatolojik ve hematolojik toksisite gibi meydan okumaları da beraberinde getirdiği görülüyor. Bu nedenle, hasta seçimi bu tedavi rejimlerinde kritik bir öneme sahip olacak. Yine de bu yeni tedavi rejimlerinin FDA onayı alması ve genel sağkalım verilerinin olgunlaşmasına kadar, osimertinib tedavisi sonrası ilerleme gösteren çoğu KHDAK hastası için kemoterapi, tercih edilen tedavi rejimi olmaya devam edecektir. Bu durum, KHDAK tedavisinde sürekli bir gelişme ve değerlendirme sürecinin önemini vurgulamaktadır.
PAPILLON Çalışması: EGFR Ekzon 20 İnsersiyo Mutasyonlu KHDAK’de Amivantamab artı Kemoterapi
Amivantamab, platin bazlı kemoterapi sırasında veya sonrasında hastalığı ilerleyen EGFR ekzon 20 inserisyonlarına sahip ileri evre küçük hücreli olmayan akciğer kanseri (KHDAK) hastalarının tedavisi için onaylanmıştır. Faz 1 verileri, amivantamab ve karboplatin-pemetreksed (kemoterapi) kombinasyonunun güvenliğini ve antitümör aktivitesini göstermiştir. Bu kombinasyon tedavisi hakkında ek verilere ihtiyaç duyulmaktadır.
Faz 3, uluslararası, randomize PAPILLON çalışmasında, daha önce sistemik tedavi almamış EGFR ekzon 20 inserisyo mutasyonlarına sahip ileri evre KHDAK hastalarını, intravenöz amivantamab artı kemoterapi (amivantamab-kemoterapi) veya sadece kemoterapi almak üzere 1:1 oranında gruplara atandı. Birincil sonuç, kör bağımsız merkezi inceleme göre progresyonsuz sağkalım (PFS) idi. Kemoterapi grubundaki hastaların hastalığı ilerlediğinde, amivantamab monoterapisi almasına izin verildi.
Sonuçlar
- Toplamda 308 hasta randomize edildi (amivantamab-kemoterapi almak için 153, sadece kemoterapi almak için 155).
- Progresyonsuz sağkalım, amivantamab-kemoterapi grubunda kemoterapi grubuna göre anlamlı derecede daha uzundu (ortanca, sırasıyla 11.4 ay ve 6.7 ay; hastalık ilerlemesi veya yaşam kaybı için tehlike oranı, 0.40; %95 güven aralığı [CI], 0.30-0.53; P<0.001).

- 18 ayda, progresyonsuz sağkalım, amivantamab-kemoterapi grubundaki hastaların %31'inde ve kemoterapi grubundaki hastaların %3'ünde bildirildi.
- Ara genel sağkalım analizinde (%33 olgunluk), amivantamab-kemoterapi ile kemoterapiye kıyasla yaşam kaybı için tehlike oranı 0.67 idi (%95 CI, 0.42-1.09; P=0.11).
Amivantamab-kemoterapi ile ilişkili baskın advers olaylar, geri dönüşümlü hematolojik ve EGFR ile ilgili toksik etkilerdi; hastaların %7'si advers reaksiyonlar nedeniyle amivantamab tedavisini bıraktı.
Sonuç olarak bu çalışmada, amivantamab-kemoterapi kullanımının, EGFR ekzon 20 inserisyonlarına sahip ileri evre KHDAK hastalarının birinci basamak tedavisinde, kemoterapiye göre üstün etkililik sağladığı görüldü.
Osimertinibin Beyin Metastazları Üzerine Etkisi: FLAURA2 Çalışması
EGFR mutasyonlu ileri evre KHDAK hastalarında birinci basamak tedavi olarak osimertinibin beyin metastazları üzerindeki etkinliğini, FLAURA2 çalışmasında değerlendirildi. Çalışma, özellikle beyin metastazı olan hastalarda osimertinib ve kemoterapi kombinasyonunun osimertinib monoterapisi ile karşılaştırılmasını içermektedir.
Hastalar, osimertinib artı platin-pemetreksed (kombinasyon) veya sadece osimertinib monoterapisi (monoterapi) alacak şekilde rastgele atandı. Hastalığın ilerlemesine veya tedavinin kesilmesine kadar tedavi sürdürüldü. Tüm hastalar için başlangıçta ve ilerlemede beyin taramaları yapıldı ve beyin metastazı olan hastalar için ilerlemeye kadar düzenli değerlendirmeler yapıldı.
Sonuçlar
Başlangıçta çalışmaya rastgele dahil edilen 118 hasta (osimertinib ve kemoterapi kombinasyonu grubu) ve 104 hasta (sadece osimertinib monoterapi grubu) en az bir ölçülebilir veya ölçülemeyen beyin metastazına sahipti. Bu hastalar, çalışmanın Beyin Metastazı Tam Analiz Seti'ne (cFAS) dahil edildi. Bu grup içinde, en az bir ölçülebilir hedef beyin metastazına sahip olan 40 hasta (kombinasyon grubu) ve 38 hasta (monoterapi grubu) ise Yanıt Değerlendirilebilir Beyin Metastazı Seti'ne (cEFR) dahil edildi.
- cFAS grubunda, beyin metastazının ilerlemesi veya yaşam kaybı riski için tehlike oranı (Hazard Ratio, HR) 0.58 olarak belirlendi (%95 Güven Aralığı [CI], 0.33-1.01).
- Beyin metastazı olmayan hastalarda, beyin metastazının ilerlemesi veya yaşam kaybı riski için HR 0.67 olarak hesaplandı (%95 CI, 0.43-1.04).
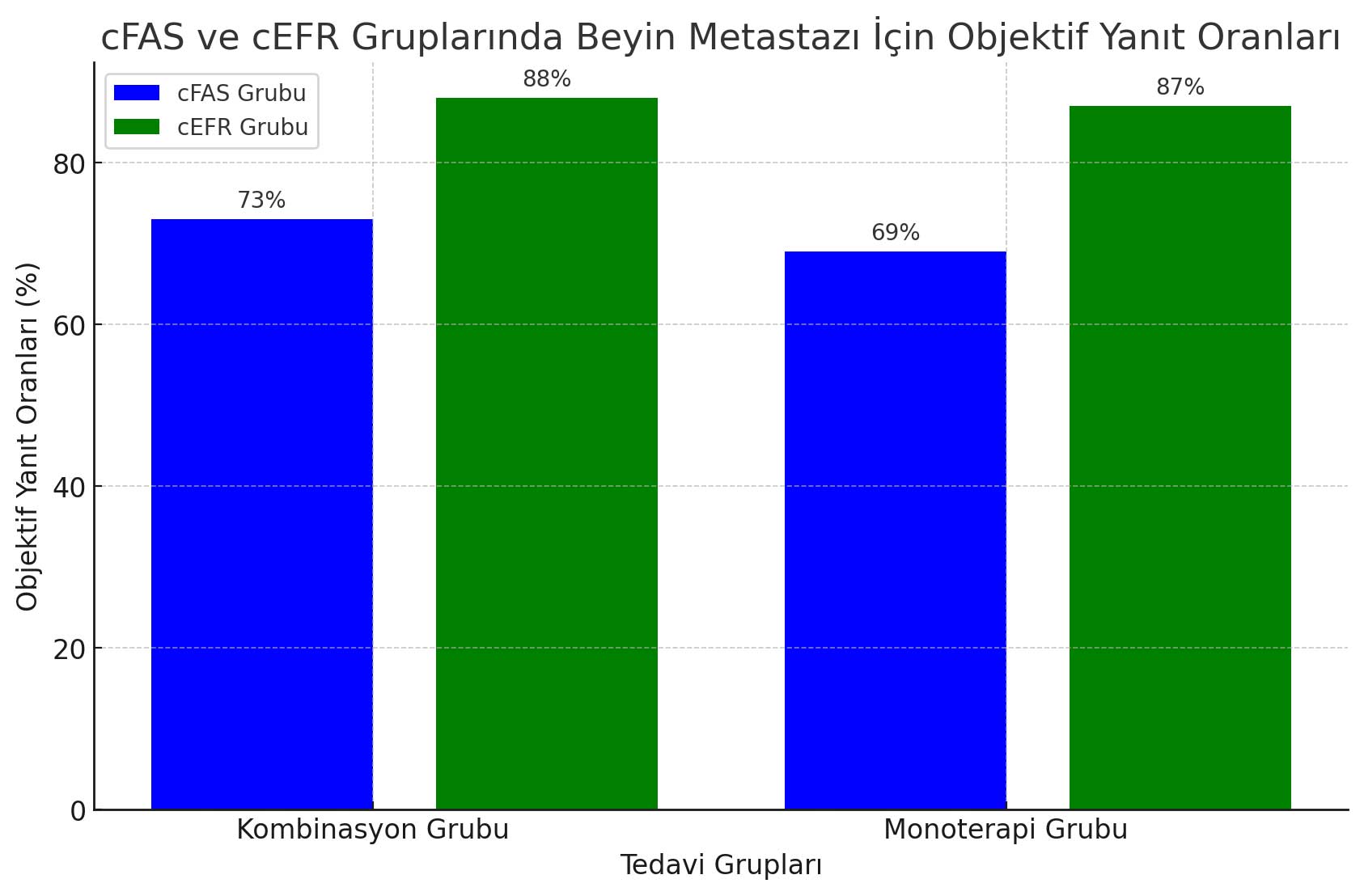
- cFAS grubunda beyin metastazı için belirlenen objektif yanıt oranları (ORR; %95 CI) kombinasyon grubunda %73 (64-81) ve monoterapi grubunda %69 (59-78) olarak saptandı. Bu hastaların %59'u (kombinasyon grubu) ve %43'ü (monoterapi grubu) beyin metastazında tam yanıt gösterdi.
- cEFR grubunda ise beyin metastazı için objektif yanıt oranları (ORR; %95 CI) kombinasyon grubunda %88 (73-96), monoterapi grubunda ise %87 (72-96) olarak belirlendi. Bu grubun %48'i (kombinasyon grubu) ve %16'sı (monoterapi grubu) beyin metastazında tam yanıt gösterdi.
Sonuç olarak, osimertinib ile birlikte platin-pemetreksed kombinasyonunun, osimertinib monoterapisi ile kıyaslandığında, beyin metastazı varlığına bakılmaksızın merkezi sinir sistemi (CNS) üzerindeki etkinliğini artırdığı ve beyin metastazının ilerlemesini geciktirdiği görülmüştür. Bu bulgular, özellikle beyin metastazı olan EGFR mutasyonlu ileri evre KHDAK hastaları için bu kombinasyon tedavisinin birinci basamak tedavi seçeneği olarak önerilmesini destekler niteliktedir. Bu çalışmanın sonuçları, EGFR mutasyonlu ileri evre KHDAK hastalarının tedavisinde yeni bir dönüm noktası oluşturabilir ve özellikle beyin metastazı olan hastalar için önemli bir tedavi seçeneği sunar.
*
Görselin açıklaması: Yazının görseli ChatGPT 4.0 tarafından şu komut ile oluşturulmuştur: "Bir adamın güzel bir manzarada yürüyüşünü gösteren görüntü. Işığın ve havanın etkilerini canlı, ressam fırça darbeleriyle yakalayan bir stil."
1. Cho BC, Felip E, Spira AI, et al. Amivantamab plus lazertinib vs osimertinib as first-line treatment in patients with EGFR-mutated, advanced non-small cell lung cancer (NSCLC): Primary results from MARIPOSA, a phase III, global, randomized, controlled trial. Presented at ESMO Congress 2023. Oct. 20-24, 2023. Madrid, Spain. Abstract LBA14.
2. Passaro A, Cho BC, Wang Y, et al. Amivantamab plus chemotherapy (with or without lazertinib) vs chemotherapy in EGFR-mutated advanced NSCLC after progression on osimertinib: MARIPOSA-2, a phase III, global, randomized, controlled trial. Presented at ESMO Congress 2023. Oct. 20-24, 2023. Madrid, Spain. Abstract LBA15.
3. Girard N, Park K, Tang K, et al. Amivantamab plus chemotherapy vs chemotherapy as first-line treatment in EGFR exon 20 insertion-mutated advanced non-small cell lung cancer (NSCLC): Primary results from PAPILLON, a randomized phase III global study. Presented at ESMO Congress 2023. Oct. 20-24, 2023. Madrid, Spain. Abstract LBA5.
4. Zhou C, Tang KJ, Cho BC, Liu B, Paz-Ares L, Cheng S, Kitazono S, Thiagarajan M, Goldman JW, Sabari JK, Sanborn RE, Mansfield AS, Hung JY, Boyer M, Popat S, Mourão Dias J, Felip E, Majem M, Gumus M, Kim SW, Ono A, Xie J, Bhattacharya A, Agrawal T, Shreeve SM, Knoblauch RE, Park K, Girard N; PAPILLON Investigators. Amivantamab plus Chemotherapy in NSCLC with EGFR Exon 20 Insertions. N Engl J Med. 2023 Oct 21. doi: 10.1056/NEJMoa2306441. Epub ahead of print. PMID: 37870976.
5. Pasi A. Jänne, et al. CNS Efficacy of Osimertinib With or Without Chemotherapy in Epidermal Growth Factor Receptor–Mutated Advanced Non–Small-Cell Lung Cancer. DOI: 10.1200/JCO.23.02219 Journal of Clinical Oncology. Published online December 02, 2023.






