
Ürotelyal (Mesane ve Üreter) Kanser Tedavisinde Ayakta Alkışlanan Çalışma
Yıllarca süren araştırmalar ve klinik çalışmalar sonunda, bilim insanları ve doktorlar nihayet ürotelyal (mesane ve üreter) kanser için etkili yeni bir tedavi kombinasyonu ortaya koydular.
ESMO (Avrupa Tıbbi Onkoloji Derneği) 2023 Kongresi'nin en dikkat çekici sunumu, enfortumab vedotin (Padcev) ve pembrolizumab (Keytruda) kombinasyonunun, ileri evre ürotelyal kanserin birinci basamak tedavisinde yeni bir standart haline geldiğini ortaya koyan, EV-302/KEYNOTE-A39 adlı bir faz-3 çalışma idi. Bu sunum gerçekleşirken ESMO Kongresi'ndeydim ve sunum sonrasında yaklaşık 5 dakika boyunca ayakta alkışlanması oldukça etkileyiciydi.
Bu gelişme, ürolojik kanser tedavisinde önemli bir dönüm noktası olarak görülüyor ve bu kombinasyonun, tedavi akışlarını kökten değiştirebileceği düşünülüyor.
Ürotelyal kanserlerin en sık görülen alt türü mesane (idrar torbası) kanseridir. Mesane kanseri 2020 Türkiye Kanser İstatistiklerine göre 10.426 vaka ile erkekler arasında en sık görülen 4. kanser türü ve 1.772 vaka ile kadınlar arasında ise en sık görülen 14. kanser türüdür. Erkeklerdeki toplam yeni kanser vakalarının yaklaşık %7'si, kadınlardaki vakaların ise yaklaşık %2'si mesane kanseridir. Mesane kanserli hastaların yaklaşık %30'u tanı anında bölgesel ileri veya metastatik evrede bulunur.
Daha önce 3 Nisan 2023'te, platin-bazlı kemoterapiye uygun olmayan ileri evre ürotelyal kanserlerin birinci basamak tedavisi için enfortumab vedotin ve pembrolizumab kombinasyonu, EV-103/KEYNOTE-869 çalışması ile hızlandırılmış FDA onayı almıştı.
Enfortumab Vedotin + Pembrolizumab, Kemoterapi ile Elde Edilen Sonuçları İkiye Katladı
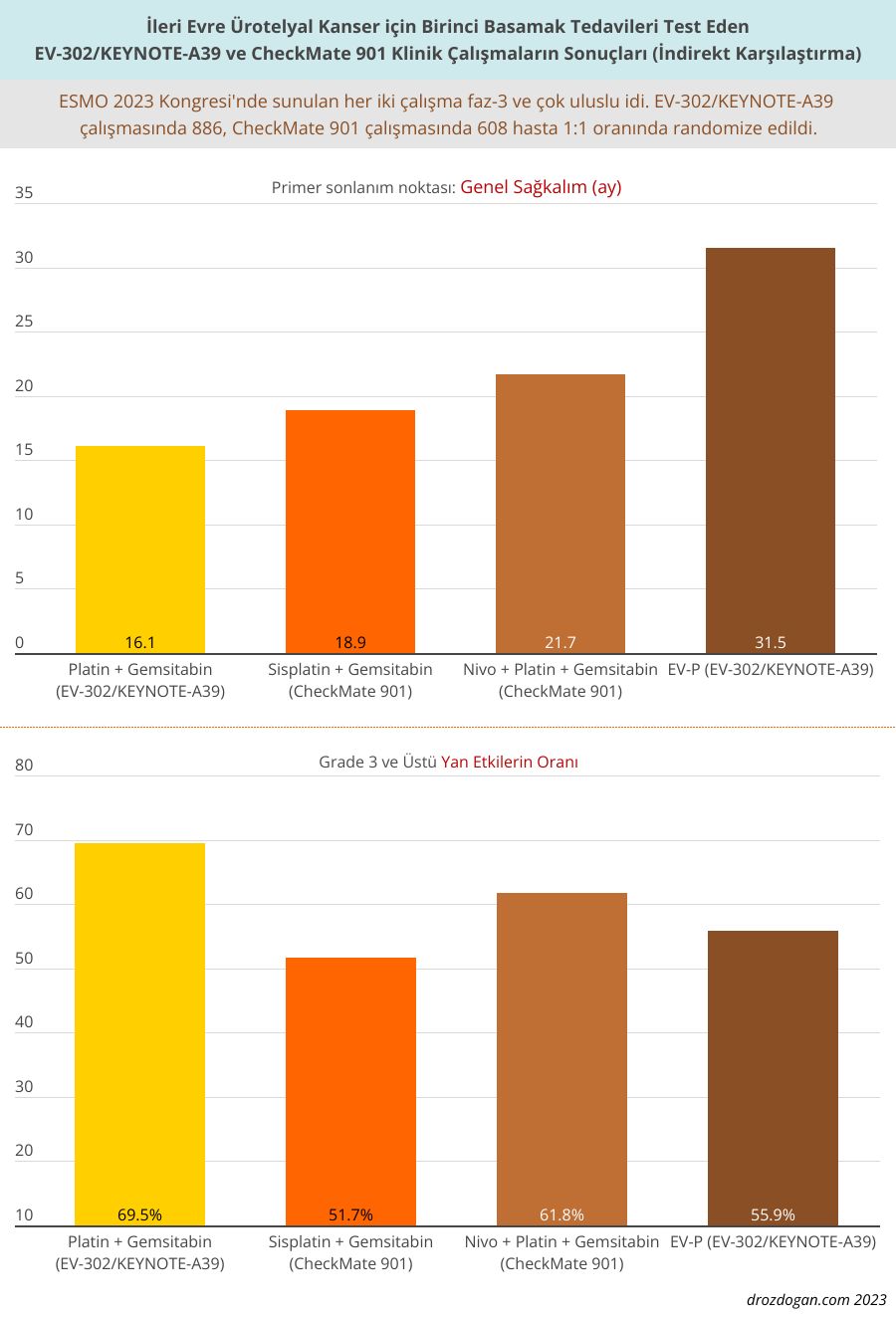
Bu kombinasyon, 442 denek üzerinde yapılan testlerde 31,5 aylık ortanca genel sağkalım ile mevcut bakım standardı olan platin-tabanlı kemoterapiyi belirgin bir şekilde geride bıraktı. Bu durum, gemcitabin ile cisplatin veya karboplatin alan 444 denek üzerinde yapılan testlerde kaydedilen 16,1 aylık ortanca genel sağkalıma kıyasla, yaşam kaybı riskinde %53'lük bir azalma anlamına gelmektedir (P < .00001).
Kemoterapinin kaldırılması, yeni kombinasyonun 3. derece veya daha yüksek yan etkileri önemli ölçüde azaltmasını sağladı.
Bu, ilk basamak tedavide genel sağkalım için kemoterapiyi aşmayı başardığımız ilk kezdir. Enfortumab vedotin ile pembrolizumab kombinasyonu, 4. evre solid (doku/organ kaynaklı) kanserde daha önce hiç rastlanmamış bir %30 remisyon oranı sundu (Remisyon, bir hastalığın belirtilerinin ortadan kalktığı ve hastalığın ilerlemesinin durduğu bir dönemi ifade eder).
Bu gelişme, EV-302/KEYNOTE-A39 çalışmasının hemen ardından sunulan ve genel sağkalımda standart platin tabanlı kemoterapiye kıyasla iyileşme gösteren bir diğer çalışma olan CheckMate 901'i geride bıraktı.
CheckMate 901 çalışmasında, kemoterapiyi tamamen iptal etmek yerine nivolumab eklendi. Her bir kol için randomize edilen 304 hastada, nivolumab eklemesi, gemsitabin/sisplatin ile elde edilen 18,9 aylık ortanca genel sağkalıma kıyasla 21,7 aylık ortanca genel sağkalım sağladı, bu da yaşam kaybı riskinde %22'lik bir azalma anlamına gelmektedir (P = .0171).
Böylelikle immünoterapinin birinci basamak kemoterapiye eklenmesinin metastatik ürotelyal kanserde sağkalımı iyileştirdiği ilk kez gösterildi.
İleri evre mesane kanserinin birinci basamak tedavilerinde yıllar süren bir durgunluk yaşandıktan sonra, bu çalışmalar oldukça kıymetli bir ilerlemeyi temsil ediyor; zira her iki çalışma da, ilk seans tedavide kemoterapiyi aşmayı başardı.
Ancak, enfortumab vedotin / pembrolizumab kombinasyonu ile elde edilen çok daha iyi sağkalım oranları, bu kombinasyonun artık "ileri evre ürotelyal kanserler için en iyi ilk basamak tedavi rejimi olduğu" anlamına geliyor.
Tedavi Akışındaki Büyük Değişiklikler
Lokal olarak ileri veya metastatik idar yolu kanseri için yeni birinci basamak tedavi standardının belirlenmesi, mevcut tedavi yaklaşımlarında önemli değişikliklerin ve bir dizi yeni sorunun ortaya çıkmasını beraberinde getiriyor.
Öne çıkan başlıca konular arasında, daha önce birinci basamak tedavi standardı olarak belirlenen platin-tabanlı kemoterapinin, artık ikinci basamak tedavi seçeneği olarak mı düşünülmesi gerektiği bulunuyor. Eğer pembrolizumab birinci basamak tedavide başarısız olursa, pembrolizumab ve diğer immünoterapilerin daha önce belirlenmiş ikinci basamak tedavi standartlarındaki rolleri hala geçerli mi?
Ayrıca, gelecekte, enfortumab vedotin ve pembrolizumab kombinasyonunun daha erken evre hastalıklar için, özellikle de kas tabakasına yayılmış mesane kanseri gibi durumlar için uygun olup olmadığı, ve enfortumab vedotinin dozunun ve tedavi süresinin, göz gibi belirli yan etkileri azaltmak amacıyla azaltılıp azaltılamayacağı belirlenmesi gerekecek.
Son olarak elbette maliyeti tartışmalıyız. Enfortumab vedotin ve pembrolizumab (EV+P) oldukça maliyetli bir tedavi. Ülkeler ve geri ödeme kurumları bunu ne kadar karşılayabilecek?
EV-302/KEYNOTE-A39'un baş araştırmacısı Dr. Thomas Powles, geri ödeme müzakerelerinin nasıl gittiğini bilmediğini söyledi, ancak umuyor ki hızlı hareket edilir. Yeni tedavilerin kullanım onayı alması, ama geri ödeme almaması sorunları hakkında şöyle söylüyor: "Kanseri oldukça ileri evrede olan hastalar için bile çok anlamlı sonuçlar görüyoruz. Hastalarla bu veriler hakkında konuşmamak zor olacak."
EV-302/KEYNOTE-039 Detayları
Bu klinik çalışmada, pembrolizumab (P) 3 haftalık tedavi döngülerinin ilk gününde 200 mg dozunda verildi; toplamda en fazla 35 döngü gerçekleştirildi. Enfortumab vedotin (EV) ise döngünün ilk ve sekizinci günlerinde, hastalık ilerlemesi veya kabul edilemez toksisite gözlemlenene kadar, döngü sayısında herhangi bir sınırlama olmaksızın uygulandı.
Kontrol kolu olarak belirlenen sisplatin veya karboplatin (C) tedavisi ise ilk gün uygulandı ve gemcitabin (G) ilk ve sekizinci günlerde, en fazla altı adet 3 haftalık döngü boyunca verildi.
Hastaların performans durumlarına göre iki ayrı kol oluşturuldu ve her iki koldaki hastaların büyük bir kısmı performans durumları 0 veya 1 olarak değerlendirildi; her iki grupta da performans durumu 2 olan hastaların oranı %4'ten daha azdı.
Sonuçlar
Genel sağkalım sonuçlarına paralel olarak, progresyonsuz sağkalım (PFS) oranları da önemli farklar gösterdi.
- EV-P kombinasyonu ile tedavi edilen hastalar, ilerleme veya yaşam kaybı riskinde %55'lik bir azalma saptandı (P < .00001).
- EV-P kolunda ortanca genel sağkalım 31,5 ay iken, GC kolunda bu süre 16,1 ay idi.
- Ortanca progresyonsuz sağkalım EV-P grubunda 12,5 ay iken, GC ile tedavi edilen hastalar için bu süre 6,3 aydı.
Bu sonuçlar, PD-L1 pozitifliği, sisplatin uygunluğu ve visseral (iç organ) metastazın varlığı veya yokluğu göz önünde bulundurulmaksızın aynı kaldı.
Çalışmada, GC ile tedavi edilen hastaların neredeyse %60'ı, sonraki bakım veya hastalık ilerlemesi durumlarında bir immünoterapi tedavisine geçiş yaptı. EV+P ile tedavi edilen hastaların ise yaklaşık dörtte biri, sonraki aşamada platin tabanlı kemoterapi tedavisine geçiş yaptı.
EV+P grubunda tedavi gören deneklerin %55,9'unda 3. derece veya daha yüksek yan etkiler gözlemlendi, bu oran GC kolunda %69,5 olarak kaydedildi.
Kemoterapi kolunda en sık rastlanan yan etkiler; anemi, nötropeni, trombositopeni, yorgunluk ve mide bulantısı olarak belirlendi. EV+P grubunda ise en yaygın yan etkiler; deri reaksiyonları, hiperglisemi, nötropeni, periferik nöropati, ishal ve anemi şeklinde sıralandı.
CheckMate 901 Detayları
Bu faz 3, çok uluslu, açık etiketli çalışmaya, daha önce tedavi edilmemiş, cerrahi olarak çıkarılamaz veya metastatik ürotelyal kanserli hastalar rastgele seçilerek iki gruba ayrıldı. Birinci grup, altı döngüye kadar her 3 haftada bir nivolumab (360 mg dozunda) ile gemsitabin-sisplatin (nivolumab kombinasyonu) aldı, ardından maksimum 2 yıl boyunca her 4 haftada bir nivolumab (480 mg dozunda) aldı. İkinci grup ise altı döngüye kadar her 3 haftada bir sadece gemsitabin-sisplatin aldı. Ana hedefler genel ve progresyonsuz sağkalımdı.
Sonuçlar
Toplam 608 hasta randomize oldu (her grupta 304).
- Ortanca 33.6 aylık takip süresinde, nivolumab kombinasyon terapisi ile genel sağkalım, sadece gemsitabin-sisplatin ile karşılaştırıldığında daha uzundu; yaşam kaybı riskinde %22 azalma saptandı (yaşam kaybı için risk oranı, 0.78; %95 güven aralığı [CI], 0.63 ile 0.96; P=0.02).
- Ortanca sağkalım sırasıyla 21.7 ay (%95 CI, 18.6 ile 26.4) ve 18.9 ay (%95 CI, 14.7 ile 22.4) idi.
- Progresyonsuz sağkalım da nivolumab kombinasyon terapisi ile sadece gemsitabin-sisplatine göre daha uzundu (ilerleme veya yaşam kaybı risk oranı, 0.72; %95 CI, 0.59 ile 0.88; P=0.001).
- Ortanca progresyonsuz sağkalım sırasıyla 7.9 ay ve 7.6 ay idi.
- 12. ayda, progresyonsuz sağkalım sırasıyla %34.2 ve %21.8 idi.
- Nivolumab kombinasyon terapisi ile genel objektif yanıt %57.6 (tam yanıt, %21.7) ve sadece gemcitabin-sisplatin ile %43.1 (tam yanıt, %11.8) idi.
- Tam yanıtın 0rtanca süresi nivolumab kombinasyon terapisi ile 37.1 ay ve sadece gemsitabin-sisplatin ile 13.2 ay idi.
- 3. derece veya daha yüksek yan etkiler sırasıyla hastaların %61.8 ve %51.7'sinde meydana geldi.
*
Yazının görseli, "Onkoloji araştırmalarında önemli bir anı kutlamak için coşkuyla ellerini çırpan, hem erkek hem de kadın onkologlardan oluşan bir toplantının illüstrasyonu." komutu ile DALL-3'e tarafından oluşturulmuştur.
1. Powles TB, et al. EV-302/KEYNOTE-A39: Open-label, randomized phase 3 study of enfortumab vedotin in combination with pembrolizumab (EV+P) vs chemotherapy (chemo) in previously untreated locally advanced metastatic urothelial carcinoma (la/mUC). ESMO Congress 2023, LBA6
2. Van der Heijden MS, et al. Nivolumab plus Gemcitabine–Cisplatin in Advanced Urothelial Carcinoma. NEJM 22 October 2023.
3. Enfortumab Vedotin/Pembrolizumab Hailed As New Standard for Upfront mUC - Medscape - Oct 25, 2023.






