Kanser hücreleri birbiriyle nasıl iletişim kuruyor – kanserin kompleksitesi
Hücreler birbirleriyle iletişim kurmak için birbirlerine bağlanmak için sinyal ağları kurarlar. Bu sinyal ağları hücreler için protein sentezi, hücre mimarisi, farklılaşma ve apoptozis (planlanmış hücre ölümü) gibi önemli bilgileri taşır. Ayrıca hücre içerisinde bulunan sinyal ağları bilgiyi bütünleştirebilir, dağıtabilir ve uyarılara cevap verebilir. Sinyal ağlarının keşfi, kanser hücrelerinin anlaşılması ve tedavi edilmesinde büyük etkiler sahip olmuştur.
Kanser hücreleri sinyal ağlarında meydan gelen mutasyonlar tarafından oluşur. Bu nedenle vücudun oluşturduğu birçok savunma mekanizmasından kaçabilirler ve büyüme faktörü gibi bazı faktörleri kendi başlarına üretebilirler. Sinyal ağlarında iletilen sinyaller protein ve enzimler tarafından oluşturulur. Bu nedenle kanser hücrelerinin özellikleri araştırılırken protein ilişkilerine bakılır. İnsanda keşfedilen ilk protoonkogen (mutasyon sonucunda kansere sebep olan genlere verilen ad) Src’dir.
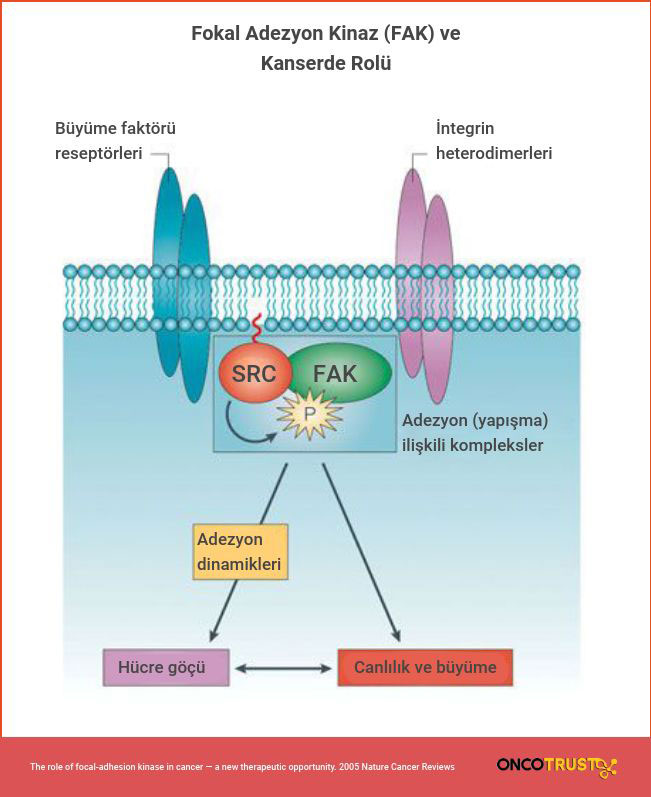
Src’nin FAK (fokal adezyon kinaz) ile ilişkisinin tümör hücrelerinin istilaları tarafından önemli bir rol oynadığı keşfedilmiştir. Src ve FAK hücrede hücre hareketiyle ilgilen kinazlardır (hedef proteine fosfat ekleyerek proteinin işlevini değiştir enzimler). Bazı durumlarda Src, FAK’ı fosforile (bir fosfat grubunun organik moleküle bağlanması) eder ve bazı sinyal proteinleri için kenetlenme alanı yaratır. Bu nedenle Src kinazlarının ve FAK’ın genetik olarak pasifleştirilmesi hücre hareketliliğini bozar. Bunun dışında Src ve FAK bazı invaziv (metastaz yapmış) kanserlerde yüksek eksperasyon (protein gibi ürünlerin üretilme süreci) sergiler. Bu gözlem Src ve FAK’ın hücre hareketliliği ve istilasındaki rolü için bazı kanıtlar sağlamıştır.
Margaret Frame, FAK’ın karsinojenezdeki (kanser oluşumu) rolünü anlamak için araştırmalar yapmış ve elde ettiği sonuçlarda FAK’ın kanserli hücrelerde protein seviyesinin başlangıç ve ilerlemesinde belirleyici olduğu anlaşılmıştır. Aynı araştırmada farklı olarak aktif Src’nin noninvaziv (metastaz yapmamış) kanserle eklendiği zaman kanseri invaziv hale getirdiği fark edilmiştir. Bunun dışında yapılan başka araştırmalarla birlikte çıkarılan ortak sonuç Src’nin hücre hareketliliğini ve tümör hücresinin büyümesini çoklu mekanizmalarla destekler. Fakat bu mekanizmaların çoğu FAK’a bağımlıdır (RAC’ın lokal aktivasyonu ve FISH’in fosforilasyonu FAK’tan bağımsızdır).
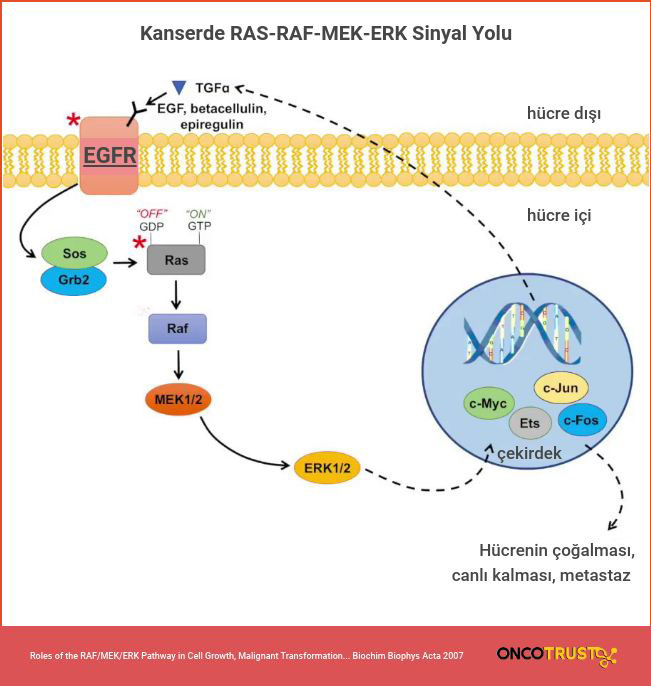
Bir diğer ilişki ise Ras-MAP ilişkisidir. Bu ilişki kanser hücrelerinin hedeflerinin belirlenmesinde rol oynar. Ras mutasyonlar tarafından aktif edilir ve 20’den fazla efektörle etkileşime girer. Serin / treonin Rafı, bir dizi onkogen Ras transformasyonu (bir hücrenin yabancı bir gene girmesi sonucunda o genin parçalanması) için gerekli olan MAP yolunu ve RAF-MEK-ERK yolunu aktifleştirir. Bu yollar kendi substratlarına (enzim tepkimelerinde işlenen madde) sahiptirler ve iskele proteinleri tarafından düzenlenirler. Map kinaz yolu Ets familyasında transkripsiyonları (bir DNA dizisinin RNA’ya aktarılması) aktive eder ve çoklu genlerin ekspresyonunu düzenler. EphA2 kinazı bazı enzimlerle birlikte vahşi tipli bir RAS’ı indirgemekte, mutasyonel olarak aktifleştirilmemiş RAS’ı düzenlemektedir. MAP kinazının aktivasyonu tümör hücrelerinde hayatta kalabilmeleri için önemli etkiye sahiptirler. MAP kinazının sinyalleri kaspaz 9 genine yeni hedefleri tarif eder. Kaspaz 9 ise kanser karşıtı faktörlerin bazılarını engeller. Bu nedenle kaspaz 9 Ras MAP ilişkisinin tümör hücrelerinin sağ kalımını teşvik ettiğini destekler niteliktedir. Bunların yanında p14 geni MAP’ın bazı tümör baskılayıcılardan kaçması için MAP kinaz aktivasyonunu lokalize edilmesine hizmet eder.
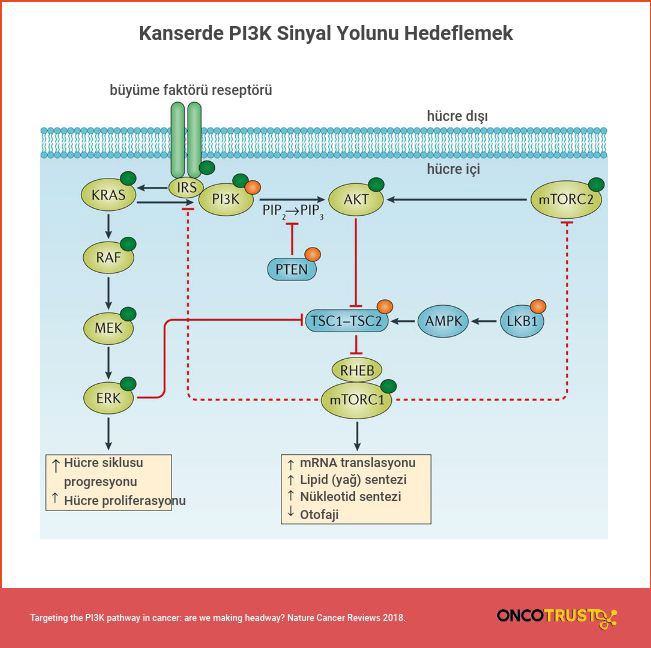
PI3 kinazı hücre büyümesinin, hareketliliğinin ve sağ kalımın düzenlenmesinde görev alır. PI3 kinazı lipit tanıma alanlarını içeren proteinleri zara dönüştüren fosfoinosititleri üretir. PI3 kinazının hücre büyümesini kontrol etmesi bir zincir şeklinde gerçekleştirilir. İlk PI3 kinazı PDK1’i ve AKT’ti üretir. AKT daha sonra mTOR kinazını aktive eder. mTOR çeviriyi 2 şekilde etkinleştirir. İlki proteinleri ve translasyon makinesinin diğer bileşenlerini şifreleyen 5-terminal oligopimidin kanal (TOP) mRNA’ların artmış çevirisine katılmış olan ribozomal S6 protein kinazını aktifleştirir ve başlangıç faktörü eIF4E’nin bir inhibitörü olan 4EBP-1’i etkisiz hale getirir. PI3 bu şekilde hücre büyümesini düzenler. Akt ve PI3 DNA ve RNA bağlayıcı bir protein olan YB-1 yeniden düzenler. YB-1’in mutant hali sitoplazma yerine çekirdeğe yerleşir ve transformasyonu bloke etmez. Bu da kanser hücrelerin çoğalmasına olanak sağlar. Son araştırmalar mTOR’un TSC-1 ve TSC-2 hormonları tarafından düzenlendiğini ortaya koymaktadır. Bu hormonlar büyüme inhibitörü ve tümör baskılayıcı olduklarından dolayı bu hormonlarda meydana gelen mutasyonlar başka organlarda sklerotik (sertleşmiş) tümörlere yol açabilir. PI3 kinazı hücre büyümesine olan etkisine ek olarak Akt ile kanserli hücrelerin hayatta kalmalarını ve metastazı destekleyebilir. PI3 kinazı Akt, Mad3, Myc ve s6 kinazı ile birlikte Ras kaynaklı hücre yaşlanmasına aracılık eder. Böylece kanser hücrelerine olan katkılarına ek olarak bir de koruyucu kontrol mekanizması geliştirir.
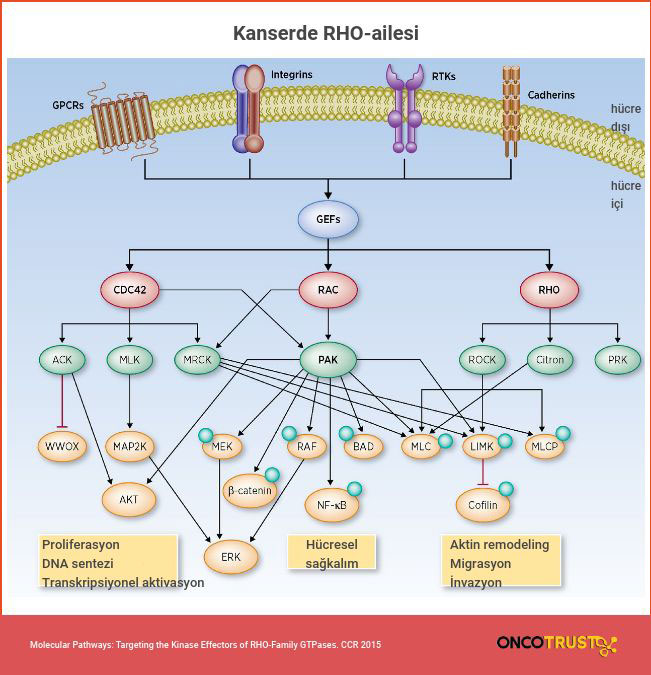
Rho ailesinde bulunan GTPazları aktivatörleri ve etkileyicileri ile kansere sebep olabilirler. GTPazları normal hücrelerde hücre hareketliliği ve hücre çoğalmasında görev alır. GTPazları dışında Rho ailesine mensup olan başka genler çeşitli kanserlerde görülür ve Rho, Rac, Ras, Cdc42 genleri için transformasyon için gereklidir. Channing Der’in yaptığı araştırmada Rac ve Ras geninin Tiam1 geniyle olan ilişkisi incelenmiştir. Rac GEF Tiam1 geni Ras bağlanma alanı içerir. Tiam1 eksikliği olan fareler Ras ve Rac kaynaklı kanserlere karşı dirençlidir. Bu çalışma Rho ailesinin üyelerinin onkogen olduğu anlaşıldı. Aktif edilmiş K-Ras taşıyan pankreas kanseri hücrelerinin bağımsız büyümesi hem aktive edilmiş Ras hem de Tiaml geninin sürekli ekspresyonuna bağlıdır. Başka bir örnek ise Rho’ya bağlı transformasyonlarda rol oynayan PAR1 geninin onkojenliğidir. Par1 aşırı üretildiğinde bir onkojene dönüşür ve bu durum RhoA fonksiyonuna bağlıdır. Ayrıca Rho ailesi mikrotübülleri de etkiler. Böylece RhoA, RhoB, Erk, Map, Cdc42, mDia2, MTOC ve ROCK gibi çeşitli kinazlarla birlikte hücre hareketinde ve kanser anında hücre hedeflenmesinde görev alır. WAVE ve Scar proteinleri GTPazlarının aktin hücre iskeleti üzerindeki etkilerine aracılık eden iskele protein grubudur. Bu proteinler GTPazlarını aktin filament düzeğini ayarlayan ve dallanmasını çekirdekleştiren Arp2 /3 kompleksine bağlar. WAVE proteinleri böylece hücre hareketliliğine yardımcı olurlar.
Bunlar gibi daha birçok protein ilişkisi kanserli hücrelerin iletişiminde görev alırken kanserli hücrelere bazı özellikler kazandırırlar. Halihazırda mutasyonlu genlerin bazıları için anti-kanser terapötikleri (tedavi ile ilgili olan) için olası hedefler yoğun bir şekilde araştırılmaktadır. Bu karmaşık sinyal mekanizması ve protein ilişkileri daha iyi anlaşıldıkça yeni kanser tedavileri oluşturulacaktır. Bu mekanizmalar sayesinde kanserin anlaşılması da artacağı için oluşturulan tedaviler daha etkili hale gelecektir. Böylece kanserde sağ kalım oranları artacaktır.