Küçük Hücreli Akciğer Kanserinde Serplulimab ile Şimdiye Kadar Alınan En İyi Sonuçlar
Küçük hücreli akciğer kanseri, akciğer kanserinin iki ana tipinden biridir ve hızlı büyüme ve erken yayılma eğilimi gösterir. Küçük hücreli akciğer kanseri (KHAK), genellikle yoğun bir şekilde sigara içenlerde görülür ve tüm akciğer kanserlerinin yaklaşık %15-20'sini oluşturur.
KHAK, mikroskop altında küçük boyutlu hücrelerin bir araya gelmesiyle oluşur. Diğer akciğer kanseri ana türü olan küçük hücreli dışı akciğer kanseri (KHDAK) ile karşılaştırıldığında, KHAK daha hızlı büyür ve yayılır. Bu nedenle, KHAK teşhisi konduğunda genellikle daha agresif bir tedavi planı uygulanır. KHAK çoğunlukla ileri evrelerde tanı alır ve erken metastaz yapma eğilimindedir.
Günümüzde ileri evre KHAK’nın standart tedavisi, Mart 2019’da atezolizumab immünoterapisinin FDA onayı alması ile değişmiştir ve artık birinci basamakta kemoterapi artı immünoterapi bilinen en etkili tedavi seçeneği haline gelmiştir. Bu yazıda ise ileri evre KHAK için yeni bir immünoterapi ajanı olan serplulimabdan bahsediyoruz.
Etken madde adı serplulimab olan Hansizhuang adlı immünoterapi, solid (doku/organ kaynaklı) tümörlerin tedavisi için Çinli Shanghai Henlius biyoteknoloji şirketi tarafından geliştirilen intravenöz olarak uygulanan bir anti-PD-1 antikorudur. Serplulimab, önceki standart tedavilere yanıt vermeyen ilerlemiş, ameliyatla çıkarılamayan veya metastatik mikrosatellit instabilite yüksek (MSI-H) solid tümörleri olan yetişkin hastaların tedavisi için Çin'de 25 Mart 2022'de ilk onayını aldı. Başvuruları bulunmakla birlikte henüz FDA (ABD Gıda ve İlaç İdaresi) ve EMA (Avrupa İlaç Ajansı) onayı almadı.
ASTRUM-005 Çalışması
27 Eylül 2022’de JAMA dergisinde Cheng ve arkadaşları faz III ASTRUM-005 çalışmasının bir ara analizini yayımladı: PD-1 inhibitörü serplulimabın kemoterapiye eklenmesinin, ileri evre küçük hücreli akciğer kanseri olan hastaların birinci basamak tedavisinde genel sağkalımı iyileştirdiğini gösterdiler.
Çalışma Detayları
Çift kör deney, Çin, Gürcistan, Polonya, Rusya, Türkiye ve Ukrayna'daki merkezlerden 585 hastayı içeriyordu. Toplamda, serplulimab grubundaki hastaların %67'si ve kontrol grubundaki hastaların %71'i Asyalı idi.
Sağkalım Verileri
Ara analiz için Ekim 2021'deki veri kesme noktasında ortanca takip süresi 12,3 aydı (aralık = 0,2-24,8 ay).

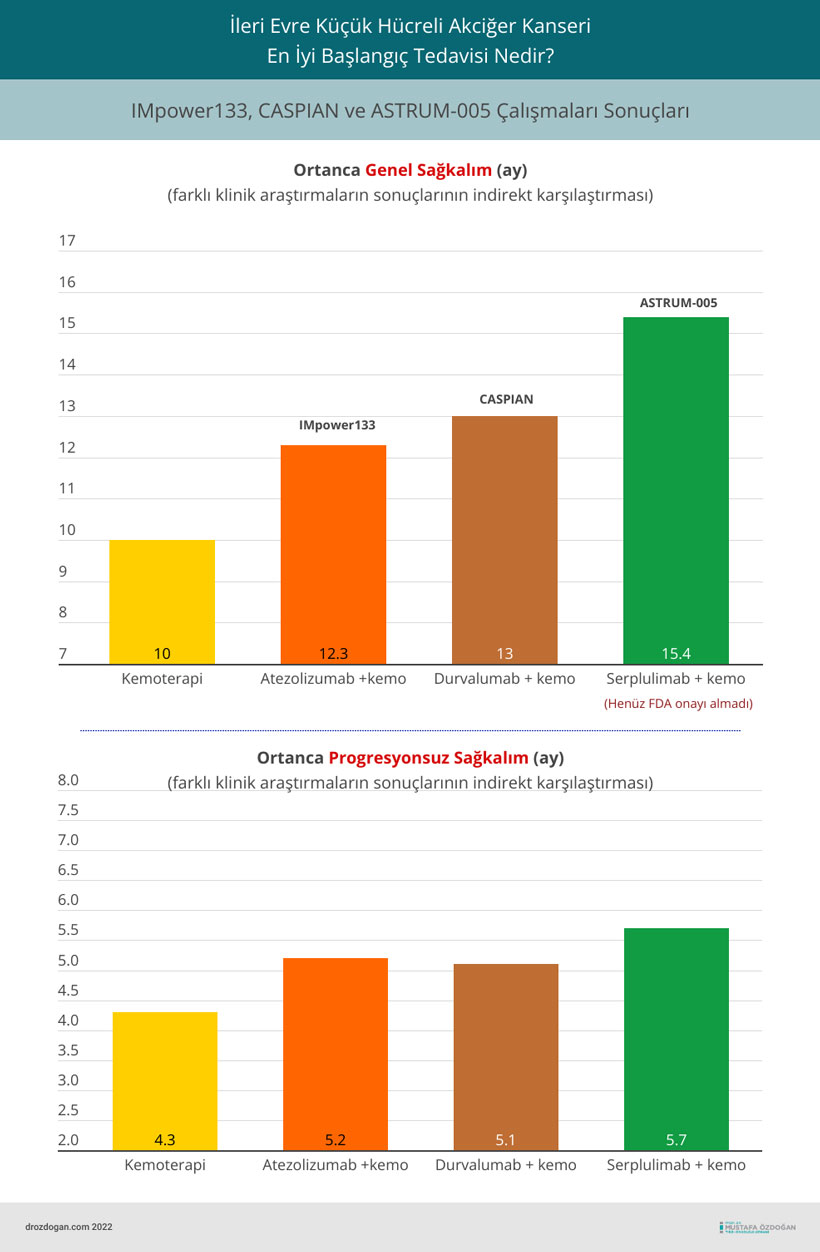
- Ortanca genel sağkalım, serplulimab grubunda 15,4 aydı (%95 güven aralığı [GA] = 13,3 ay – değerlendirilemez) ve kontrol grubunda 10,9 ay (%95 GA = 10,0–14,3 ay) (tehlike oranı [HR] = 0,63) , %95 GA = 0,49–0,82, P < ,001).
- Bağımsız radyoloji inceleme komitesi değerlendirmesinde ortanca progresyonsuz (ilerlemesiz) sağkalım, serplulimab grubunda 5,7 aydı (%95 GA = 5,5–6,9 ay) ve plasebo grubunda 4,3 aydı (%95 GA = 4,2–4,5 ay) (HR = 0,48, %95 GA = 0,38–0,59).
- Hastaların %70,4'üne karşı %80,2'sinde objektif yanıt, %0'a karşı %0,8'inde tam yanıt gözlendi.
- Ortanca yanıt süreleri 5,6'ya karşılık 3,2 aydı.
Yan Etkiler
Serplulimab grubundaki hastaların %33,2'sinde ve kontrol grubundakilerin %27,6'sında tedaviye bağlı derece ≥ 3 (ciddi) yan etkiler meydana geldi. Herhangi bir derecedeki immünoterapi ilişkili yan etkiler hastaların %18.4'üne karşı %37 oranında rapor edildi (derece ≥ 3, %9.5'e karşı %5.6); serplulimab grubunda daha yaygın olan yan etkiler arasında hipotiroidizm (%11,6'ya karşı %1,5) ve hipertiroidizm (%9,0'a karşı %3,1) vardı. Serlulimab'a atfedilen yan etkilere bağlı yaşam kaybı, akut koroner sendrom, pireksi ve azalmış trombosit sayısından oluşan nedenlerle üç hastada (%0,8) meydana geldi.
Yorum
İleri evre küçük hücreli akciğer kanseri (KHAK) başlangıç tedavisinde kemoterapiye immünoterapi eklenmesi artık standart yaklaşım olmuştur. Bu amaçla 2019'da atezolizumab (Tecentriq) ve 2020'de durvalumab (Imfinzi) FDA onayı aldı. Ülkemizde de bu amaçla hem atezolizumabın hem de durvalumabın T.C. Sağlık Bakanlığı ruhsatı vardır, fakat henüz geri ödeme kapsamına alınmamıştır.
İmmünoterapilerden önce bu durumdaki hastaların ortanca genel sağkalımı 10 ay civarında iken, günümüzde serplulimab ile 15 ayı geçtiğini görüyoruz.
Aşağıda, ileri evre KHAK birinci basamak tedavisinde dikkat çeken 3 çalışmanın sonuçlarının indirekt karşılaştırması görülebilir.
Cheng Y, Han L, Wu L, et al. Effect of First-Line Serplulimab vs Placebo Added to Chemotherapy on Survival in Patients With Extensive-Stage Small Cell Lung Cancer: The ASTRUM-005 Randomized Clinical Trial. JAMA. 2022