Yassı hücreli cilt kanseri tedavisi için immünoterapi pembrolizumab FDA onayı aldı
Cerrahi veya radyoterapi ile tedavi edilemeyen, tekrarlayan veya metastatik kutanöz skuamöz hücreli karsinomu (kSHK) olan hastalar için pembrolizumab (Keytruda) adlı immünoterapi ilacını, 24 Haziran 2020'de ABD Gıda ve İlaç İdaresi (FDA) onayladı.
Skuamöz/yassı hücreli cilt kanserleri, melanom-dışı cilt kanserleri arasında bazal hücreli karsinomdan sonra 2. sıklıkta yer almaktadır. Hayat boyu ortaya çıkma sıklığı %7-11 arasında değişmekte olup, her yıl dünya çapında %3-8 oranında artış göstermektedir.
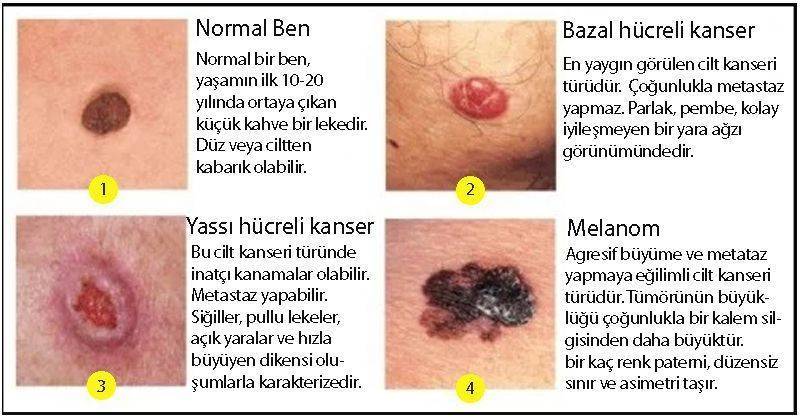
Aşağıdaki şekil: En sık görülen 3 cilt kanseri türü, normal bir ben ve özellikleri görülebilir.
KEYNOTE-629 çalışması
Etkinlik, çok merkezli, çok kohortlu, randomize olmayan, açık etiketli bir çalışma olan KEYNOTE-629'da araştırıldı. Çalışma daha önce bir anti-PD-1, anti-PD-L1 veya anti-CTLA-4 antikoru ile tedavi görmeyen, otoimmün hastalığı olmayan veya immünosupresyon gerektiren tıbbi bir durumu olmayan hastaları kapsadı. Hastalara hastalık ilerlemesi, kabul edilemez yan etkiye veya maksimum 24 ay olana kadar her 3 haftada bir 200 mg pembrolizumab verildi. Tümör durumunun değerlendirilmesi ilk yıl boyunca her 6 haftada bir ve ikinci yıl boyunca her 9 haftada bir gerçekleştirildi.
Başlıca etkinlik sonuç ölçütleri, bağımsız merkezi inceleme ile değerlendirilen objektif yanıt oranı ve yanıt süresiydi.
Objektif yanıt oranı %34 idi ve ortanca yanıt süresine ulaşılmadı.
KEYNOTE-629'a kayıtlı kutanöz skuamöz hücreli karsinom (kSHK) hastalarında görülen yan etkiler, diğer klinik çalışmalarda tek bir ajan olarak pembrolizumab alan hastalarda meydana gelenlere benzerdi (bakınız immünoterapi yan etkileri). Pembrolizumaba karşı en yaygın yan etkiler yorgunluk, kas-iskelet ağrısı, iştah azalması, kaşıntı, ishal, bulantı, döküntü, pireksi/ateş, öksürük, nefes darlığı, kabızlık, ağrı ve karın ağrısıdır. Pembrolizumab, pnömonit, kolit, hepatit, endokrinopatiler, nefrit ve cilt advers reaksiyonları gibi immün aracılı ciddi yan etkilerle de ilişkilidir.
kSHK için her 6 haftada bir 400 mg'lık bir dozaj kullanılarak pembrolizumabın etkinliği ve güvenliği, esas olarak, melanomlu hastalarda doz / maruziyet etkinliği ve güvenlik ilişkilerinin modellenmesine ve gözlemlenen farmakokinetik verilere dayanıyordu.
kSHK için önerilen pembrolizumab dozları, 3 haftada bir 200 mg veya 6 haftada bir 400 mg'dır.
FDA approves pembrolizumab for cutaneous squamous cell carcinoma.
fda.gov - 24 June 2020.