Yumurtalık Kanserinde PARP İnhibitörleri ve İkincil Lösemi Bağlantısı
Yeni bir araştırma, over (kadın yumurtalık) kanseri olan kadınlarda poli(ADP-riboz) polimeraz (PARP) inhibitörü tedavisinin ardından miyelodisplastik sendrom (MDS) veya akut miyeloid lösemi (AML) riskinde artış olduğunu doğruladı ve bu riski bireysel olarak tahmin etmeye yardımcı olabilecek potansiyel öngörücü faktörleri saptadı.
Yumurtalık kanseri, dünya genelinde kadınlar arasında en sık görülen jinekolojik kanserlerden biridir. Erken teşhisin zorluğu ve sıklıkla ileri evrede tanı konulması, bu hastalığın tedavisini karmaşık hale getirir. Tanı anında yumurtalık kanseri, genellikle karın içinde yayılım göstermiş durumdadır. Bu evrede kanser, sadece lokal tedavi yöntemleriyle kontrol altına alınamayacak kadar ilerlemiş olup, geniş kapsamlı sistemik tedaviler gerektirir. İleri evre hastalığın doğal seyri, tedaviye başta iyi yanıt vermesiyle birlikte, aylar-yıllar içinde tedaviye dirençli olmasıyla karakterizedir.
İlk FDA (ABD Gıda ve İlaç idaresi) onayını 2014'te alması ile birlikte kanser tedavi alanına giren PARP (poli(ADP-riboz) polimeraz) inhibitörleri, ileri evre yumurtalık kanseri tedavisinde devrim niteliğinde bir ilerleme olarak öne çıkmıştır. Bu ilaçlar, DNA onarım mekanizmalarını hedef alarak kanser hücrelerinin ölümünü tetikler ve özellikle BRCA mutasyonu taşıyan hastalarda daha etkili olduğu gözlemlenmiştir. PARP inhibitörleri, hastalığın ilerlemesini yavaşlatmak, yaşam süresini uzatmak ve hastaların yaşam kalitesini artırmak adına önemli faydalar sunar. Ancak, bu tedavilerin kendine özgü zorlukları ve potansiyel yan etkileri vardır; görece nadir olarak bu ilaçlara bağlı olarak gelişebilen ikincil hematolojik maligniteler (kan kanserleri), tedavi kararlarında önemli bir dikkat noktasıdır.
PARP inhibitörü Alanlarda İkincil Hematolojik Kanser Riski Ne Kadar?
Texas Üniversitesi MD Anderson Kanser Merkezi'nden Dr. Amma Asare tarafından, Society of Gynecologic Oncology 2024 Annual Meeting on Women's Cancer (Kadın Kanserleri Üzerine 2024 Jinekolojik Onkoloji Derneği Yıllık Toplantısı) sırasında yapılan bir sunumda, PARP inhibitörü ile ilişkili miyeloid neoplazmların "benzersiz klinik veya moleküler ilişkilere sahip olabileceğini" ve bu durumun riski belirlemeye yardımcı olabileceğini önerdi.
Bireysel hasta riskini anlamanın önemi, PARP inhibitörü tedavisiyle ilişkili ikincil hematolojik malignitelerin özellikle kötü hasta sonuçlarına sahip olmasıdır. Şu anda, riski tahmin etme yeteneği "sınırlı kalmaktadır."
Çalışma ekibi, 2000 ile 2022 yılları arasında kurumlarında herhangi bir jinekolojik kanser için tedavi edilen 32.356 hastayı tanımladı.
Tüm hasta grubuda ikincil MDS/AML oranı %1 civarında seyretti, bu da önceki raporlarla uyumluydu, diye belirtti Asare. Ancak, PARP inhibitörü ile tedavi edilen yumurtalık kanseri hastaları arasında bu oran yaklaşık on kat daha yüksekti (%9, 355 hastadan 32 vaka).
İkincil lösemi gelişenlerle gelişmeyenler karşılaştırıldığında, araştırmacılar, ikincil lösemi gelişenlerde, yumurtalık kanseri tanısından PARP inhibitörü ile tedaviye başlama süresinin daha uzun olduğunu buldular. PARP inhibitörü kullanımının toplam gün sayısı veya tedaviye başlama yaşı ile ilişki saptanmadı.
Kemoterapiyle ilişkili faktörlere bakıldığında, ikincil lösemi gelişen ve PARP inhibitörü tedavisi alan daha az hastanın neoadjuvan kemoterapi aldığı görüldü.
İkincil lösemi olanlarda daha fazla karboplatin döngüsü ve toplam kemoterapi hattı olduğu da belirtildi.
Hastalara özgü faktörlere bakıldığında, Asare ve meslektaşları, ikincil lösemi gelişenlerde, diğer tüm mutasyon tiplerine göre germline BRCA1 mutasyonlarında bir zenginleşme olduğunu belirttiler.
Ayrıca, ikincil lösemi gelişenlerde PARP inhibitörü tedavisi sırasında daha düşük minimum trombosit değeri vardı, ancak tedavi öncesinde trombosit minimumu veya PARP inhibitörü türü ile ilişki bulunmadı.
Çok değişkenli analiz, üç önemli faktörü belirledi:
- Neoadjuvan kemoterapi uygulanması koruyucu bir etki ile ilişkilendirildi (OR, 0.24; P = .017),
- PARP inhibitörü tedavisi sırasında düşük trombositler (OR, 0.99; P = .014) ve
- Daha yüksek toplam karboplatin döngüsü (OR, 1.15; P = .13) ikincil lösemi ile ilişkilendirildi.
Moleküler analiz, PARP inhibitörü ile tedavi edilen ve ikincil hematolojik kanser gelişen hastaların %68'inde TP53 mutasyonları olduğunu gösterdi.
Bu veriler, hem genetik hem de çevresel faktörlerin PARP [inhibitörü]-ilişkili hematolojik malignitede önemli roller oynadığını desteklemektedir.
Tedavi sırasında trombosit düşüşleri, "gelecekteki MDS/AML riskinin potansiyel bir göstergesi" olabilir. Bu değişiklikler, bireysel risk tahminini bilgilendirmek ve PARP inhibitörleri ile tedavi edilen hastaların kanıta dayalı yönetimi ve izlenmesini yönlendirmek için kullanılabilir.
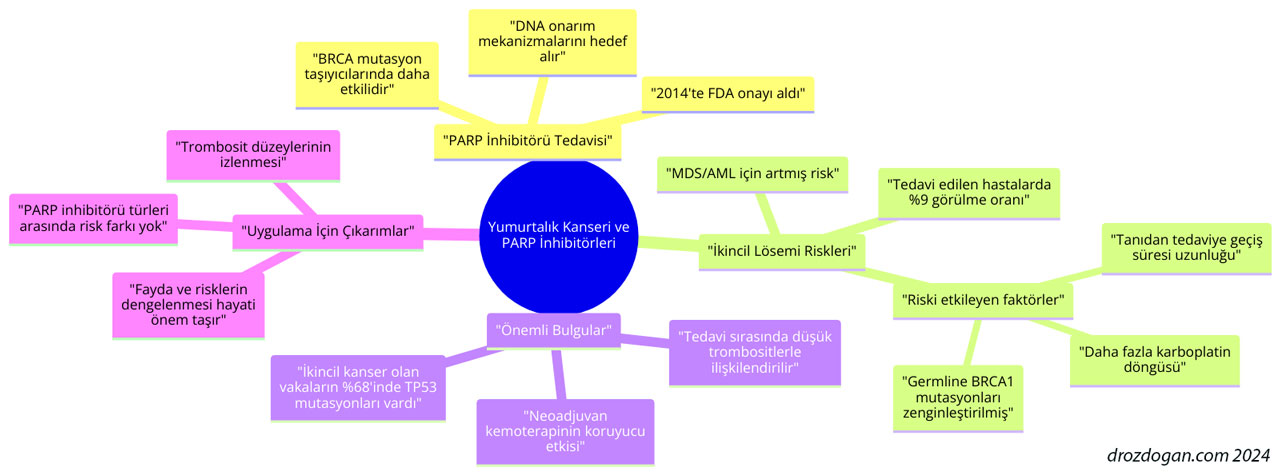
Aşağıda, "Yumurtalık Kanseri ve PARP İnhibitörleri" konusunu görselleştiren zihin haritası diagramı:
Risk-Fayda Dengesi
İkincil lösemi riskinde, PARP inhibitörü türü arasında fark saptanmadı.
PARP inhibitörü kullanım süresi ile MDS/AML riski artışı arasında bir ilişki olmamasının, bazı diğer denemelerden farklı olduğunu belirtmek önemlidir.
Lösemi gelişenlerde TP53 zenginleşmesi de "oldukça ilginç". Bu durum, PARP inhibitörü kullanımı ile artan MDS ve AML risklerinde TP53 klonal hematopoezinin potansiyel bir belirteci olup olamayacağı sorusunu gündeme getiriyor.
Sonuç olarak bugüne kadar elde edilen verilere göre, PARP inhibitörlerinin potansiyel riskleri ve toksisiteleri üzerinde dikkatle durmamız gerekmektedir. Bu tedavilerin sağladığı yararlar ile beraberinde getirebileceği riskler arasında dengeli bir yaklaşım benimsemek büyük önem taşımaktadır. Ayrıca, bu tedavilerden en iyi şekilde yararlanabilmek ve onların faydalarını daha kesin bir şekilde tespit edebilmek için daha gelişmiş biyobelirteçlere ihtiyaç duyulmaktadır.
1. Ovarian Cancer: Predicting Risk for Secondary Leukemia after PARPi Therapy - Medscape - March 22, 2024.