Hemofagositik lenfohistiyositoz tedavisi için Emapalumab FDA onayı aldı
Hemofagositik lenfohistiyositoz nedir?
Hemofagositik lenfohistiyositoz (HLH), vücutta sitokin denilen maddelerin aşırı salınması sonucu kontrolsüz hemofagositozun görüldüğü, nadir bir hematolojik (kan ve kemik iliği kaynaklı) hastalıktır. İlk kez 1952'de James Farquhar tarafından tanımlanmıştır ve 30 yıl öncesine kadar 5 yıllık sağkalım oranları % 10'larda iken, günümüzde % 70'ler civarındadır.
Ailevi / primer ve akkiz / sekonder (sonradan kazanılmış) olmak üzere iki formu vardır:
- Ailevi form, sıklıkla viral bir enfeksiyonun tetiklemesi ile bebeklik döneminde bulgu verir ve otozomal resesif olarak kalıtılır. Doğal öldürücü (NK) ve CD8 pozitif T-lenfositlerin kullandığı perforin/granzim sistemini ilgilendiren çeşitli gen defektleri sorumludur.
- Sekonder hemofagositik lenfohistiyositoz ise bu bilinen genetik mutasyonlar olmaksızın, bağışıklık sisteminin anormal derecede aktifleşmesi ile seyreden enfeksiyon, malignite (kanser) ve otoimmünite ile birlikte görülür.
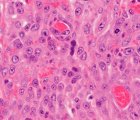
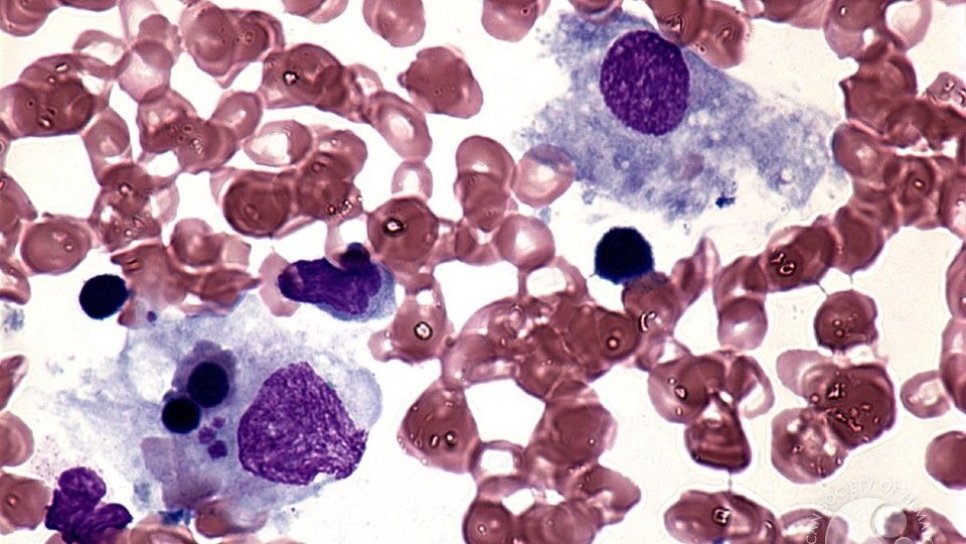
Hemofagositik lenfohistiyositoz her iki formunda da ortak olarak tanı belirtileri ateş, bisitopeni (kan düşüklüğü), hipertrigliseridemi (kanda yağ yüksekliği) ve/veya hipofibrinojenemi, hiperferritinemi, hemofagositoz, kanda yüksek serbest interlökin-2 reseptör (CD25) düzeyi, CD8+ T ve NK hücre aktivitesinde azalma veya kayıp ve splenomegalidir (dalak büyümesi).
Hemofagositik lenfohistiyositozun standart tedavisi kemoterapi ve kök hücre naklidir.
Emapalumab (Gamifant), FDA onayı ile hemofagositik lenfohistiyositozun standart tedavisinde
20 Kasım 2018'de, ABD Gıda ve İlaç İdaresi (FDA), mevcut tedavilere dirençli, tekrarlayan veya ilerleyici primer (ailevi) hemofagositik lenfohistiyositozlu (HLH) yetişkin ve pediatrik (çocuk) hastalar için interferon gamaya bağlanan ve nötralize eden bir monoklonal antikor olan Emapalumab'ı (Gamifant) onayladı.
Emapalumab'a FDA onayı getiren çok merkezli ve tek kollu klinik araştırmaya, 27 pediatrik HLH hastası alındı. Tüm hastalara başlangıç dozu olarak 3 günde bir 1 mg / kg emapalumab verildi. Tüm hastalara 5 ila 10 mg / m2 / gün dozunda deksametazon (kortizon) da verildi. Hastalar emapalumab uygulamasından önce, Herpes Zoster, Pneumocystis jirovecii ve mantar enfeksiyonları için profilaksi (koruyucu tedavi) aldı.
Çalışmanın sonucunda, tedaviye objektif yanıt oranı % 63 olarak bulundu (7 tam ve 8 kısmi yanıt vardı).
Hastaların en az % 20'sinde meydana gelen en yaygın yan etkiler enfeksiyonlar, hipertansiyon, infüzyonla (ilacın damar içine uygulanmasıyla) ilişkili reaksiyonlar ve pireksi (ateş) idi.
Önerilen başlangıç emapalumab dozu, haftada iki kez, en az 1 saatte, 1 mg / kg dozunda intravenöz (toplardamardan) infüzyondur. İlk doza müteakip dozlar klinik ve laboratuvar verilere göre artırılabilir.
FDA approves emapalumab for hemophagocytic lymphohistiocytosis.
fda.gov - 20 November 20 2018