
Beyin metastazlı HER-2 pozitif meme kanserinde etkili bir tedavi: Tucatinib
HER-2 pozitif metastatik meme kanseri hastalarının önemli bir kesiminde hastalıklarının gidişatında beyin metastazı görülebilmektedir. Bu hastalarda gelişen beyin metastazı için sistemik tedaviye ek olarak lokal hedefli tedaviler (cerrahi, stereotaktik radyocerrahi ve/veya tüm beyin radyoterapisi) hastalığın yönetiminde kullanılmaktadır. Ancak bu tedavi yaklaşımı, ASCO 2020’de sunulan çalışma ile değişeceğe benziyor. Tucatinibin trastuzumab ve kapesitabin ile üçlü kombine kullanılmasının bu hastalarda klinik olarak yararlı olduğunu gösterir bilimsel kanıt, HER2CLIMB klinik çalışmasının alt grup analiz sonuçları ile ortaya konuldu.
HER2CLIMB çalışması ve tucatinib
Toplamda 612 hastanın katıldığı HER2CLIMB; çok merkezli, randomize-kontrollü, çift-kör bir faz-III klinik çalışmadır. 2019 San Antonio Meme Sempozyumunda, daha önce trastuzumab, pertuzumab ve ado-trastuzumab emtansine (T-DM1) ile tedavi edilen, lokal ileri veya metastatik HER2 pozitif meme kanseri olan 612 hastada, tucatinibin trastuzumab ve kapesitabin ile kombinasyonunun sonuçlarının değerlendirildiği çalışma yer aldı. Ardından bu çalışma sonuçları, FDA’in 17 Nisan 2020’de tucatinib için verdiği onay için kanıt oluşturdu (bakınız).
Alt grup analiz dizaynı ve sonuçları
- HER2CLIMB’a alınan 612 hastanın 291’inde başlangıçta beyin metastazı ya da beyin metastazı hikayesi mevcut idi (tucatinib kolunda 198 hasta, kontrol kolunda 93 hasta).
- Tedavi edilmiş, stabil beyin metastazı olan hastaların sayısı başlangıçta, tucatinib kolunda 80, kontrol kolunda 37 idi. Aktif ilerleme gösteren beyin metastazı, tucatinib kolunda 118 hastada, kontrol kolunda 56 hastada mevcuttu. Her iki koldaki hastaların neredeyse tümünde (her iki kol için de yaklaşık %97), beyin dışında eş zamanlı eşlik eden hastalık vardı. Görülebileceği gibi hastalık özelliklerinin dağılımı, genel çalışma randomizasyonu (rastgele dağıtım) olan 2:1 ile uyumlu idi.
- Santral sinir sistemi (SSS) için olan 1 yıllık progresyonsuz sağkalım süresinin (PFS, yeni tedaviden itibaren hastalığın kötüleşmesine,ilerlemesine kadar olan süre) gözlendiği hasta oranı, tucatinib kolunda %40,2 (%95 CI; %29,5–%50,6) iken kontrol kolunda bu oran %0 idi. Ortanca SSS-PFS tucatinib kolunda 9,9 ay, kontrol kolunda 4,2 ay idi.
- İntrakranial (kafa içi) hastalık ilerleme veya ölüm riski tucatinib kolunda %68 daha az bulundu (HR, 0,32; %95 CI; 0,22–0,48).
- Ölüm riski tucatinib kolunda %42 az bulundu (OS için HR, 0,58; %95 CI; 0,40–0,85). Ortanca genel sağkalım, tucatinib uygulanan hastalarda 18,1 ay; kontrol grubunda 12 ay idi.
- Tucatinib kolunda intrakranial tedavi yanıtı (ORR-IC) kontrol kolundan daha yüksek idi. Tucatinib kolunda tam ORR-IC %5,5 hastada, kısmi ORR-IC %43,6 hastada görüldü.
- Hem aktif beyin metastazı hem de stabil beyin metastazı olan hastalarda, SSS-progresyonsuz sağ kalımda ve ortanca genel sağ kalım içim tucatinibin yarar sağladığı görüldü fakat bir tek ortanca genel sağkalım, stabil beyin metastazı olan hastalarda istatistiksel anlamlılığa ulaşamadı (1 yıllık hesaplanmış OS stabil metastazlı hastalarda tucatinib kolunda %67,6; kontrol kolunda ise %55,6 [HR, 0,88; %95 CI; 0,45–1,70; p= .696]).
Çalışmanın anlamı
Özet olarak bu alt-grup analizi, daha önceden tedavi almış (T-DM1, pertuzumab, trastuzumab) beyin metastazı olan HER-2 pozitif meme kanseri hastalarında tucatinibin transtuzumab ve kapesitabine eklenmesinin, intrakranial tedavi yanıt oranını iki katına çıkardığını, SSS progresyonu veya ölüm riski oranını 3’te 2 oranında azalttığını ve ölüm riskini yaklaşık yarı yarıya azalttığını gösterdi. Tucatinib, yukarıda bahsedilen özelliklere sahip hastalarda antitümör etkinliği randomize kontrollü klinik çalışma ile gösterilen ilk tedavi ajanı oldu.
Tucatinib etki mekanizması nasıldır?
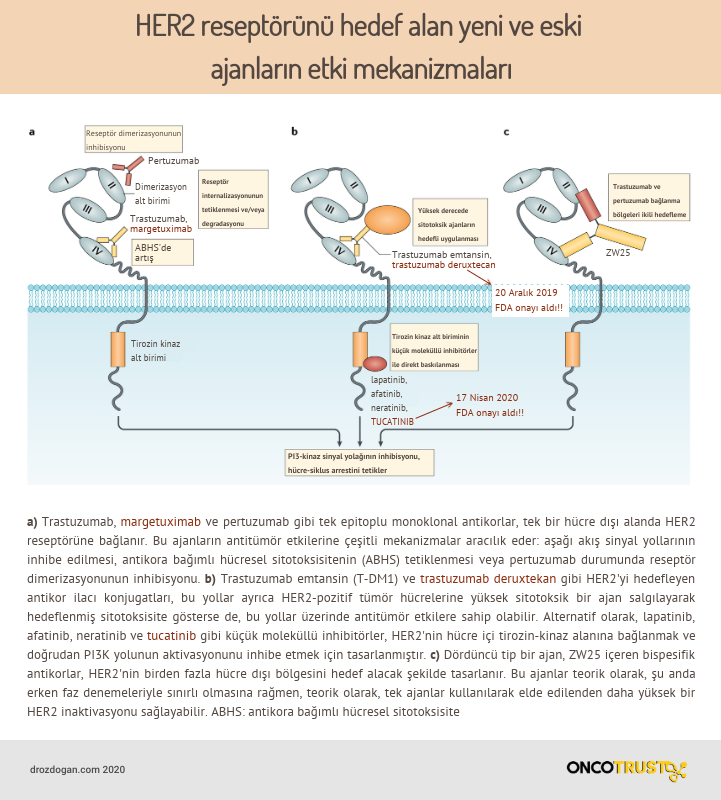
HER-2 (human epidermal büyüme faktörü resptörü-2), EGFR (epidermal büyüme faktörü reseptörleri) ailesinin üyesi olan bir tirozin kinaz reseptördür. Bu aile üyeleri; EGFR (HER 1/erbB1), HER2 (neu/erbB2), HER-3 (erbB3) ve HER-4 (erbB4)’ü içerir. Hücre zarındaki bu reseptörlere bağlanan farklı ligandlar (ilgili uyarıyı hücre dışında taşıyan molekül) sonucunda reseptörler dimerize olur ve hücre içi bir dizi sinyal molekülünün aktivasyonu başlatılır. HER-2 hücre zarında bir diğer HER-2 (homodimer) ile veya HER-3 (heterodimer) ile dimer (ikili yapı) oluşturabilir.
Günümüzde kullanılan trastuzumab ve pertuzumab bu reseptöre karşı geliştirilmiş monoklonal antikorlardır (Trastuzumab bir HER-2’ye bağlanarak etki gösterir iken Pertuzumab, reseptör dimerizasyonunu bozar). Böylelikle hem bu reseptörlerin aracılık ettiği yolaklar bloke edilir hem de antikor bağımlı hücresel sitotoksisite–bağışıklık yanıtı oluşturulur. Ado-trastuzumab-emtansin ise sitotoksik bir ilaç olan DM1’in trastuzumaba bağlandığı bir büyük molekül ilaçtır.
Bunların dışında, tirozin kinaz reseptörlerin aktivitesini bozan ilaçlar mevuttur. İşte tucatinib, HER2 reseptör tirozin kinaza yüksek özgüllükle etki eden reverzibl (geri dönüşümlü), küçük moleküllü bir inhibitördür. Tucatinibin, EGFR ailesindeki diğer epidermal büyüme faktörlerine kıyasla HER-2’ye yüksek özgüllük göstermesi önemlidir (HER-2 için diğer EGFR’lere göre 1000 kattan fazla etkinlik göstermektedir). Tucatinib HER-2 aktivitesini engelleyerek, MAPK ve PI3K/AKT gibi aşağı yönlü hücre içi sinyal yolaklarının işlevini durdurur. Böylelikle tümör hücrelerinin kontrolsüz hücre bölünmesi, sağ kalım yeteneği ve metastaz olasılığı azaltılır.
Lin, N. U., et al. (2020). "Intracranial Efficacy and Survival With Tucatinib Plus Trastuzumab and Capecitabine for Previously Treated HER2-Positive Breast Cancer With Brain Metastases in the HER2CLIMB Trial." J Clin Oncol: JCO2000775.
Kulukian, A., et al. (2020). "Preclinical Activity of HER2-Selective Tyrosine Kinase Inhibitor Tucatinib as a Single Agent or in Combination with Trastuzumab or Docetaxel in Solid Tumor Models." Mol Cancer Ther 19(4): 976-987.






