
HER2 pozitif meme kanserinde tedavi akışını değiştirecek çalışma
Meme kanserinin HER2 pozitif olarak adlandırılan alt türünün tedavi akışını değiştirecek önemli bir çalışmanın sonuçları 4-8 Aralık 2018 tarihleri arasında ABD Teksas'ta gerçekleşen San Antonio Meme Kanseri Sempozyumu'nda sunuldu ve eş zamanlı olarak NEJM'de yayımlandı.
KATHERINE adlı bu faz-3 klinik araştırmanın sonucuna göre, neoadjuvan (ameliyat öncesi küçültücü) tedavi olarak kemoterapi ve akıllı ilaç trastuzumab (Herceptin) aldığı halde, rezidüel hastalığı kalan, yani tümörü tam olarak kaybolmadığı ameliyat patolojisi ile anlaşılan erken evre meme kanserli hastalara, ameliyat sonrası koruyucu amaçlı trastuzumab yerine ado-trastuzumab emtansine (T-DM1; Kadcyla) verilmesi, kanserin tekrarı veya meme kanserine bağlı yaşam kaybı riskini % 50 azaltmakta.
Trastuzumab Emtansine nedir, nasıl çalışır?
Diğer adı T-DM1 olan ado-trastuzumab emtansine, iki farklı ilacın kombinasyonundan oluşur:
- T: trastuzumab (hedefe yönelik akıllı ilaç)
- DM1: hücrenin iskeleti mikrotübüller üzerine etkili bir kemoterapi ilacı
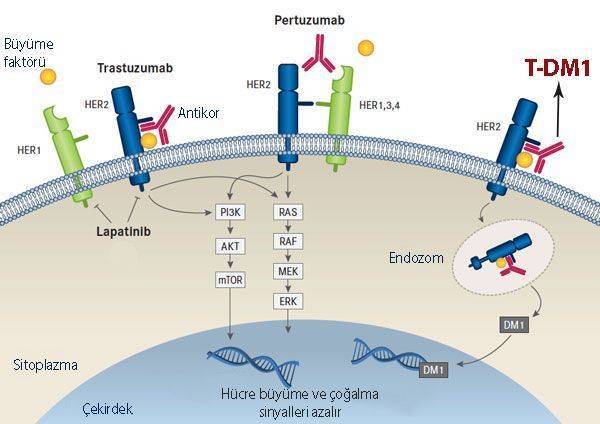
Resmin açıklaması: Kadcyla, insan epidermal büyüme faktörü reseptörü 2 (HER-2) olarak bilinen meme kanseri hücrelerinin yüzeyindeki bir reseptörü hedef alır. Protein yapıdaki bu reseptöre bağlandıktan sonra, hücrelere girer ve hücrenin büyümesini veya bölünmesini durduran DM-1 adlı bir kimyasal maddeyi serbest bırakır.
Kadcyla, 2013'de ileri evre meme kanseri için FDA onayı almıştı.
KATHERINE çalışmasının detayları ve sonuçları
- Yaklaşık 1500 HER2 pozitif meme kanserli hastanın dahil edildiği oldukça büyük çaplı bir klinik araştırma gerçekleştirildi.
- Tüm hastalar, tanı anında HER2 pozitif erken meme kanserine sahipti. Tümör boyutu T1 ila T4, nodal evre N0 ila N3 ve metastazı olmayan hastalardı (meme kanserinde evreleme için bakınız). T1aN0 veya T1bN0 evreye sahip hastalar çalışmaya alınmadı. Ayrıca, antrasiklin ile veya antrasiklin olmadan bir taksanlı kemoterapi ve en az 9 haftalık trastuzumab dahil olmak üzere neoadjuvan tedaviyi tamamladıktan sonra, ameliyatta memede veya aksillada (koltuk altı) rezidüel hastalık olan hastalar çalışmaya dahil edildi. Daha sonra hastalar, ameliyat sonrası 14 kür adjuvan tedavi (bir gruba T-DM1, diğerine trastuzumab) verilmek üzere rastgele iki kola ayrıldı.
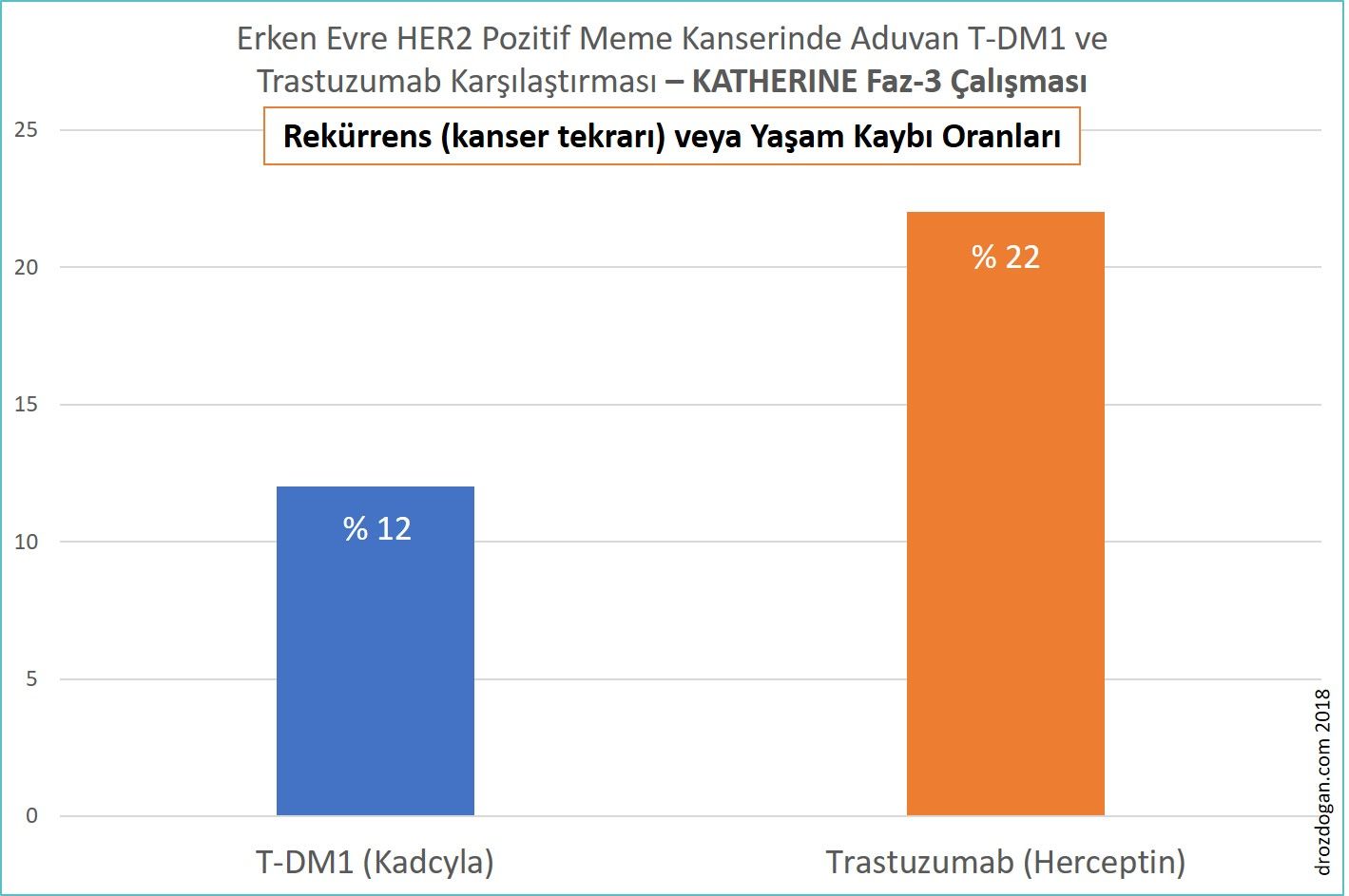
- Araştırmanın erken bir analizinde, T-DM1 grubundaki 743 hastanın 91'inde (% 12) ve trastuzumab grubundaki 743 hastanın 165'inde (% 22) kanser tekrarı veya yaşam kaybı meydana geldi (bakınız aşağıdaki şekil).
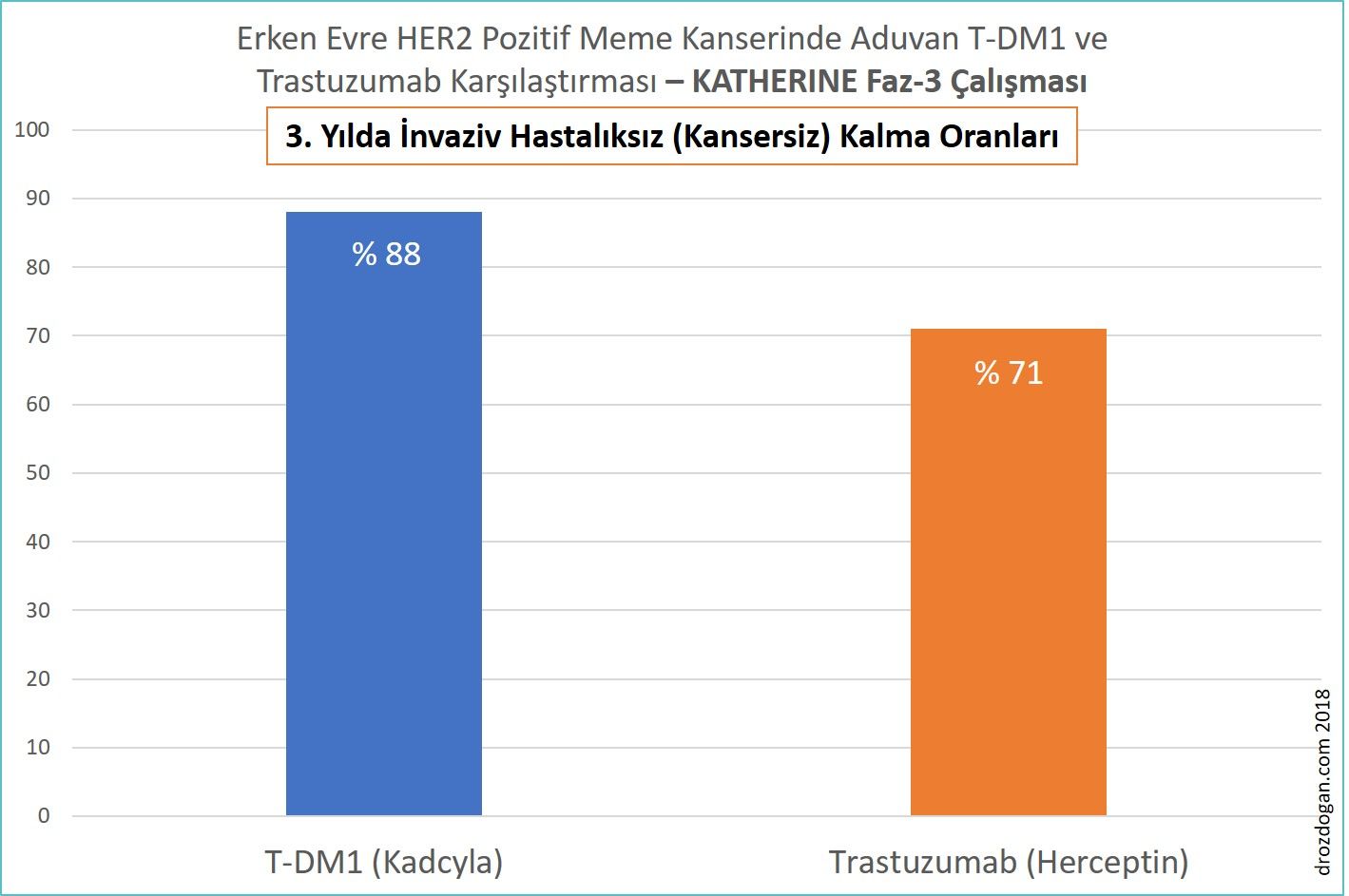
- 3. yılda kansersiz olma oranları T-DM1 grubunda % 88, trastuzumab grubunda % 77 idi. Bu % 11'lik oran, erken evre meme kanseri için oldukça dikkat çekicidir (bakınız aşağıdaki şekil).
- T-DM1'in faydası;
- Hem hormon reseptör pozitif ve negatif
- Hem farklı rezidüel hastalık düzeylerinde
- Hem de neoadjuvan rejimde tek veya çift anti-HER2 hedefli tedavi alanlarda benzer şekilde gözüktü.
- Daha da önemlisi, uzak organ metastazı, T-DM1 alan 78 hastada (% 10.5) ve trastuzumab alan 118 hastada (% 15.9) ortaya çıktı. Ancak, beyin metastazları açısından fark saptanmadı.
- Genel sağkalım yararını belirlemek için daha uzun takip gereklidir. Halen ortanca takip süresi yaklaşık 41 aydır. Bu noktada T-DM1 grubunda 42, trastuzumab grubunda 56 yaşam kaybı vardı.
- Yan etkiler açısından karşılaştırıldığında ise, T-DM1 grubunda yan etkiler, bu ilacın önceki çalışmalarında bildirilenlere benzer idi. 14 kürlük tedavi için trastuzumab alan hastaların % 81'i, T-DM1 alan hastaların ise % 71'i tamamlayabildi. T-DM1 grubundaki hastaların %18'i ve trastuzumab grubundaki hastaların %2'sinde, yan etkiler sebebi ile tedavide kesilme oldu. Bununla birlikte T-DM1 grubundaki yan etkilerin çoğu geçici ve yönetilebilir bulundu. Örneğin, el ve ayak uçlarında duyu kusuru (periferal nöropati), T-DM1 grubundaki hastaların %19'unda gelişmekle birlikte, hastaların sadece %5'inde bu yan etki ciddi düzeyde idi.
Bir diğer anti-HER2 tedavi olan pertuzumab (Perjeta) hakkında bazı fikirler
HER2 pozitif meme kanserli hastaların ameliyat öncesi küçültücü tedavisinde, trastuzumabın yanına pertuzumab (Perjeta) eklenmesinin tedavi başarısını artırdığının gösterilmesi üzerine, 2013 yılında pertuzumab neoadjuvan tedavi için FDA onayı almıştı. Bu onaydan sonra HER2 pozitif meme kanserinin standart neoadjuvan tedavisi, ikili anti-HER2 uygulama olmuştu. KATHERINE çalışmasında ise hastaların az bir kısmının (% 18) standartlaşmış neoadjuvan tedavi olan pertuzumab alması, bu çalışmanın zayıf bir yönü olarak görülebilir. Bir başka soru ise, neoadjuvan tedavi olarak ikili anti-HER2 tedavi alan hastaların, ameliyat sonrası T-DM1'e geçip geçmemesi gerektiğidir. Bu sorunun cevabı "evet" olabilir, çünkü pertuzumab ile patolojik tam bir yanıt yoksa, bu hastaların pertuzumabdan faydalanmayacağı olasıdır.
Sonuç olarak KATHERINE çalışması, T-DM1'in ameliyat sonrası kullanımı için çok değerli bilgiler sunmaktadır ve olasılıkla HER2 pozitif erken evre meme kanserinin klinik pratiğini değiştirecektir.
G. von Minckwitz ve ark.
Trastuzumab Emtansine for Residual Invasive HER2-Positive Breast Cancer.
NEJM, December 2018.






