Trastuzumab Derukstekan (Enhertu) Nedir? FDA Onayı, Türkiye Ruhsatı ve Geri Ödeme Durumu
Enhertu (Trastuzumab Deruxtecan), HER2 hedefli tedavilerde çığır açan, antikor-ilaç konjugatı (ADC) sınıfında bir "akıllı bomba" teknolojisidir. 2025 yılı sonu itibarıyla FDA, bu ajanın Pertuzumab ile kombinasyonunu, metastatik HER2-pozitif meme kanserinin birinci basamak tedavisinde yeni standart olarak onaylamıştır.
Bu dosya; ilacın etki mekanizması, farmakolojik özellikleri, DESTINY-Breast09 verileri, Türkiye'deki ruhsat durumu ve yan etki yönetimini kapsar.
- Etken Madde: Trastuzumab deruxtecan (T-DXd)
- Sınıf: Antikor-İlaç Konjugatı (ADC)
- Üretici: Daiichi Sankyo / AstraZeneca
- Uygulama: İntravenöz (IV)
- Endikasyon: Metastatik HER2(+) Meme Kanseri 1. Basamak
- Rejim: Enhertu + Pertuzumab
- Sonuç: Klasik THP rejimine göre üstün PFS.
- Ruhsat: Var (Meme, Akciğer, Mide).
- Geri Ödeme: Yok (SGK kapsamında değil).
- Enhertu 100 mg flk fiyatı : 41.112,14TL. Maliyet: Yaklaşık 164,448,56 TL / kür (70 kg için).
Enhertu Nedir? Nasıl Çalışır?
Enhertu, HER2 reseptörüne bağlanan bir monoklonal antikor (Trastuzumab) ile buna bağlı güçlü bir kemoterapi ajanının (Deruxtecan - DXd) birleşimidir.
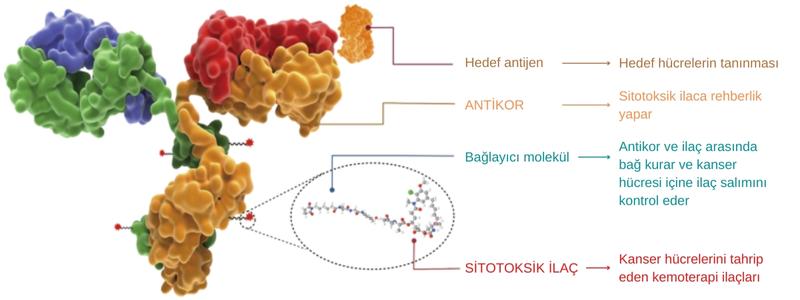
- Mekanizma: İlaç, HER2 pozitif kanser hücresine yapışır ve içine alınır. Hücre içinde bağlayıcı kopar ve kemoterapi (DXd) serbest kalarak DNA sentezini bozar.
- Seyirci Etkisi (Bystander Effect): DXd, hücre zarından geçebilir. Böylece ilacı alan kanser hücresi ölürken, ilaç dışarı sızarak yandaki HER2 negatif kanser hücrelerini de öldürür. Heterojen tümörlerdeki başarısının sırrı budur.
HER2 Durumu Ne Anlama Gelir?
Patoloji raporlarında HER2 durumu İmmünohistokimya (İHK) ile belirlenir:
- 0: Negatif.
- 1+: HER2-Düşük (Low) Pozitif. (Enhertu bu grupta da etkilidir).
- 2+: Şüpheli. (FISH testi ile doğrulanmalıdır).
- 3+: Tam Pozitif. (Klasik hedef kitle).

Enhertu sadece İntravenöz (IV) yolla uygulanır. Oral yoldan alındığında biyoyararlanımı yoktur.
Plazma proteinlerine bağlanma oranı yaklaşık %97 düzeyindedir.
- Trastuzumab bileşeni: Katabolizma yoluyla küçük peptidlere ve amino asitlere parçalanır.
- Deruxtecan (DXd): Karaciğerde esas olarak CYP3A4 enzimi aracılığıyla metabolize edilir.
- Yarı Ömür: DXd bileşeninin yarı ömrü yaklaşık 5.8 gündür.
İlaç Etkileşimleri: Mevcut klinik veriler ışığında bildirilmiş belirgin bir ilaç-ilaç etkileşimi bulunmamaktadır. Ancak CYP3A4 inhibitörleri ile birlikte kullanımında dikkatli olunması genel farmakolojik prensip olarak önerilir.
- HER2 reseptörünün hücre yüzeyindeki yoğunluğunun azalması (down-regülasyon) veya mutasyonlar.
- Antikor-ilaç konjugatının tümör hücresi içine alımının (internalizasyon) bozulması.
- Lizozomal yıkımın yetersiz kalması sonucu DXd (kemoterapi yükü) salınımının azalması.
- p95HER2 formunun ekspresyonunun artışı.
- 15 Aralık 2025 (YENİ): Metastatik HER2-pozitif meme kanserinde 1. Basamak tedavi olarak Pertuzumab ile kombinasyonu onaylandı. (DESTINY-Breast09).
- 6 Nisan 2024: Tümör türünden bağımsız (Tümör Agnostik) olarak, daha önce tedavi görmüş tüm metastatik HER2-pozitif solid tümörler için onaylandı.
- 27 Ocak 2024: HER2 düşük veya ultra-düşük meme kanserinde, endokrin tedavi sonrası kullanım onayı genişletildi.
- 12 Ağustos 2022: HER2-mutant Küçük Hücreli Dışı Akciğer Kanseri (KHDAK) için onaylanan ilk ilaç oldu.
- 6 Ağustos 2022: "HER2-Düşük" (HER2 Low) metastatik meme kanseri tanımıyla onay alan tarihteki ilk ajan oldu.
- 15 Ocak 2021: İleri evre Mide Kanseri (Gastrik) tedavisi için onaylandı.
- 20 Aralık 2019: İlk FDA onayı (Metastatik meme kanserinde 3. basamak ve sonrası).
Enhertu ülkemizde ruhsatlıdır ancak geri ödeme listesinde değildir. Ruhsatlı olduğu ana endikasyonlar:
- HER2 Pozitif: Daha önce en az bir basamak tedavi almış, inoperable veya metastatik hastalık.
- HER2 Düşük: Daha önce kemoterapi almış metastatik hastalık.
Enhertu 3 haftada bir (21 günde bir) IV infüzyon olarak uygulanır. Dozaj kanser türüne göre değişir:
- Meme Kanseri, Akciğer Kanseri ve Tümör Agnostik: 5.4 mg/kg
- Mide (Gastrik) Kanseri: 6.4 mg/kg
- Enhertu: 5.4 mg/kg (21 günde bir)
- Pertuzumab: İlk doz 840 mg (Yükleme), sonraki dozlar 420 mg (İdame).

🚨 En Önemli Risk: İnterstisyel Akciğer Hastalığı (İAH)
Enhertu kullanan hastalarda akciğer dokusunda inflamasyon (pnömonitis) gelişebilir. Erken teşhis hayat kurtarır.
| İAH Derecesi | Belirtiler | Yönetim |
|---|---|---|
| Grade 1 | Belirti yok, sadece tomografide görülür. | İlacı kes. Steroid başla. Düzelirse tekrar başla. |
| Grade 2-4 | Öksürük, nefes darlığı, ateş. | Enhertu KALICI OLARAK BIRAKILIR. Yüksek doz steroid başla. |
Diğer Sık Yan Etkiler
- Bulantı/Kusma: Yüksek/orta risklidir. Koruyucu ilaç şarttır.
- Miyelosupresyon: Nötropeni (beyaz kan düşüklüğü) ve anemi.
- Kardiyotoksisite: Kalp pompalama gücünde (LVEF) azalma. (3 ayda bir EKO yapılmalı).
- Alopesi: Hastaların yaklaşık yarısında saç dökülmesi görülür.
Enhertu, Türkiye'de eczanelerden temin edilebilir ancak SGK geri ödeme kapsamında değildir. Hastalar genellikle endikasyon dışı onay aldıktan sonra ilacı kendi imkanlarıyla temin etmekte veya hukuki süreç başlatmaktadır.
- Kutu Fiyatı (100 mg flakon): 41.112,14 TL
- Örnek Hesaplama (70 kg hasta):
Doz: 5.4 mg/kg x 70 kg = 378 mg.
Gereken miktar: 4 kutu (400 mg). - Bir Kür Maliyeti: Yaklaşık 164,448,56 TL
- Not: Fiyatlar döviz kuruna ve ilaç kararnamesine göre değişkenlik gösterebilir.
- FDA Approval Announcement, Dec 15, 2025. Fam-trastuzumab deruxtecan-nxki with pertuzumab.
- Cortés J, et al. DESTINY-Breast09 Trial Results.
- Modi S, et al. Trastuzumab Deruxtecan in Previously Treated HER2-Low Advanced Breast Cancer (DESTINY-Breast04). N Engl J Med 2022.
- Enhertu (fam-trastuzumab deruxtecan-nxki) Kısa Ürün Bilgisi (KÜB), TİTCK.
- T.C. Sağlık Bakanlığı, Türkiye İlaç ve Tıbbi Cihaz Kurumu (TİTCK) İlaç Fiyat Listesi.
Chu, Edward; DeVita Jr., Vincent T.. Physicians' Cancer Chemotherapy Drug Manual 2024.






