İdrar yolu (mesane ve üreter) kanseri idame tedavisinde immünoterapi avelumab FDA onayı aldı
Metastaz yapmış veya bölgesel olarak tümörü ilerlemiş ürotelyal (idrar yolu = üreterler ve mesane) kanseri olup, birinci basamak platin içeren kemoterapiye yanıt veren hastaların tedavisi için avelumab (Bavencio) adlı immünoterapi ilacını, 30 Haziran 2020'de ABD Gıda ve İlaç İdaresi (FDA) onayladı.
Avelumabın ürotelyal kanserin idame tedavisinde etkili olup olmadığını değerlendirmek için, JAVELIN Bladder 100 adlı klinik araştırma gerçekleştirildi. Randomize, çok-merkezli, açık etiketli bu çalışmaya, tümörü bölgesel olarak ilerlemiş veya metastatik ürotelyal kanserli 700 hasta dahil edildi. Bu hastalar daha önce 4 veya 6 döngü platin-bazlı kemoterapi almıştı ve bu tedavi altında kanserleri ilerlememişti.
Hastalar 1'e 1 oranında 2 kola rastgele ayrıldı; deney koluna en iyi destekleyici tedavi artı avelumab uygulanırken, kontrol koluna sadece en iyi destek tedavi uygulandı. Tedavi, son kemoterapi dozundan 4-10 hafta sonra başlatıldı.
Çalışmadan ölçülmek istenen başlıca etkinlik sonuç ölçütleri tüm hastalarda ve PD-L1 pozitif tümörleri olan hastalarda genel sağkalım idi.
- Tüm hastalar için, ortanca genel sağkalım, avelumab kolunda 21.4 ay ve sadece en iyi destekleyici tedavi kolunda 14.3 aydı.
- Hastaların %51'ide PD-L1 pozitifti ve bu hastalarda immünoterapi avelumab kullanımı, yaşam kaybı riskini %44 azalttı.
- PD-L1-negatif tümörleri hastalarda avelumab kullanımı, yaşam kaybı riskini %15 azalttı.
Avelumab alan hastaların >% 20'sinde en sık görülen yan etkilker yorgunluk, kas-iskelet ağrısı, idrar yolu enfeksiyonu ve döküntüdür. Bir hasta sepsisten (ciddi enfeksiyon) öldü ve hastaların %28'inde ciddi yan etkiler vardı (bakınız immünoterapi yan etkileri).
Önerilen avelumab dozu, hastalığın ilerlemesine veya kabul edilemez yan etki gelişene kadar her 2 haftada bir 60 dakika boyunca intravenöz infüzyon olarak 800 mg'dır.
Avelumab, daha önce 2017 yılında Merkel hücreli karsinom, 2017 yılında ileri evre ürotelyal karsinom, 2019 yılında aksitinib ile kombine şekilde ileri evre böbrek kanseri tedavilerinde olmak üzere 3 FDA onayı almıştı.
*
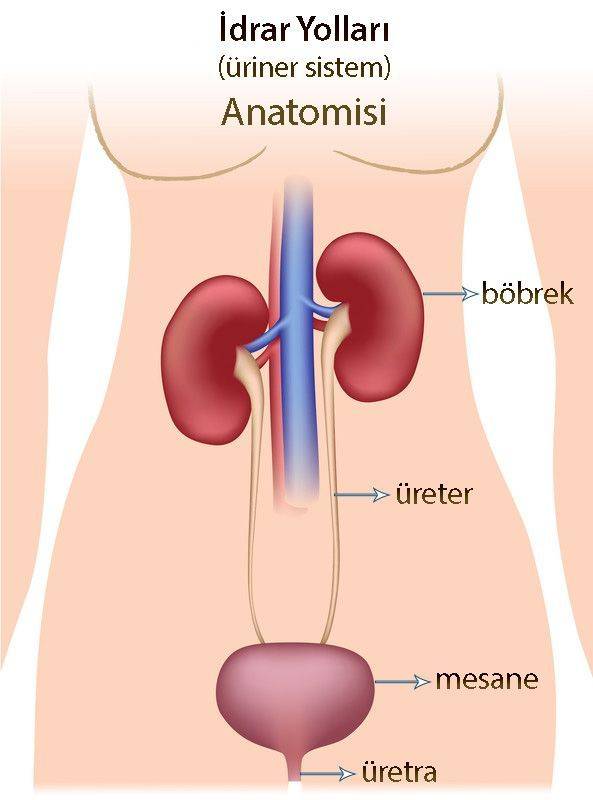
İdrar yolu organları; böbrekler, üreterler (böbrekler ile mesane arasındaki tüpler), mesane (idrar kesesi) ve üretradan (mesaneyi vücut dışına bağlayan kanal) oluşur. Ürotelyal kanserler, "böbrekler dışındaki" idrar yolu organlarını kapsamaktadır.
FDA approves avelumab for urothelial carcinoma maintenance treatment.
fda.gov - 02 July 2020