Trodelvy (sacituzumab govitecan-hziy) FDA Onayı, Türkiye Ruhsatı ve Geri Ödeme Durumu
İlaç Hakkında
- FDA onaylı: Evet (İlk onay tarihi 22 Nisan 2020)
- Kutu adı: Trodelvy
- Etken madde adı: Sacituzumab govitecan-hziy
- Uygulama şekli: İntravenöz enjeksiyon
- Sınıfı: Antikor-ilaç kojugatı
- Kategori: Biyolojik yanıt modifiye edici ajan, kemoterapi ilacı
- Üretici: Immunomedics, Inc.
- Türkiye dağıtımı: Gilead Sciences İlaç LTD. ŞTİ.
- Onaylı olduğu kanserler: Meme kanseri, ürotelyal (idrar yolları ve mesane) kanser
Sacituzumab govitecan-hziy Etki Mekanizması Nasıldır?
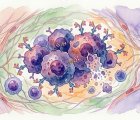
- Bir topo I inhibitörü olan SN-38'e konjüge edilmiş Trop-2'ye yönelik hümanize monoklonal antikor sacituzumab, bir antikor-ilaç konjugatıdır. Her bir antikor molekülüne yaklaşık 7-8 SN-38 molekülü konjuge edilir.
- Trop-2'ye bağlandıktan sonra sacituzumab govitecan hızla lizozomlara içselleştirilir ve daha sonra topo I proteinini hedeflemek ve inhibe etmek için hücrede SN-38 salınır. Topo I'in inhibisyonu, çift sarmallı DNA kırılmalarına ve nihai hücre ölümüne yol açar.
- Trop-2, hücre büyümesini ve proliferasyonunu, invazyonu, hücre hayatta kalmasını ve karsinogenezi uyarmak için ERK/MAPK ve siklin D1 sinyal yolları aracılığıyla çalışan 46-kDa'lık bir transmembran kalsiyum sinyal proteinidir.
- Trop-2, meme kanseri de dahil olmak üzere birçok epitelyal solid tümörde aşırı eksprese edilir ve ekspresyonu, üçlü negatif meme kanserinin %85'inden fazlasında tespit edilir.
Trodelvy için FDA Onayı Zaman Çizelgesi
- 3 Şubat 2023: Sacituzumab Govitecan, Hormon Pozitif HER2 Negatif İleri Evre Meme Kanseri için FDA Onayı Aldı
- 13 Nisan 2021: İleri Evre Ürotelyal (mesane-idrar yolu) Kanseri için Sacituzumab Govitecan FDA Onayı Aldı
- 22 Nisan 2020: Sacituzumab Govitecan-hziy, İleri Evre Üçlü Negatif Meme Kanseri Tedavisinde FDA Onayı Aldı
Trodelvy için Türkiye Ruhsatı
Trodelvy, ilk olarak 25.01.2023 tarihinde aşağıdaki endikasyonla T.C. Sağlık Bakanlığı Ruhsatı almıştır.
Terapötik endikasyonları
- Aktif beyin metastazı olmayan,önceden en az iki basamak kemoterapialmış (en azbir basamağı metastatik evrede alma şartıyla),rezeke edilemeyen lokal ilerlemiş veya metastatik üçlü negatif meme kanseri olan yetişkin hastaların tedavisinde endikedir.
- CDK4/6 inhibitörü içeren endokrin bazlı tedavi almış ve metastatik evrede en az iki basamak sistemik kemoterapi almış rezeke edilemeyen lokal ilerlemiş veya metastatik, hormon reseptörü (HR) pozitif, insan epidermal büyüme faktörü reseptörü 2 (HER2) negatif (IHC0,IHC1+ veya IHC2+/ISH–) meme kanseri olan yetişkin hastaların tedavisinde endikedir.
Trodelvy Geri Ödemesi Var mı?
Trodelvy, aşağıda tarif edilen durum için Sosyal Güvenlik Kurumu (GSK) tarafından geri ödeme kapsamına alınmıştır.
"Aktif beyin metastazı olmayan, önceden en az iki basamak kemoterapi almış, rezeke edilemeyen lokal ileri veya metastatik triple negatif meme kanseri olan hastalarda progresyona kadar kullanılır."
Fiyatı: Trodelvy 200 mg flk: 68.568,53 TL
Bir kürlük maliyeti: Yaklaşık 60 kg bir insan için ; 205,705,59 TL dir.
Direnç Mekanizması
Henüz iyi bir şekilde tanımlanmadı.
Dağılım
İlacın plazma proteinlerine orta düzeyde bağlanması (%77). Kararlı durum ilaç seviyelerine 21 gün içinde ulaşılır.
Metabolizma
Sacituzumab govitecan ile resmi bir metabolizma çalışması yapılmamıştır, ancak antikor-ilaç konjugatının küçük peptidlere ve amino asitlere yıkılıyor olması beklenmektedir. SN-38, karaciğerde UGT1A1 tarafından metabolize edilir. Sacituzumab govitecanın ortanca terminal yarı ömrü 16 saattir ve serbest SN-38'in terminal yarı ömrü yaklaşık 18 saattir.
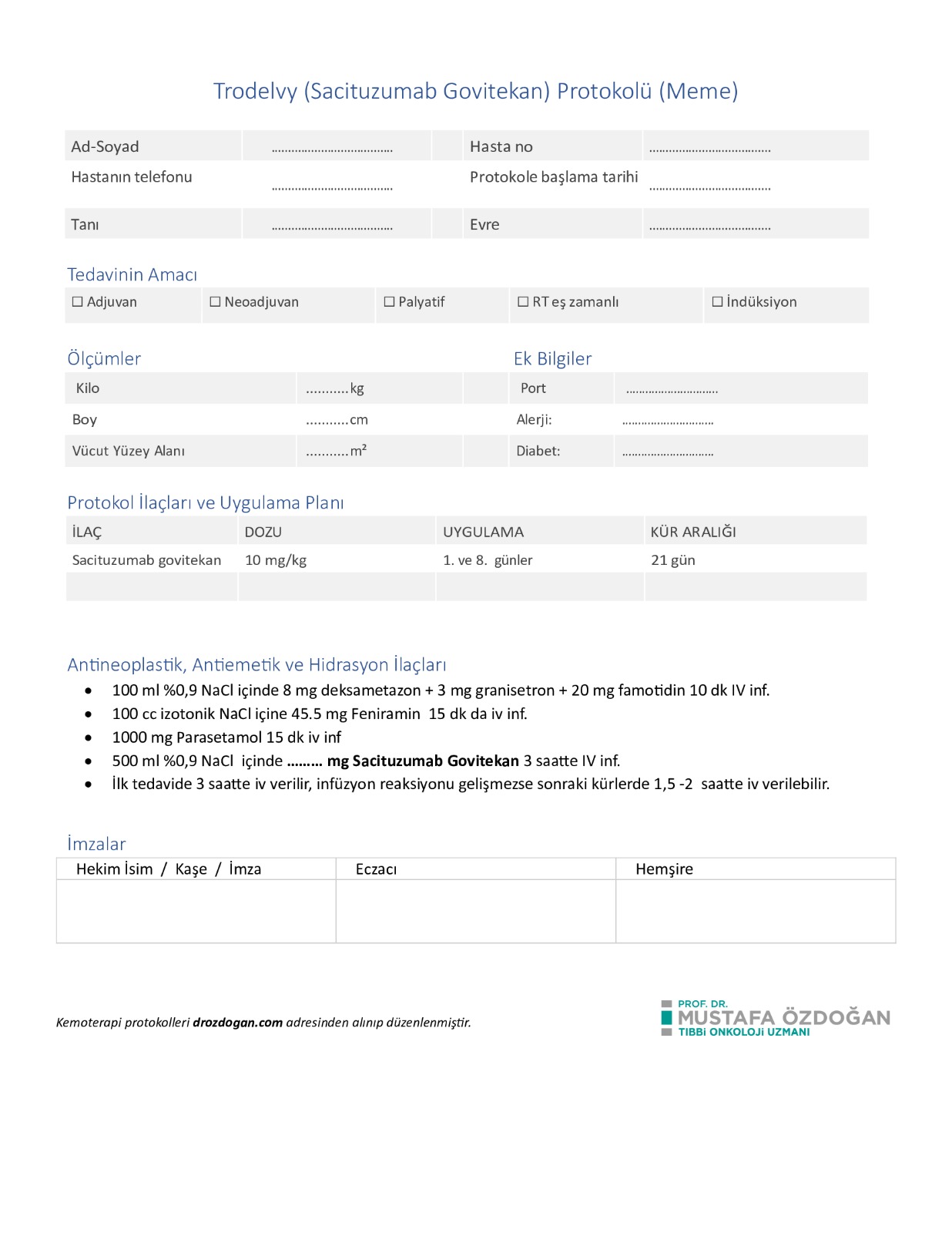
Doz ve Uygulama
| Başlık | Ayrıntı |
|---|---|
| Standart doz | 10 mg/kg IV, Gün 1 ve 8; her 21 günde bir döngü. |
| İnfüzyon süresi | İlk doz ≈ 3 saat; iyi tolere edilirse sonraki dozlar 1–2 saat. |
| Uygulama şekli | IV yavaş infüzyon; IV push/bolus kesinlikle DEĞİL. İlk dozdan sonra ≥ 30 dk gözlem. |
| Premedikasyon | Antiemetik + H1/H2 bloker ± antipiretik; önceki infüzyon reaksiyonu varsa steroid eklenebilir. |
Yan Etkiler
Miyelosupresyon / Nötropeni
En sık görülen yan etki. Şiddetli/yaşamı tehdit eden nötropeni olabilir. Tam kan sayımı ile yakın izlem ve gerektiğinde doz geciktirme/azaltma ve G-CSF değerlendirilir.
İshal (Erken & Geç)
Erken: infüzyon sırasında/≤24 s (kızarma, terleme, kramp) → atropin düşünülebilir. Geç: >24 s, genelde 3–10 günde başlar; G3–4 ≈ %10, tüm dereceler ≈ %60. İlk gevşek gaitada loperamid; 24 s düzelmezse PO florokinolon; refrakterse IV hidrasyon/antibiyotik ve yatış.
GİS / Diğer
Bulantı-kusma (genelde dozla ilişkili), anoreksi, yorgunluk, iştahsızlık, alopesi.
Aşırı Duyarlılık / İnfüzyon Reaksiyonları
Premedikasyon (H1/H2 ± antipiretik, gerekirse steroid). Reaksiyonda hız azaltma/geçici durdurma veya medikal tedbir.
Özel Durumlarda Dikkat
- UGT1A1*28 (7/7) genotipi: Miyelosupresyon ve ishal açısından yüksek risk — daha sık TKS ve erken destek tedbirleri.
- Karaciğer fonksiyon bozukluğu: Hafif bozuklukta tipik olarak doz değişikliği gerekmez; orta/ağır bozuklukta çalışma verisi kısıtlı olduğundan kaçınılmalıdır.
- Böbrek yetmezliği: Veri kısıtlı; son dönem böbrek hastalığında dikkat.
- Gebelik & Emzirme: Fetotoksisite riski; üreme potansiyeli olan kadınlarda tedavi süresince ve son dozdan en az 2 ay sonrasına kadar, erkek partnerlerde 4 ay kontrasepsiyon. Emzirme önerilmez.
- İnfüzyon tekniği: Yalnızca IV yavaş infüzyon (push/bolus değil); ilk dozdan sonra ≥30 dk gözlem.
- İlaç etkileşimleri: UGT1A1 inhibitörleri (SN-38 ↑ → toksisite ↑) ve indükleyicileri (SN-38 ↓ → etkinlik ↓) ile eşzamanlı kullanımdan kaçının veya yakın izleyin.
Kaynaklar
Chu, Edward; DeVita Jr., Vincent T.. Physicians' Cancer Chemotherapy Drug Manual 2022. Jones & Bartlett Learning.